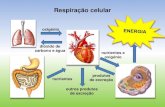
Sistema Respiratório. Tipos de respiração: –Respiração celular –Respiração pulmonar.
2ª e 3ª etapas da Respiração Celular
-
Upload
adriana-quevedo -
Category
Health & Medicine
-
view
27.045 -
download
0
Transcript of 2ª e 3ª etapas da Respiração Celular

CICLO DE KREBS

Continuou os trabalhos Carl y Gerty Cori sobre a hidrólise do glicogênio e a conseqüente geração de ácido láctico. Usando músculo peitoral de pombo, integrou os elementos reconhecidos do processo num único esquema coerente conhecido como ciclo do ácido cítrico ou ciclo de Krebs. Esta descoberta lhe rendeu o Prêmio Nobel de Fisiologia e Medicina em 1953.


1ª parte: CONVERSÃO DO PIRUVATO À ACETIL CoA
(ELO DE LIGAÇÃO DA GLICÓLISE AO CICLO DO ÁCIDO CÍTRICO)
C
C
O-O
CH3
O CSO CoA
CH3+
CO2
CoA-SHNAD+
TPP, lipoato,FAD
NADH
E1 + E2 + E3
PIRUVATO ACETIL CoA
HS CH2 CH2 N
H
C
O
C C N C
H
C
O
C
H
CH2
OH
O
CH3
P
CH3 O-
O
O
P
O
O-
CH2 O
HH
O
H
P
OH
O-O
O-
H
N
N
N
N
NH2
Coenzima A

Características do COMPLEXO DA PIRUVATO DESIDROGENASE
Complexo multienzimático (agregado de 3 enzimas);
Localizado na mitocôndria dos eucariotos e no citossol dos procariotos;
Canalização de substratos;
Cofatores: TPP, FAD, Coenzima A, NAD+, lipoato;
Vitaminas essenciais no processo: tiamina (no TPP), riboflavina (no FAD) , niacina (no NAD+), pantotenato (na CoA);
Cinco reações consecutivas de descarboxilação e desidrogenação do piruvato até Acetil-CoA.

COMPLEXO PIRUVATO-DESIDROGENASE

2ª parte: CICLO DO ÁCIDO CÍTRICO propriamente dito
Sinônimos: ciclo de Krebs, ciclo dos ácidos tricarboxílicos
Ocorre na mitocôndria dos eucariotos e no citossol dos procariotos;
Sequência cíclica de oito passos;
Em cada volta entra um grupo acetil-CoA e saem duas moléculas de CO2.
Na verdade, os carbonos que entram pelo Acetil-CoA não são os mesmos liberados na forma de gás carbônico na mesma volta. São necessárias algumas voltas adicionais para que isto ocorra.

CICLO DO ÁCIDO CÍTRICO
Não há conversão líquida de acetato a oxaloacetato.

Acetil-CoA
1CH3 CO
S CoA +C CH2C
O-
OC
O-
O
O
Oxaloacetato
H2O
CoA-
SH CH2
C
CO
O-
CH2
CHOO
O-
CO
O-
Citrato
H2C
C
COO-
C
COO-
COO-
H
Cis-aconitato
H2O
3
acon
itase
Citrato sintase
H2C
C
COO-
C
COO-
COO-
H
H
HO
Isocitrato
H2O
acon
itase
CH2
CH2
COO-
C COO-
O
NAD +
NADH + H +-Cetoglutarato
isocit
rato
desid
roge
nase
CoA-
SH
NAD
+
NAD
H
CO2+
CH2
CH2
CO
O-
C S
O
CoA
Succinil-CoAcomplexo
-cetoglutaratodesidrogenase
GDP+Pi
GTP
CoA-SH
CH2
CH2
CO
O-
C O-
OSuccinato
succ
inil-
CoA
sint
etas
e
-OOC C
H
C
H
COO-
FAD
FADH2
Fumarato 2
2
4
5
6
-OOC C C COO-H
H
OH
H
-OOC C C COO-
O H
H
NAD+
NADH
H2O
Malato
Oxaloacetato
mal
ato
desi
drog
enas
e
fumarase
CO2+

A energia liberada pela oxidação é conservada na forma de coenzimas reduzidas: 3NADH e 1FADH2.
Quando se tratam de processos metabólicos, interessa ao organismo um grande número de passos para que a liberação de energia se dê gradualmente.
Com a oxidação direta de toda a molécula, a energia produzida seria muito grande, causando danos à célula e/ou prejudicando o aproveitamento eficaz da energia liberada.

Deficiência genética
Mutação dos genes das subunidades da piruvato desidrogenase
Deficiência de tiamina (vit. B1)
Tiamina pirofosfato é o grupamento prostético da piruvato desidrogenase, a ceto-glutarato desidrogenase e transcetolase.
BERIBÉRI: perda parcial das funções neurais (problemas de memória, desorientação e coma), níveis de piruvato no sangue
Bebidas alcoólicas (calorias vazias), dieta pobre ou mal absorção.
*arroz branco

ETAPAS REGULATÓRIAS piruvato desidrogenase: inibida por ATP, NADH, acetil-
CoA etc. citrato sintase: inibida por ATP, NADH, citrato etc. isocitrato desidrogenase: ATP etc. α-cetoglutarato desidrogenase: NADH, succinil-CoA etc.
VIA DO GLIOXALATO Vegetais, certos invertebrados, E. coli e outros; Variação do ciclo do Ácido Cítrico; Síntese líquida da glicose a partir de lipídeos (succinato
entra no ciclo de novo);

4 Reações anapleróticas
VIA ANFIBÓLICA
Os principais desvios são:
-Utilização do citrato na síntese de ácidos graxos e esteróis;
-Desvio do alfa-cetoglutarato para formação de aminoácidos ou bases nitrogenadas;
-Utilização do succinil-coA na síntese de porfirinas;
-Formação de pirimidinas a partir de oxaloacetato via aspartato e asparagina;
-Neoglicogênese e síntese de aminoácidos a partir do oxaloacetato via piruvato.

FOSFORILAÇÃO OXIDATIVA
A fosforilação oxidativa é o processo pelo qual se forma ATP quando se transferem elétrons do NADH ou do FADH2 para o O2
(redução a H2O), por uma série de transportadores de elétrons.
NADH FADH2
NAD+ FAD
e-
O2
H20

Mitocôndria (organelas de forma oval com cerca de 2µm de comprimento e 0,5 µm de largura).membrana externa porina permeabilidade;membrana interna impermeável a quase todos os íons e moléculas polares;matriz enzimas do ciclo do ácido cítrico, da β-oxidação e da oxidação dos aminoácidos.

CADEIA TRANSPORTADORA DE ELÉTRONS
Experimentos com detergentes sobre a Membrana Mitocondrial Interna (MMI) demostraram que:
os transportadores de elétrons (com exceção da ubiquinona e do citocromo c), estão organizados em 4 grandes complexos protéicos.
Complexo I - NADH-Q redutase
Complexo II – Succinato-Q redutase;
Complexo III – Citocromo redutase;
Complexo IV – Citocromo oxidase.

O fluxo de elétrons pelos complexos I, III e IV, leva ao bombeamento de 4, 2 e 4 prótons através da membrana, respectivamente. O complexo II, ao contrário dos outros complexos, não bombeia prótons.
Forma-se então um gradiente ácido e positivo no espaço intermembranas da mitocôndria.

Complexo 1NADH Ubiquinona;Os Prótons que acompanham os elétrons são lançadospara o espaço intermembranas.* Neuropatia óptica hereditária de Leber.

Complexo 2participa a enzima do ciclo do ácido cítrico, produzindoFADH2;
Succinato Ubiquinona;

Complexo 3
Ubiquinona Citocromo c;
Os Prótons que acompanham os elétrons são lançados para o espaço intermembranas.

Complexo 4Redução do O2;
Bombeamento de prótons para o espaço intermembranas à medida que os elétrons são transferidos para o Oxigênio.Redução parcial leva a produtos perigosos.

Cadeia Transportadora de Elétrons
H+ +

ATP SINTASE
Sinônimos: ATPase, ou F1F0ATPase
Enzima de estrutura muito complexa, formada por 16 subunidades polipeptídicas distribuídas em 2 frações funcionais: Fo e F1.

A fração F1 é semelhante a uma maçaneta cujo cabo seria a fração F0. Está ligada à membrana mitocondrial interna, sempre voltada para o lado da matriz. Tem atividade de síntese de ATP, mas para isso precisa estar ligada à F0.
A fração F0 atua como canal e prótons através da MMI. O o é a letra inicial de OLIGOMICINA, um potente inibidor desta enzima.

Hipótese Quimiosmótica

H+ +
H+
H+

HIPÓTESE QUIMIOSMÓTICA
Descrita em 1961 por Peter Mitchell;
Amplamente aceita.
Condições para ocorrer a fosforilação: um bombeamento de prótons pela cadeia respiratória e uma MMI impermeável a prótons e íntegra.

1- A cadeia respiratória, ao transportar os elétrons, bombeia prótons da matriz para o citossol;
2- A MMI, por ser impermeável a prótons, impede o retorno destes à matriz;
3- Cria-se um gradiente duplo (de pH e eletrostático) através da MMI, que gera uma situação de alta instabilidade e, como conseqüência, uma força que atrai os prótons de volta;
4- Esta força, chamada FORÇA PRÓTON-MOTRIZ, dirige o fluxo de prótons à matriz mitocondrial através dos canais de prótons da enzima ATPase;
5- A passagem dos prótons pela ATPase determina a síntese de ATP.

BALANÇO FINAL DA RESPIRAÇÃO CELULAR
Oxidação total de uma molécula de glicose.
Piruvato Acetil Coa Ciclo do Ácido Cítrico
2NADH 2 GTP
6 NADH
2 FADH2
GLICOSE PIRUVATO
2ATP2NADH
LANÇADEIRAS

LANÇADEIRAS:
a) Lançadeira glicerol-fosfato
Transporta os elétrons do NADH (com a ajuda do glicerol-fosfato)
e os tranfere ao FADH dentro da mitocôndria, formando FADH2.
b) Lançadeira de malato-aspartato
Transporta os elétrons do NADH (com a ajuda do malato) e os
tranfere a outro NAD+ dentro da mitocôndria, formando NADH.

Considerando-se NADH (2,5 ATP); FADH2 (1,5 ATP); GTP (1 ATP)
TOTAL= (8 x 2,5) + (4 x 1,5) + (2 x 1) + 2 = 30 ATPs
Piruvato Acetil Coa Ciclo do Ácido Cítrico
2NADH 2 GTP
6 NADH
2 FADH2
GLICOSE PIRUVATO
2ATP2NADH
LANÇADEIRAS
BALANÇO FINAL DA RESPIRAÇÃO CELULAR
Oxidação total de uma molécula de glicose.

INIBIDORES DO TRANSPORTE DE ELÉTRONS
a) Inibição da transferência de elétrons:
amital, rotenona (Complexo I)
cianeto, CO, azida (Complexo IV)
b) Inibição da ATP sintase:
oligomicina.
c) Desacoplamento da fosforilação da transferência de elétrons
valinomicina, termogenina*

TECIDO ADIPOSO MARROM (Gordura marrom)
Presente no dorso do pescoço de recém-nascidos (inclusive humanos) e nos mamíferos hibernantes.
A oxidação de combustíveis não funciona para produzir ATP, mas sim para gerar calor.
Proteína desacopladora (termogenina)
Alta [ ] mitocôndrias alta [ ] citocromos alta [ ] heme marrom.