DOENÇAS AUTOIMUNES DO SISTEMA...
-
Upload
truongliem -
Category
Documents
-
view
226 -
download
4
Transcript of DOENÇAS AUTOIMUNES DO SISTEMA...

UNIVERSIDADE DE LISBOA
FACULDADE DE FARMÁCIA
DOENÇAS AUTOIMUNES DO SISTEMA NERVOSO
MESTRADO EM ANÁLISES CLÍNICAS
Catarina Esteves Vasques de Carvalho Marinho Crespo Marques
LISBOA, 2011

Catarina Marinho Marques – Mestrado em Análises Clínicas 2
ÍNDICE GERAL
ÍNDICE DE TABELAS ................................................................................................... 5
ÍNDICE DE FIGURAS .................................................................................................... 5
ÍNDICE DE ABREVIATURAS ...................................................................................... 7
RESUMO ....................................................................................................................... 10
ABSTRACT ................................................................................................................... 10
DOENÇAS AUTOIMUNES .......................................................................................... 11
DOENÇAS AUTOIMUNES DO SISTEMA NERVOSO ............................................. 14
MIASTENIA GRAVIS .................................................................................................. 18
Epidemiologia ............................................................................................................. 18
Patogénese .................................................................................................................. 18
Manifestações Clínicas ............................................................................................... 19
Diagnóstico ................................................................................................................. 20
Tratamento .................................................................................................................. 24
Prognóstico ................................................................................................................. 25
SÍNDROME DE LAMBERT-EATON .......................................................................... 26
Epidemiologia ............................................................................................................. 26
Patogénese .................................................................................................................. 26
Manifestações Clínicas ............................................................................................... 27
Diagnóstico ................................................................................................................. 28
Tratamento .................................................................................................................. 30
Prognóstico ................................................................................................................. 30
SÍNDROME DE GUILLAIN-BARRÉ .......................................................................... 32

Catarina Marinho Marques – Mestrado em Análises Clínicas 3
Epidemiologia ............................................................................................................. 32
Patogénese .................................................................................................................. 32
Manifestações Clínicas ............................................................................................... 33
Diagnóstico ................................................................................................................. 33
Tratamento .................................................................................................................. 36
Prognóstico ................................................................................................................. 36
ESCLEROSE MÚLTIPLA ............................................................................................ 37
Epidemiologia ............................................................................................................. 37
Patogénese .................................................................................................................. 37
Manifestações Clínicas ............................................................................................... 38
Diagnóstico ................................................................................................................. 39
Tratamento .................................................................................................................. 42
Prognóstico ................................................................................................................. 43
ENCEFALITE LÍMBICA .............................................................................................. 45
Epidemiologia ............................................................................................................. 45
Patogénese .................................................................................................................. 45
Manifestações Clínicas ............................................................................................... 45
Diagnóstico ................................................................................................................. 46
Tratamento .................................................................................................................. 47
Prognóstico ................................................................................................................. 48
NEUROMIELITE ÓPTICA ........................................................................................... 49
Epidemiologia ............................................................................................................. 49
Patogénese .................................................................................................................. 49

Catarina Marinho Marques – Mestrado em Análises Clínicas 4
Manifestações Clínicas ............................................................................................... 50
Diagnóstico ................................................................................................................. 50
Tratamento .................................................................................................................. 51
Prognóstico ................................................................................................................. 52
SÍNDROME DE STIFFMAN ........................................................................................ 53
Epidemiologia ............................................................................................................. 53
Patogénese .................................................................................................................. 53
Manifestações Clínicas ............................................................................................... 53
Diagnóstico ................................................................................................................. 53
Tratamento .................................................................................................................. 55
Prognóstico ................................................................................................................. 55
SÍNDROMES PARANEOPLÁSICOS .......................................................................... 56
Epidemiologia ............................................................................................................. 56
Patogénese .................................................................................................................. 57
Manifestações Clínicas ............................................................................................... 57
Diagnóstico ................................................................................................................. 57
Tratamento .................................................................................................................. 59
Prognóstico ................................................................................................................. 59
CONCLUSÃO ................................................................................................................ 61
BIBLIOGRAFIA ............................................................................................................ 63

Catarina Marinho Marques – Mestrado em Análises Clínicas 5
ÍNDICE DE TABELAS
Tabela 1 – Métodos de detecção de AAc ...................................................................... 12
Tabela 2 – Doença autoimune e respectivo SN afectado ............................................... 17
Tabela 3 – Prevalência dos sintomas iniciais da MG [1] ............................................... 19
Tabela 4 - Classificação clínica da MG segundo Osserman [1] ..................................... 19
Tabela 5 – Ocorrência de MG com e sem timoma associado [6] ................................... 21
Tabela 6 - Testes de diagnóstico na MG [1] ................................................................... 23
Tabela 7 - Critérios de diagnóstico da MG segundo Gorshtein and Levy [1] ................ 24
Tabela 8 – Autoanticorpos detectados no LEMS [1] ..................................................... 29
Tabela 9 – Patogénese, Distribuição e Anticorpos associados aos subtipos de GBS ..... 34
Tabela 10 – Sintomas iniciais e crónicos da MS. Adaptado de Shoenfeld et al [1] ....... 39
Tabela 11 – Heterogeneidade da patologia da MS. Adaptado de Shoenfeld et al [1] .... 40
Tabela 12 – Síndromes Paraneoplásicos [1] ................................................................... 56
Tabela 13 – Anticorpos onconeuronais e PNS associado [1] [18] ................................. 58
Tabela 14 – Principais aspectos de cada patologia abordada. ........................................ 62
ÍNDICE DE FIGURAS
Figura 1 - Causas de doenças autoimunes [3] ................................................................ 12
Figura 2 – O Sistema Nervoso [8] .................................................................................. 14
Figura 3 – Nervo danificado pela MS [42] ..................................................................... 15
Figura 4 – Transmissão neuromuscular [13] .................................................................. 16
Figura 5 – Ac anti-músculo estriado Método: IFI Substrato: Músculo esquelético de
macaco [6] ...................................................................................................................... 21

Catarina Marinho Marques – Mestrado em Análises Clínicas 6
Figura 6 – Transmissão neuromuscular [41] .................................................................. 27
Figura 7 – Ac anti-AGNA Método: IFI Substrato: Cerebelo [12] ................................. 28
Figura 8 – Mecanismo de mimetismo molecular envolvido na resposta autoimune após
infecção por C. jejuni [49] .............................................................................................. 33
Figura 9 – Semelhança entre o gangliosídeo humano GM1 e o epitopo GM1-like no
C.jejuni [49] .................................................................................................................... 34
Figura 10 - Immunoblot com Ag relevantes para o diagnóstico de patologias do SN [43]
........................................................................................................................................ 35
Figura 11 – Critérios clínicos para o diagnóstico do GBS [1]........................................ 36
Figura 12 – Padrões de evolução da MS [51] ................................................................. 39
Figura 13 – Presença de bandas oligoclonais em LCR de doentes com MS [50] .......... 40
Figura 14 – Ac anti-MBP Método: IFI Substrato: Cerebelo e Secção de um nervo [12]
........................................................................................................................................ 41
Figura 15 – Critérios de diagnóstico da MS segundo McDonald [1] ............................. 42
Figura 16 – Receptor do Glutamato (tipo NMDA) [43] ................................................. 46
Figura 17 – Ac anti-NMDAr. Método: IFI Substratos: Hipocampo e cerebelo de rato
[43] ................................................................................................................................. 47
Figura 18 – Monitorização dos Ac anti-NMDAr [43] .................................................... 48
Figura 19 - Corte transversal do encéfalo humano [43] ................................................. 49
Figura 20 – Ac anti-Aquaporina 4. Método: IFI Substrato: cerebelo de macaco [6] ..... 51
Figura 21 – Ac anti-anfifisina. Método: IFI Substrato: cerebelo [12] ............................ 54
Figura 22 – Ac anti-GAD. Método: IFI Substrato: cerebelo e pâncreas [12] ................ 55

Catarina Marinho Marques – Mestrado em Análises Clínicas 7
ÍNDICE DE ABREVIATURAS
AAc – Autoanticorpo/s
AAg – Autoantigénio/s
Ac – Anticorpo/s
ACh - Acetilcolina
AChR – Receptor da Acetilcolina
Ag – Antigénio/s
AGNA – Anticorpo anti-nuclear glial
AIDP - Polineuropatia Desmielinizante Inflamatória Aguda
AMAN - Neuropatia Axonal Motora Aguda
AMPA - α-amino-3-hydroxy-5-methyl-4-isoxazolepropionic acid
AMSAN - Neuropatia Axonal Sensorial Motora Aguda
CE - Corticoesteróides
DAI – Doenças Autoimunes
EBV – vírus Epstein-Barr
EIA – Enzyme Immuno Assay
ELISA – Enzyme Linked Immuno Sorbent Assay
EUA – Estados Unidos da América
GABA - Ácido gama-aminobutírico
GAD – Descarboxilase do Ácido Glutâmico
GBS – síndrome de Guillain Barré
GM - Gangliosídeo

Catarina Marinho Marques – Mestrado em Análises Clínicas 8
HLA – Human Leucocyte Antigen
IB - Immunoblot
IF - Imunofluorescência
IFD – Imunofluorescência directa
IFI - Imunofluorescência indirecta
IgG/IgM/IgA – Imunoglobulina de classe G/M/A
IS - Imunossupressores
IVIg - Imunoglobulinas intravenosas
LCR – Líquido cefalorraquidiano
LE – Encefalite límbica
LEMS – Síndrome de Lambert-Eaton
MBP – Proteína Básica da Mielina
MFS – Síndrome de Miller-Fisher
MG – Miastenia Gravis
MOG – Glucoproteína Mielínica Oligodendrocitária
MS – Esclerose Múltipla
MuSK – Muscle-specific tyrosine kinase
NMDA - N-Methyl-D-aspartate
NMDAr – receptor do N-Methyl-D-aspartate
NMO – Neuromielite óptica
NPC – Neural Progenior Cells
PE – Plasmaferese

Catarina Marinho Marques – Mestrado em Análises Clínicas 9
PET – Tomografia de emissão de Positrões
PNS – Síndrome paraneoplásico
PP-MS – Esclerose Múltipla Primária Progressiva
RIA – Radio Imuno Assay
RM – Ressonância Magnética
ROI - Intermediários Reactivos do Oxigénio
RR-MS – Esclerose Múltipla Recaída Remissão
SCLC – Cancro de pequenas células do pulmão
SI – Sistema Imunitário
SN – Sistema Nervoso
SNC - Sistema Nervoso Central
SNP - Sistema Nervoso Periférico
SP-MS - Esclerose Múltipla Secundária Progressiva
SS – Sindrome de Stiffman
TAC – Tomografia Axial Computorizada
UV – Ultra-violeta
VGCC – Canal de cálcio dependente da voltagem
VGKC – Canal de potássio dependente da voltagem

Catarina Marinho Marques – Mestrado em Análises Clínicas 10
RESUMO
As doenças autoimunes surgem devido a falhas nos mecanismos de tolerância
imunológica do indivíduo, conduzindo à produção de autoanticorpos que atacam o
próprio. As doenças autoimunes podem ser classificadas em sistémicas e específicas de
orgão.
Na década de 60 foram associadas causas autoimunes para certas patologias do sistema
nervoso. As patologias autoimunes do sistema nervoso são um grupo de doenças
específicas de orgão, que podem afectar o sistema nervoso central, o sistema nervoso
periférico e as junções neuromusculares.
Dentro deste grupo de doenças autoimunes, existe um subgrupo no qual a neoplasia
aparece associada a doença autoimune, passando a ser chamada síndrome
paraneoplásico.
O objectivo deste trabalho foi falar das doenças do sistema nervoso mais prevalentes no
âmbito laboratorial e compará-las quanto à sua epidemiologia, patogénese,
manifestações clínicas, diagnóstico, tratamento e prognóstico.
Palavras-chave: doenças autoimunes, sistema nervoso, autoanticorpos, síndrome
paraneoplásico, neoplasia, imunofluorescência, plasmaferese, corticosteróides,
imunoglobulinas intravenosas
ABSTRACT
Autoimmune diseases appear due to a failure in the mechanisms of self immune
tolerance, which can lead to the production of autoantibodies that attack the individual.
Autoimmune diseases can be classified into systemic and organ specific. In the 60s,
causes were linked to certain autoimmune diseases of the nervous system.
The autoimmune diseases of the nervous system are a group of organ specific diseases
that can affect the central nervous system, peripheral nervous system and the
neuromuscular junctions.

Catarina Marinho Marques – Mestrado em Análises Clínicas 11
Within this group of autoimmune diseases, there is a subgroup in which cancer appears
linked to autoimmune disease, being called paraneoplastic syndrome.
The goal was to address the more prevailing nervous system diseases in the laboratorial
context and compare them in terms of their epidemiology, pathogenesis, clinical
manifestations, diagnosis, treatment and prognosis.
Keywords: autoimmune diseases, nervous system, autoantibodies, paraneoplastic
syndrome, neoplasia, immunofluorescence, plasmapheresis, corticosteroids, intravenous
immunoglobulins
DOENÇAS AUTOIMUNES
A autoimunidade consiste na resposta contra antigénios do próprio onde ocorrem dois
tipos de resposta – humoral, com formação de autoanticorpos (AAc) e celular, com
formação de células sensibilizadas.[29] A autoimunidade pode ser um fenómeno
fisiológico, como é o caso dos fenómenos de restrição MHC (Major Histocompatibility
Complex), nos humanos HLA (Human Leukocyte Antigen) e selecção tímica, ou um
fenómeno patológico no qual pode haver perda de tolerância, desenvolvimento de uma
resposta contra o próprio, e o desencadear de uma doença autoimune (DAI).[30] A sua
prevalência é de cerca de 3% em toda a população dos EUA [31], e pensa-se que a sua
etiologia seja multifactorial. A figura 1 ilustra as causas de DAI, que dependem
essencialmente de factores:
Genéticos: os alelos HLA estão associados a algumas DAI, como por exemplo,
Miastenia Gravis, Síndrome de Lambert-Eaton, Esclerose Múltipla.
Hormonais: as mulheres são, regra geral, mais afectadas.
Ambientais: radiações UV, o uso de certos medicamentos.

Catarina Marinho Marques – Mestrado em Análises Clínicas 12
Figura 1 - Causas de doenças autoimunes [3]
Actualmente, as DAI classificam-se em específicas de orgão, quando a lesão se dá num
orgão, e sistémicas quando há afecção de vários orgãos. [30]
As DAI são diagnosticadas através das manifestações clínicas, características
bioquímicas, histológicas, genéticas e serológicas na qual se inclui a pesquisa de AAc.
Na tabela seguinte enumeram-se os métodos mais utilizados na detecção de AAc,
respectivo elemento marcador, tipo de ensaio qualitativo ou quantitativo.
Técnica Elemento marcador Tipo de ensaio
Imunofluorescência (IF) Fluorocromo Quantitativo
Ensaio Imuno Enzimático (EIA) Enzima Quantitativo
Radio-Imuno-Ensaio (RIA) Isótopo radioactivo Quantitativo
Western Blot Enzima Qualitativo
Tabela 1 – Métodos de detecção de AAc
O método de IF é o método de referência usado, onde marcadores fluorescentes são
conjugados com Ac, e usados para identificar antigénios na superfície celular, no caso
da IFD, ou para detectar AAc ou Ac contra agentes infecciosos, no caso da IFI. Dada a
sua sensibilidade, é um método de screening, devendo depois ser confirmado por um
método mais sensível, como um ELISA, ou um método mais específico como um
Western blot (também chamado Immunoblot de proteínas ou simplesmente

Catarina Marinho Marques – Mestrado em Análises Clínicas 13
Immunoblot). São ambos ensaios imunoenzimáticos, mas o ELISA é um método
quantitativo que utiliza uma enzima em vez do fluorocromo, e o Immunoblot permite a
detecção qualitativa de Ac utilizando Ag altamente purificados.
O método de RIA continua a ser uma técnica muito útil dada a elevada sensibilidade e
especificidade, mas requer muitos cuidados devido ao uso de elementos radioactivos, e
é também uma técnica bastante dispendiosa, sendo sobretudo usada na detecção de Ag e
Ac infecciosos, ou quando a técnica de ELISA não serve como alternativa.[33]
O método de IF utiliza diferentes substratos que podem ser células ou tecidos de
animais em cultura. No caso dos Ac anti-neuronais, dado que os Ag se localizam
preferencialmente nos tecidos nervosos, os tecidos usados para a detecção dos AAc,
serão sobretudo cerebelo, nervo periférico, espinal medula, músculo esquelético, entre
outros.
O tratamento das DAI varia entre uma terapêutica mais leve e uma mais drástica,
consoante a gravidade e a patologia. Regra geral passa pelo restabelecimento da função
do orgão lesionado, pela imunossupressão e pelo tratamento dos sintomas
secundários.[3] O mais frequente é o uso de drogas antimitóticas e anti-inflamatórios,
sobretudo corticoesteróides. A administração de imunoglobulinas intravenosas (IVIg) e
a plasmaferese (PE) são tratamentos cada vez mais utilizados, dado o seu sucesso
terapêutico em inúmeras patologias.
As imunoglobulinas intravenosas são proteínas presentes no plasma humano,
responsáveis pela imunidade humoral, e são obtidas a partir do fraccionamento
industrial do plasma, com métodos de inactivação e eliminação de vírus. São sobretudo
de classe IgG, contendo pequenas quantidades de IgM e de IgA. Foram originalmente
desenvolvidas para reposição de anticorpos em imunodeficiências, mas graças aos seus
efeitos antinflamatórios e imunomoduladores, tornaram-se numa alternativa terapêutica
para doenças sem tratamento estabelecido.
A plasmaferese é um processo de remoção de elementos do plasma sanguíneo que
possam ser responsáveis por algumas doenças. A indicação mais comum é para
remoção de anticorpos e complexos autoimunes.
Alternativamente também se faz controlo metabólico, transplante de tecidos ou orgãos e
terapêuticas biológicas com citocinas.[29]

Catarina Marinho Marques – Mestrado em Análises Clínicas 14
DOENÇAS AUTOIMUNES DO SISTEMA NERVOSO
A associação autoimunidade – doença foi feita na década de 50, sendo na década de 60
que foram associadas causas autoimunes para certas patologias do sistema nervoso.[1]
As DAI do sistema nervoso são doenças específicas de orgão que podem ocorrer
isoladamente como uma patologia autoimune, ou estarem associadas a situações de
neoplasia, conhecidas como síndromes paraneoplásicos (PNS).
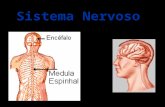
O SN é o conjunto de nervos, gânglios e centros nervosos que asseguram o comando e a
coordenação das funções vitais. É dividido em SNC e SNP.
O SNC contém o encéfalo e a espinal medula. O SNP subdivide-se em duas partes, o
sistema nervoso somático e o sistema nervoso autónomo e este por sua vez divide-se em
sistema nervoso simpático e sistema nervoso parassimpático.
A unidade básica do sistema nervoso é o neurónio. O neurónio conduz o impulso
nervoso e é composto por dendrites, corpo celular e axónio. As dendrites trazem o
impulso nervoso para o corpo celular, enquanto o axónio leva o impulso para fora do
corpo celular.
Figura 2 – O Sistema Nervoso [8]
Na presença de uma DAI, há uma resposta imune que leva à produção de AAc, que
podem ser específicos de orgão ou não específicos de orgão. No âmbito das DAI do SN
são focados os Ac específicos de orgão, já que são mais relevantes para o diagnóstico
das patologias referidas.
A resposta imune pode ser dirigida contra componentes tecidulares específicos, por
exemplo contra a mielina, no caso da Esclerose Múltipla (MS). A mielina é uma
substância lipídica que está presente na chamada bainha de mielina. A bainha de mielina

Catarina Marinho Marques – Mestrado em Análises Clínicas 15
é formada pelos oligodendrócitos no SNC e pelas células de Schwann no SNP, e rodeia
algumas fibras nervosas, fazendo com que tenham uma condução de impulsos nervosos
mais rápida.[7] [8]
A figura 3 ilustra a falta de “isolamento eléctrico” devido à desmielinização, que está na
origem das queixas de fraqueza, paralisia ou cegueira temporárias.[3]
Figura 3 – Nervo danificado pela MS [42]
Noutros casos, a resposta imune pode dirigir-se contra as junções neuromusculares,
como é o caso da Miastenia Gravis (MG). As junções neuromusculares são zonas de
ligação entre a parte terminal de um axónio motor com uma placa motora, que é a
região da membrana plasmática de uma fibra muscular onde se dá o encontro entre o
nervo e o músculo, permitindo desencadear a contracção muscular. Na junção
neuromuscular o neurotransmissor predominante é a acetilcolina. Portanto, na MG a
afecção das junções neuromusculares com a produção de Ac contra os receptores da
acetilcolina, dá origem a um defeito na transmissão do impulso nervoso e
consequentemente, à fraqueza muscular. Na figura 4 pode ver-se a transmissão
neuromuscular, que envolve o neurotransmissor acetilcolina, o seu receptor e os canais
de cálcio e potássio dependentes da voltagem (VGCC e VGKC), que estarão implicados
nalgumas patologias abordadas.

Catarina Marinho Marques – Mestrado em Análises Clínicas 16
Figura 4 – Transmissão neuromuscular [13]
O SNC tem como objectivo o processamento e integração da informação. É o local onde
ocorre a tomada de decisões e o envio de ordens (frio, luz, som, odor, quente, sabor e
vibrações). O SNP carrega informações dos orgãos sensoriais para o SNC e deste para
os orgãos efectores (músculos e glândulas).
O SNP somático é responsável pelo controlo da musculatura esquelética e pela
transmissão de informação dos orgãos sensoriais. Engloba vários nervos que se
ramificam a partir do SNC: sensoriais ou aferentes (recolhem da periferia as excitações
que conduzem ao SNC, traduzindo-se depois em sensação táctil e térmica) e motores ou
eferentes (conduzem o estimulo do SNC que vai fazer contrair os músculos, segregar as
glândulas, orientando deste modo diversos comportamentos como o andar, o escrever e
o chorar). Os nervos de conexão permitem estabelecer a relação entre nervos sensoriais
e nervos motores. O SNP autónomo controla as diversas estruturas viscerais
responsáveis pelos processos vitais básicos, como o coração, os vasos sanguíneos, o
sistema digestivo, os orgãos sexuais, entre outros, e funciona de um modo automático.
O SN simpático é formado por dois grupos de neurónios, os pré-ganglionares, situados
na medula espinal, e os pós-ganglionares situados junto à coluna vertebral. O SN
simpático estimula acções que permitem ao organismo responder a situações de stress,
como a aceleração dos batimentos cardíacos, o aumento da pressão arterial, o aumento
da adrenalina, a concentração de açúcar no sangue e a activação do metabolismo geral
do corpo. O SN parassimpático é a parte do SN autónomo cujos neurónios se localizam
no tronco cerebral. É o responsável por estimular acções que permitem ao organismo
responder a situações de calma, como desaceleração dos batimentos cardíacos,

Catarina Marinho Marques – Mestrado em Análises Clínicas 17
diminuição da pressão arterial, diminuição da adrenalina e diminuição do açúcar no
sangue.[8] Algumas DAI do SN estão limitadas ao SNC, outras ao SNP, e outras
afectam ambos, como é o caso dos PNS.
Os PNS estão presentes exclusivamente ou com elevada frequência em doentes com
cancro. Por definição, os PNS não são explicados por infiltração local, regional ou
metastática, disfunção metabólica ou infecção, efeitos secundários da terapêutica
oncológica ou coagulopatia relacionada com o cancro. Pensa-se sim, que são DAI
caracterizadas por terem uma resposta imune contra um Ag que se expressa, tanto nas
células tumorais como nos neurónios.
Como DAI que são, levam à produção de AAc, que adoptam o nome de AAc
onconeuronais. Quando presentes exclusivamente nos doentes com cancro chamam-se
PNS clássicos. São PNS a Miastenia Gravis, o síndrome de Lambert-Eaton, o síndrome
de Stiffman e a Encefalite Límbica. Destes, apenas o síndrome de Lambert-Eaton e a
Encefalite Límbica são PNS clássicos. A Esclerose Múltipla, o síndrome de Guillain
Barré e a Neuromielite Óptica não têm neoplasia associada.[1]
Existem muitas DAI do SN, mas optou-se por abordar as mais prevalentes no âmbito do
diagnóstico laboratorial. O objectivo deste trabalho é comparar os diferentes aspectos de
cada patologia autoimune do SN, focando em cada uma: Epidemiologia, Patogénese,
Manifestações Clínicas, Diagnóstico, Tratamento e Prognóstico.
Na tabela seguinte são enumeradas as DAI abordadas neste trabalho:
Doença Autoimune Sistema nervoso afectado Síndrome
Paraneoplásico
Miastenia gravis SNP Sim
Síndrome de Lambert-Eaton SNP Sim
Síndrome de Guillain Barré SNP Não
Esclerose múltipla SNC Não
Encefalite Límbica SNC Sim
Neuromielite óptica SNC Não
Síndrome de Stiffman SNC Sim
Tabela 2 – Doença autoimune e respectivo SN afectado

Catarina Marinho Marques – Mestrado em Análises Clínicas 18
MIASTENIA GRAVIS
A MG, que em grego significa fraqueza muscular severa, é a DAI do foro neurológico
mais bem conhecida. É uma doença crónica que afecta a transmissão neuromuscular. A
existência de anticorpos contra os receptores da acetilcolina provoca a diminuição
destes mesmos receptores e consequentemente a fadiga e debilidade dos músculos
esqueléticos.[1] [4] [5] [34]
Epidemiologia
Tal como a maior parte das DAI, é mais prevalente na mulher do que no homem
ocorrendo numa relação de 2:1, sendo que o pico de incidência da MG nas mulheres
ocorre na 3ª década de vida e nos homens na 3ª e 6ª décadas de vida. Curiosamente, a
incidência de MG, tem vindo a aumentar nos homens idosos. Por cada 100.000
habitantes julga-se que afecta cerca de 20 a 40 pessoas. Entre 10% a 13% dos doentes
com MG apresentam um timoma associado, dando-se o início da doença nestes doentes,
entre a 4ª e 5ª década de vida. A MG ocorre indiferentemente em todas as raças.[1] [6]
Patogénese
O receptor da acetilcolina (AChR) é uma proteína transmembranar de tipo canal iónico.
A acetilcolina libertada no terminal nervoso liga-se a duas subunidades α no AChR e
abre o canal, permitindo a passagem de catiões, o que cria um potencial de acção. É a
perda de AChR que ocorre na MG que conduz à fraqueza muscular.[4]
Há três factores envolvidos na patogenecidade:
1. Os Ac fixam o complemento e causam lise da membrana pós-sináptica com
perda de AChR e libertação de complexos AChr-Ac-complemento na fenda
sináptica;
2. Os Ac podem modular AChR;
3. Uma pequena quantidade de Ac ligam-se directamente ao sítio de ligação,
provocando o bloqueio.
A resposta autoimune é desencadeada pelos linfócitos T helper CD4+ e mediada
primariamente por Ac contra os AChR, sobretudo de classe IgG.[4] A existência destes
AAc tem um grande impacto tanto na transmissão do impulso nervoso como na
fraqueza neuromuscular levando ao bloqueio dos receptores, aumento da sua

Catarina Marinho Marques – Mestrado em Análises Clínicas 19
degradação e destruição da fenda pós-sináptica mediada pelo complemento. Pensa-se
que o timo está envolvido na patogénese da MG já que costuma estar alterado na
maioria dos doentes com esta doença.
Manifestações Clínicas
A MG provoca fraqueza e dores musculares sobretudo após esforço físico. Os reflexos
sensoriais dos tendões e funções cerebelares não são afectados. Os sinais e sintomas
iniciais incluem: pálpebra descaída, diplopia, envolvimento dos músculos faciais e
bulbares, afectando a fala, as expressões faciais, a mastigação e a disfagia. Na tabela
seguinte é apresentada a prevalência dos sintomas iniciais da MG.
Tabela 3 – Prevalência dos sintomas iniciais da MG [1]
Pode ocorrer ainda fraqueza dos músculos respiratórios dificultando a respiração, termo
designado por crise miasténica. A crise miasténica, que pode colocar o doente em risco
de vida, ocorre usualmente no início da doença sendo frequentemente provocada por
uma infecção intercorrente. A tabela seguinte apresenta a escala com que Osserman
define a gravidade clínica da MG.[1]
I Sinais e sintomas oculares
II Miastenia generalizada
IIa Doença média
IIb Doença moderada
III Doença generalizada severa
IV Crise miasténica
Tabela 4 - Classificação clínica da MG segundo Osserman [1]
O curso clínico da MG é bastante variável: nalguns doentes a fraqueza fica confinada a
um único grupo muscular por muito tempo, regra geral os músculos da pálpebra ou

Catarina Marinho Marques – Mestrado em Análises Clínicas 20
extraoculares, enquanto em 85% pode progredir para fraqueza generalizada. Podem
ocorrer flutuações na severidade da doença durante os primeiros anos.
Os sintomas podem agravar-se pelo esforço físico, exposição ao calor, alterações
emocionais (stress e ansiedade), estados infecciosos e pelo uso de alguns medicamentos,
como por exemplo, alguns tranquilizantes e antibióticos.[1]
Diagnóstico
Em 80-90% dos doentes com MG o timo apresenta alterações histológicas, ocorrendo
hiperplasia tímica (sobretudo nos doentes mais novos), que se caracteriza por folículos
linfóides com centros germinativos activos. Em 10-13% dos doentes verifica-se a
existência de timomas. Por microscopia electrónica observa-se uma diminuição
significativa de receptores de acetilcolina na zona das junções neuromusculares, uma
redução da complexidade das fendas pós-sinápticas e depósitos de IgG e complemento.
Existem 3 tipos de AAc que podemos encontrar na MG:
1. Anticorpos contra os receptores da acetilcolina (Ac anti-AChR)
Estes AAc são detectados em cerca de 85% doentes com MG (MG
seropositiva): em 90% dos indivíduos com doença generalizada e em cerca de
50% com doença ocular. A presença dos anticorpos não se correlaciona com a
severidade da doença, mas tem carácter diagnóstico.[5] [6] Estes AAc são
muito específicos, não aparecendo em indivíduos saudáveis nem noutras
doenças do foro neurológico. São habitualmente detectados por
imunoprecipitação, por EIA ou por IFI. Surgem na MG, associados a timomas,
e em raros casos na doença de Hodgkin.[1] [5] [18]
2. Anticorpos contra a cinase específica do músculo (Ac anti-MuSK)
Os Ac anti-MuSK são específicos da MG seronegativa. A cinase específica do
músculo é uma proteína de membrana que na vida adulta está restrita à junção
neuromuscular.[4] A prevalência de Ac anti-MuSK na MG seronegativa
depende da população à qual nos referimos: 4% nos chineses, 22% nos
holandeses e 40-70% nos norte-americanos e europeus. Os Ac anti-MuSK são
detectados sobretudo em mulheres jovens com envolvimento facial e bulbar e a

Catarina Marinho Marques – Mestrado em Análises Clínicas 21
sua presença correlaciona-se com a gravidade da doença. A detecção de Ac
anti-MuSK é feita por EIA e por RIA.[6]
3. Anticorpos anti-músculo estriado
Estes Ac reagem contra elementos contrácteis do músculo estriado. O alvo dos
Ac anti- músculo estriado são as proteínas sarcoméricas do músculo estriado –
titina, miosina e actina. A titina é uma proteína gigante que aumenta o
comprimento do sarcómero e que tem uma região mais imunogénica, chamada
MGT-30.[6] Os Ac anti-actina e anti-miosina não se correlacionam e não
causam MG.[14] Os Ac anti- músculo estriado são detectados em cerca de 80%
dos doentes com MG com timoma associado. A sua precisão é semelhante à
precisão da TAC, no prognóstico dos timomas. A associação de MG e timoma
deve-se provavelmente a anomalias no timo que levam à produção de Ac contra
as fibras do músculo estriado, que então se ligam aos músculos motores. Na
tabela 5 é evidenciada a ocorrência de MG associada ou não, a neoplasia. Pode
ser observado que na maioria das vezes esta patologia ocorre associada a cancro
e sobretudo em pessoas idosas.
MG associado a timoma 90%
MG sem timoma > 60 anos 55%
MG sem timoma < 40 anos 6%
MG sem timoma < 20 anos raro
Tabela 5 – Ocorrência de MG com e sem timoma associado [6]
A detecção de Ac anti-músculo estriado é feita por IFI.
Figura 5 – Ac anti-músculo estriado Método: IFI Substrato: Músculo esquelético de macaco [6]

Catarina Marinho Marques – Mestrado em Análises Clínicas 22
O diagnóstico da MG é feito pela combinação de factores clínicos, electrofisiológicos e
laboratoriais.[34] É importante que se faça um diagnóstico diferencial de MG: distingui-
la de MG induzida por drogas, a síndrome de Lambert-Eaton, o botulismo, lesões
intracranianas, oftalmoplegia externa progressiva, entre outros. As lesões orbitais e
intracranianas devem ser excluídas por imagiologia. Na tabela seguinte referenciam-se
vantagens e desvantagens dos testes actualmente usados no diagnóstico da MG, a sua
sensibilidade, especificidade e correlação clínica dos AAc detectados nos doentes de
MG. Nenhum teste é suficientemente preciso para ser usado isoladamente no
diagnóstico da doença. O teste com edrofónio é especialmente útil nos casos de MG
ocular mas não é específico de MG, e esta droga pode causar efeitos secundários
colinérgicos. Testes electrodiagnósticos (estimulação repetitiva do nervo e
electromiografia de fibra única) são sensíveis mas não específicos e dependem do
operador. A determinação de Ac é de utilidade variável dado que a sua sensibilidade é
baixa nos doentes com MG ocular. A nível histológico a detecção de uma massa no
mediastino anterior sugestiva de timoma pode suportar o diagnóstico de MG.[5]

Catarina Marinho Marques – Mestrado em Análises Clínicas 23
Teste Vantagens dos
testes serológicos Desvantagens Sensibilidade Especificidade
Edrofónio Bom para MG ocular No caso de
glaucoma agudo
e obstrução
urinária e
intestinal.
Efeitos
secundários
colinérgicos.
85% na MG
ocular
60% na MG
generalizada
É de curta duração para
a avaliação dos vários
grupos de músculos (é
preferível usar
neostigmina)
Falsos positivos na
esclerose lateral
amiotrófica, tumores
intracranianos, paralisia
supranuclear
Ac anti-
AChR
Não há correlação com
a actividade da doença
Mau para MG
ocular
40-60% na MG
ocular
80-90% na MG
generalizada
Específico para MG
Resultado negativo não
exclui MG
Ac anti-
músculo
estriado
Mais prevalente nos
doentes mais idosos
Associação com
timoma
Correlação com a
severidade da doença
Falta de
informação
quanto ao papel
patogénico
10-30% na MG
generalizada
60-85% na MG
com timoma
Não específico
Valor preditivo de
timoma
Ac anti-
MuSK
Sobretudo na mulher,
quando o início da
doença se dá na idade
jovem e
predominantemente na
fraqueza bulbar
Correlação com a
actividade da doença
Grande
variabilidade
geográfica na
prevalência
4-70% dos
doentes com MG
seronegativa
Muito específico para a
MG seronegativa
Estimulaçã
o repetitiva
do nervo
Pode ser combinado
com o teste do
edrofónio
Desagradável
para o doente
Depende do
operador
50-60% na MG
ocular
70-80% na MG
generalizada
Até 90% quando
são testados os
músculos
proximais
Não específico
Electromio
grafia de
fibra única
Muito sensível Demorado
Depende da
colaboração do
doente e da
habilidade do
operador
90-99% para MG
ocular e
generalizada
Não específico
Tabela 6 - Testes de diagnóstico na MG [1]

Catarina Marinho Marques – Mestrado em Análises Clínicas 24
A fraqueza clínica e a resposta a drogas anticolinérgicas devem ser medidas por um
instrumento objectivo, como um score quantitativo para a MG que meça a severidade da
doença. Já que os Ac anti-MuSK são específicos para a MG seronegativa, devem ser
testados somente em doentes seronegativos para Ac anti-AChR. Deve-se estabelecer um
critério clínico e serológico ou clínico, farmacológico e electrofisiológico para um
diagnóstico definitivo. Na tabela 7, Gorshtein e Levy [1] apresentam critérios de
diagnóstico a serem usados em pessoas com idade superior a 2 anos. Para um
diagnóstico provável bastará um critério clínico e farmacológico ou clínico e
electrofisiológico.
1. Critério clínico – fraqueza muscular e fadiga sem prejuízo das funções sensoriais, reflexos e
cerebelares
2. Critério farmacológico – melhoramento da fraqueza muscular após administração de uma
medicação anticolinérgica
3. Critério serológico – presença de anticorpos anti-receptores da acetilcolina e anti-MuSK
4. Critério electrofisiológico – evidência de um defeito na transmissão neuromuscular
Tabela 7 - Critérios de diagnóstico da MG segundo Gorshtein and Levy [1]
Em relação à susceptibilidade genética, existe, na MG, uma forte correlação entre os
doentes com Ac anti-AChR e os antigénios HLA B8 e DR3.[5]
Tratamento
As terapêuticas usadas hoje em dia para o tratamento da MG incluem moduladores da
transmissão neuromuscular, imunosupressores e imunomoduladores. As drogas
anticolinesterase melhoram a fraqueza miasténica pelo melhoramento provisório da
transmissão neuromuscular na maioria dos doentes com MG, mas raramente tratam por
completo a doença. A sobredosagem destas drogas pode causar aumento da fraqueza e
efeitos secundários muscarínicos. As drogas imunosupressoras incluem
corticoesteróides, azatioprina, micofenolato mofetil, ciclofosfamida, ciclosporina e
tacrolimus. O rituximab é um fármaco intravenoso que pertence à classe dos anticorpos
monoclonais, dirigido contra a proteína de superfície celular CD20, encontrada em
linfócitos B. É usado no tratamento da artrite reumatóide, no linfoma não Hodgkin a
células B e na MG com anticorpos anti-MuSK. Perante doentes de MG com timoma

Catarina Marinho Marques – Mestrado em Análises Clínicas 25
sujeitos a timectomia usa-se terapia imunomoduladora. Nos restantes doentes de MG
esta forma de tratamento não tem mais-valias.
Não há dados suficientes que suportem o sucesso terapêutico da IVIg, a não ser em
casos muito exacerbados de fraqueza muscular.
Na doença severa, não existe vantagem em usar IVIg e PE, mas dada a natureza de cada
tratamento, a primeira é escolhida. Alguns doentes de MG dependentes de CE podem
beneficiar de etanercepte. O etanercepte é um fármaco proteico que actua como inibidor
competitivo da ligação do TNF aos seus receptores da superfície celular, inibindo deste
modo a actividade biológica do TNF.[46]
Prognóstico
O prognóstico é menos favorável:
Em idosos e em doentes que não podem fazer uma timectomia: 40% não
sobreviverão aos primeiros 5 anos após o diagnóstico;
Se coexistirem os AAc AChR e AAc MuSK.
O facto de os Ac anti-músculo estriado serem mais prevalentes na população idosa e nos
casos de doença mais grave, faz com que sejam marcadores importantes no prognóstico
da MG.
Com tratamento, a maioria dos doentes tem uma qualidade de vida quase normal, sem
problemas significativos. Alguns casos de MG podem entrar em remissão temporária e
a fraqueza muscular pode desaparecer totalmente, de modo que a medicação pode ser
descontinuada. Remissões completas, estáveis e duradouras são o objectivo final da
timectomia.

Catarina Marinho Marques – Mestrado em Análises Clínicas 26
SÍNDROME DE LAMBERT-EATON
O síndrome de Lambert-Eaton (LEMS) é uma DAI do sistema nervoso periférico que se
caracteriza por fraqueza muscular e disfunções do sistema nervoso autónomo como
xerostomia, visão turva e obstipação.
Começou por ser descrito por Lambert et al que descreveram o doente como
apresentando uma doença Miastenia-like e um carcinoma dos brônquios associado. Por
esta razão ainda se refere a este síndrome como Síndrome Miasténico de Lambert-
Eaton. Estudos electrofisiológicos demonstraram que esta patologia é diferente da MG,
já que o envolvimento respiratório, músculos ocular e bulbar é reduzido.
Cerca de 60% dos doentes com LEMS apresentam carcinoma das pequenas células do
pulmão (SCLC), um cancro agressivo que quase sempre se relaciona com hábitos
tabágicos. O SCLC representa cerca de 20-25% de todos os cancros do pulmão e é um
tumor de origem neuroendócrina que expressa canais de cálcio dependentes da
voltagem (VGCC) à sua superfície.
Cerca de 90% dos doentes com o LEMS apresentam Ac anti-VGCC. Estes AAc, que
são produzidos como resposta a epitopos nas células tumorais, podem reagir com os
VGCC presentes nos terminais nervosos dando origem a disfunções neurológicas.[1]
[13]
Epidemiologia
Na generalidade da população a incidência é de cerca de 1 por cada 100.000 habitantes;
no entanto, a prevalência de LEMS em todos os doentes com SCLC é cerca de 3%.
A idade de início da doença varia entre os 17 e os 79 anos sendo menor em doentes com
neoplasia associada.
Patogénese
Existem duas formas da doença:
LEMS associado a Cancro
Cerca de 60% dos doentes com LEMS têm cancro associado, na maioria das vezes
SCLC, normalmente evidente 2 anos após o início da doença. A quase totalidade destes
doentes tem hábitos tabágicos. Os homens são cerca de duas vezes mais afectados do

Catarina Marinho Marques – Mestrado em Análises Clínicas 27
que as mulheres, o que pode estar relacionado com o facto de existirem mais homens
fumadores do que mulheres. A maioria dos doentes deste grupo apresenta problemas
neurológicos, meses a anos antes da detecção do tumor e curiosamente o tempo de
sobrevivência é superior ao do grupo LEMS sem Cancro associado (LEMS idiopática).
LEMS sem carcinoma associado (Idiopática)
Os restantes 40% nunca desenvolvem tumor. O início da doença é mais precoce e a
LEMS idiopática predomina nas mulheres. Há uma maior incidência de outras DAI
neste grupo: muitos doentes apresentam DAI específicas de orgão como tiroidite,
doença celíaca, miastenia ou vitiligo.
A figura 6 ilustra a transmissão neuromuscular e seus intervenientes.
Figura 6 – Transmissão neuromuscular [41]
Manifestações Clínicas
Na LEMS ocorre fraqueza dos músculos proximais e disfunções autonómicas como
hipersudorese, xerostomia, hipotensão postural e impotência nos indivíduos do sexo
masculino. Os reflexos nos tendões estão diminuídos ou mesmo ausentes; muitos

Catarina Marinho Marques – Mestrado em Análises Clínicas 28
doentes afirmam ter mais força quando principiam um exercício mas quando param,
perdem a força.[1] [13]
Diagnóstico
O diagnóstico é feito por métodos electrofisiológicos e por métodos laboratoriais.
As características clínicas e electrofisiológicas são semelhantes na LEMS seropositiva e
seronegativa.[6] [44] É recomendado fazer uma TAC e uma RM ao tórax. A detecção
de Ac é útil nos casos em que a disfunção cerebelar mascara os sintomas da LEMS.
O diagnóstico laboratorial passa pela detecção de Ac anti-VGCC, Ac anti-nuclear glial
(AGNA) e Ac anti-SOX1. Os Ac anti-AGNA são detectados por IFI e a sua utilidade no
diagnóstico, deve-se ao facto de aparecem em cerca de 11% dos doentes com SCLC e
cerca de 43% dos doentes com LEMS associado a cancro. A detecção de Ac anti-
AGNA faz-se no cerebelo de rato na camada das células de Purkinje, mais propriamente
no núcleo de células da glia.
Figura 7 – Ac anti-AGNA Método: IFI Substrato: Cerebelo [12]
Na LEMS estão também descritos Ac contra subtipos dos VGCC.
Na LEMS associada a cancro, pode ocorrer reacção cruzada entre os Ac anti-VGCC da
superfície das células do SCLC e os canais de cálcio dependentes da voltagem presentes
no sistema nervoso.[1] [13]
Os VGCC são uma família multimérica de proteínas que se dividem em subtipos
funcionais de acordo com as suas propriedades electrofisiológicas, farmacológicas e

Catarina Marinho Marques – Mestrado em Análises Clínicas 29
bioquímicas. São formados como um complexo de diferentes subunidades: α1, α2δ, β1-4
e γ. As subunidades α1 dos VGCC são transmembranares e constituem o sensor de
voltagem e o poro selectivo para o ião cálcio. Apresentam uma vasta distribuição,
consoante os subtipos de subunidades consideradas. No âmbito deste trabalho foco
apenas alguns tipos desta subunidade α1:
α1A
(tipo P/Q) que controlam a libertação de neurotransmissores nas junções
neuromusculares periféricas. Os VGCC tipo P/Q encontram-se no cerebelo e na
superfície das células do SCLC. Aparecem em 85-90% dos doentes;
α1B (tipo N): encontram-se nos sistemas nervoso central e periférico. Detectados
em 40% dos doentes;
α1C (tipo L) encontram-se no coração, fibroblastos, pulmão, músculo liso;
α1D (tipo L) encontram-se no cérebro e pâncreas. Os VGCC do tipo L, surgem em
25% dos doentes.[1] [27]
Os canais de cálcio dependentes da voltagem do tipo P/Q e N, são os antigénios contra
quais são dirigidos os Ac.[18]
Regra geral, os Ac anti-VGCC dos tipos N e L só se encontram em conjunto com o tipo
P/Q, o que significa que 10-15% dos doentes são seronegativos para qualquer tipo de
Ac contra os VGCC. A detecção dos Ac anti-VGCC faz-se por imunoprecipitação. O
título de anticorpo anti-VGCC tipo P/Q não se correlaciona com a gravidade da doença.
Ac detectado LEMS todos os
tipos
LEMS associado a
cancro
LEMS idiopática
Todos tipos VGCC 85-90 90-100 76-91
Tipo P/Q 85-90 90-100 76-91
Tipo N 40-50 40 22
Tipo L 25 0 25
Ac anti-VGCC - Positivo Negativo
Tabela 8 – Autoanticorpos detectados no LEMS [1]
A microscopia electrónica evidencia a desorganização e redução dos VGCC. Os VGCC
encontram-se no nervo terminal motor e controlam a libertação de ACh. A existência de

Catarina Marinho Marques – Mestrado em Análises Clínicas 30
Ac anti-VGCC prejudica a função dos terminais nervosos pré-sinápticos, existindo
falhas na formação de potenciais de acção.[1] [28]
O SOX1 é um antigénio tumoral altamente imunogénico presente nas células do SCLC.
Os Ac anti-SOX1 são importantes na medida em que ajudam ao diagnóstico diferencial
entre LEMS associada a cancro e LEMS idiopática. Estão presentes em 64% dos
doentes com LEMS associada a cancro e ausentes na LEMS idiopática. [55]
Estudos HLA mostram uma sobre expressão de HLA B8, um haplotipo que se julga
estar associado a outras DAI como a MG. A associação de HLA B8 e a predominância
nas mulheres levam a crer que a LEMS idiopática tenha causa autoimune.[1] [6]
Tratamento
A administração de amifampridina é eficaz e actua pelo bloqueio dos canais de potássio
dependentes da voltagem, prolongando assim a despolarização da membrana celular
pré-sináptica. O prolongamento do potencial de acção melhora o transporte de cálcio
para o interior das terminações nervosas. O consequente aumento das concentrações de
cálcio intracelular facilita a exocitose de vesículas que contêm acetilcolina, o que por
sua vez melhora a transmissão neuromuscular.
A acção da amifampridina melhora a força muscular e a amplitude do potencial de
acção muscular composto em repouso.[47]
As terapias que provocam imunossupressão, como a azatioprina e a prednisolona, são
usadas como adjuvantes. Nos casos de doença severa, exacerbada ou intolerância aos
esteróides, recorre-se à PE ou IVIg, com bons resultados.[1] [6]
Na LEMS associada a cancro a quimioterapia é a primeira escolha, podendo ainda ser
feita radioterapia. Após o tratamento, regista-se um aumento de força muscular nestes
doentes.
Prognóstico
Doentes com SCLC têm um mau prognóstico (taxas de sobrevivência entre 5-10% após
5 anos), mas doentes que têm SCLC associada a LEMS com Ac anti-VGCC positivos
apresentam um aumento na taxa de sobrevivência média comparativamente a doentes
Ac anti-VGCC negativos.

Catarina Marinho Marques – Mestrado em Análises Clínicas 31
Nos doentes com LEMS associada a cancro, o tumor torna-se detectável nos 2 primeiros
anos após o diagnóstico de LEMS.
Em doentes com LEMS que apresentam sinais neurológicos há mais de 5 anos, há um
baixo risco de desenvolverem um tumor. Na LEMS idiopática, a terapia
imunossupressora é eficaz, indicando um bom prognóstico.[1] [6]

Catarina Marinho Marques – Mestrado em Análises Clínicas 32
SÍNDROME DE GUILLAIN-BARRÉ
O síndrome de Guillain-Barré (GBS) é uma neuropatia autoimune aguda que afecta o
SNP. Pertence a um conjunto de neuropatias autoimunes na qual estão envolvidos AAc
conta vários epitopos neuronais. As manifestações clínicas incluem fraqueza dos
membros, sendo a GBS considerada a causa mais comum de paralisia aguda
generalizada.
Existem 4 subtipos de GBS que diferem quanto à fisiopatologia, perfil imunológico e
distribuição mundial: polineuropatia desmielinizante inflamatória aguda (AIDP),
neuropatia axonal motora aguda (AMAN), neuropatia axonal sensorial motora aguda
(AMSAN) e o síndrome de Miller Fisher (MFS).
Epidemiologia
O GBS ocorre por todo o mundo em crianças e adultos, homens e mulheres numa
proporção de 1,5:1 (ao contrário da maioria das DAI). A sua incidência é de 1,3 casos
por cada 100.000 habitantes.
Patogénese
A GBS é uma patologia mediada por processos imunitários. A patogénese dos
diferentes subtipos de GBS varia e é sumariamente descrita na Tabela 9, na página 34.
Verifica-se um risco aumentado de desenvolver GBS após vacinação, sobretudo com a
vacina do vírus Influenza.
Seis semanas antes do diagnóstico, calcula-se que cerca de dois terços dos doentes
tenham uma infecção, regra geral, uma gripe ou gastroenterite. Os microrganismos
normalmente associados a estas infecções são: Campylobacter jejuni, citomegalovírus,
Mycoplasma pneumoniae e o EBV, por esta ordem de incidência.
Julga-se que esteja envolvido na patogénese da doença, um mecanismo de mimetismo
molecular, no qual a semelhança entre sequências de péptidos do self e péptidos
estranhos, é suficiente para resultar numa activação cruzada, por parte dos péptidos
estranhos, de células T autoreactivas ou células B. Pensa-se que este fenómeno de
mimetismo molecular ocorra com o microrganismo Campylobacter jejuni (ver figura
seguinte).

Catarina Marinho Marques – Mestrado em Análises Clínicas 33
Figura 8 – Mecanismo de mimetismo molecular envolvido na resposta autoimune após infecção por C.
jejuni [49]
Manifestações Clínicas
Os sintomas mais precoces são parestesias e entropecimento nos dedos dos pés e das
mãos. A fraqueza generalizada atinge o seu pico por volta das 4 semanas após o início
dos sintomas. Os sintomas progridem com um padrão ascendente, dos membros
inferiores para os superiores. Há envolvimento dos músculos faciais (normalmente os
músculos oculares não são afectados), sendo que, em metade dos doentes surge paralisia
facial.[5] Em cerca de 25% dos doentes, a fraqueza dos músculos respiratórios é muito
acentuada levando à necessidade de respiração assistida. Cerca de 50% dos doentes
afirmam sentir dor e desconforto nas ancas, costas e coxas. O envolvimento do SN
autónomo pode levar a retenção da urina, obstipação, taquicardia, hipertensão, arritmia
cardíaca e hipotensão postural. Esta patologia é muitas vezes precedida de infecções no
tracto gastrointestinal ou respiratório.[1] [18]
Diagnóstico
O diagnóstico baseia-se em primeiro lugar no exame clínico, juntamente com o perfil
electrofisiológico, seguido do estudo dos AAc. Se necessário, faz-se a análise do LCR e
biópsia do nervo.

Catarina Marinho Marques – Mestrado em Análises Clínicas 34
Na GBS encontram-se Ac contra os gangliosídeos (GM). Os gangliosídeos são
esfingolípidos que se encontram em grande quantidade nas células ganglionares do
SNC, especialmente nas terminações nervosas, onde funcionam como receptores de
membrana. Os Ac anti-gangliosídeos estão implicados na patogénese desta doença.
Pensa-se que têm a sua origem em pools de células B estimuladas por Ag presentes nos
carbohidratos de certos microrganismos. Como exemplo, temos o C.jejuni que apresenta
estruturas gangliosídeos-like na sua parede celular, promovendo assim uma resposta
imunitária segundo o mecanismo de mimetismo molecular.[4]
Figura 9 – Semelhança entre o gangliosídeo humano GM1 e o epitopo GM1-like no C.jejuni [49]
Existem diferentes tipos de Ac anti-gangliosídeos consoante o subtipo de GBS.
Subtipo de GBS Patogénese
Distribuição
mundial: % nos
países ocidentais
Anticorpo
Polineuropatia
Desmielinizante
Inflamatória Aguda
(AIDP)
Lesão na bainha
de mielina
cerca de 90 desconhecido
Neuropatia Axonal
Motora Aguda (AMAN)
Lesão nos axónios cerca de 10 GM1, GM1b,
GD1a, GalNac-
GD1a
Neuropatia Axonal
Sensorial Motora Aguda
(AMSAN)
Lesão nos axónios residuais GM1, GM1b,
GD1a, GD1a
Síndrome de Miller Fisher
(MFS)
Desconhecida residuais GQ1b, GT1a
Tabela 9 – Patogénese, Distribuição e Anticorpos associados aos subtipos de GBS

Catarina Marinho Marques – Mestrado em Análises Clínicas 35
A nomenclatura dos ganglósidos é a seguinte: o prefixo G refere-se ao início da palavra
gangliosídeos – ganglio. A letra seguinte, M, D, T e Q, refere-se ao número de
moléculas de ácido siálico presentes, a numeração refere-se à ordem com que os
gangliosídeos migram nos cromatogramas.[4]
A detecção de Ac anti-gangliosídeos é feita por EIA e IB.
Figura 10 - Immunoblot com Ag relevantes para o diagnóstico de patologias do SN [43]
O exame electrofisiológico é importante para distinguir AIDP (lesão na bainha de
mielina, forma desmielinizante) de AMAN/AMSAN (lesão nos axónios, formas
axonais). O LCR apresenta poucos leucócitos e um aumento de proteínas que atinge o
pico entre a 2ª e a 4ª semana.[5]
Existem critérios clínicos, descritos por Asbury e Cornblaths, (ver figura seguinte) e
critérios electrofisiológicos, mas para estes últimos não há consenso.

Catarina Marinho Marques – Mestrado em Análises Clínicas 36
Figura 11 – Critérios clínicos para o diagnóstico do GBS [1]
Como a resposta dos Ac aos carbohidratos é independente da célula T, pensa-se que não
hajam associações HLA.
Tratamento
Tal como a maioria das neuropatias imunes, recorre-se à PE e à IVIg, sendo este último
menos propenso a complicações subsequentes. O uso de CE, usados noutras DAI do
SN, não parece ser eficaz no tratamento da GBS.[1]
Prognóstico
Existe uma elevada taxa de recuperação destes doentes (entre 4 e 15% morrem), apesar
de cerca de 20% apresentarem sequelas ao nível do SNP permanentes. No entanto, nos
doentes que recuperam, as forças voltam lentamente e em primeiro lugar nos membros
proximais, e depois nos distais.
A existência de o anticorpo anti-GM1 de classe IgG1 sugere um pior prognóstico, face
ao Ac anti-GM1 de classe IgG3, que indica melhor prognóstico.[5]

Catarina Marinho Marques – Mestrado em Análises Clínicas 37
ESCLEROSE MÚLTIPLA
A Esclerose Múltipla (MS) é a doença inflamatória do SNC mais comum. É uma
doença crónica que se caracteriza por infiltrados perivasculares de células inflamatórias
mononucleadas, desmielinização e perda de axónios, com formação de múltiplas placas
no cérebro e espinal medula; daí ser também chamada esclerose em placas. O percurso
clínico e a fisiopatologia são variáveis, já que na MS surgem remissões e recaídas, o que
torna esta doença muito heterogénea. O diagnóstico baseia-se sobretudo na clínica e na
exclusão de outras doenças.[1] [5] [34]
Epidemiologia
Surgem cerca de 60 casos por cada 100.000 habitantes na Europa e EUA. A incidência é
de cerca de 3-4,5 casos em cada 100.000 habitantes por ano. Surge sobretudo no adulto
jovem, por volta dos 20-40 anos, ocorrendo o pico de incidência por volta dos 30 anos.
A MS afecta três vezes mais as mulheres do que os homens.[1] [5]
Patogénese
A MS é uma doença multifactorial que resulta da interacção entre genes de
susceptibilidade, factores ambientais e factores imunológicos.
Julga-se que seja mediada por linfócitos Th1 autoreactivos, que proliferam, secretam
mediadores pró-inflamatórios e metaloproteinases. Activam e interagem com a barreira
hematoencefálica, penetrando depois no cérebro, onde são reactivados por
autoantigénios locais. Estes AAg são apresentados por moléculas de MHCII e expressos
à superfície de células da microglia, astrócitos e macrófagos. A partir daqui inicia-se
uma cascata de acontecimentos que culmina na activação de componentes do SI e no
ataque à bainha de mielina, axónios e glia. Destes acontecimentos resultam edema,
desmielinização, transecção axonal, perda de oligodendrócitos e activação de astrócitos,
que contribui para a disfunção neurológica, formação de placas e gliose.[1]
Em 2003 foram descobertas as células Th17. Pensa-se que as células Th17 tenham um
papel no tratamento da MS. Estas células produzem IL-17, uma citocina envolvida no
desenvolvimento de várias doenças inflamatórias. As células Th17 têm um papel
importante como mediadores autoimunes da neuroinflamação, à semelhança das células
Th1. Dados recentes sugerem que, tanto as células Th1 como as células Th17 são
capazes de induzir e promover a doença. Assim, será necessária mais informação para

Catarina Marinho Marques – Mestrado em Análises Clínicas 38
perceber a função destas células na patogénese da MS, já que algumas moléculas
relacionadas com as Th17 surgem como bons alvos para futuras estratégias
terapêuticas.[57]
Pensa-se que a exposição a agentes infecciosos, como o EBV possa estar associada ao
aparecimento da MS. O EBV infecta células B em repouso que são activadas e
proliferam, sendo depois eliminadas por linfócitos citotóxicos T CD8+. Persistem então
células B de memória. O EBV tem um pentapéptido antigénico nuclear que é homólogo
do epitopo da proteína básica da mielina (MBP). Para além disso o EBV também induz
a expressão, à superfície da célula B, de um AAg que é invulgarmente expresso no
cérebro de doentes com MS. Estes factos explicam como o EBV pode estimular a
geração de células T autoreactivas específicas da mielina, na MS. Assim sendo, o risco
de desenvolver MS aumenta muito com a infecção do vírus Epstein-Barr.[34]
Manifestações Clínicas
O doente de MS é geralmente um adulto jovem que apresente manifestações
neurológicas atribuíveis a lesões da substância branca. Os sintomas incluem debilidade
muscular, parestesias, lesão cerebelosa (ataxia e vertigo), diplopia, visão turva e
desconforto na bexiga.
A MS pode evoluir de maneiras diferentes (ver figura 11, abaixo). No início da doença
pode ter uma evolução do tipo recaída-remissão (RR-MS), o que ocorre em 85% dos
casos, ou do tipo primária progressiva (PP-MS), que ocorre em 15% dos casos. Os
sintomas das recaídas desenvolvem-se normalmente dentro de horas e persistem por
dias ou semanas. A evolução do tipo PP-MS consiste numa mielopatia progressiva,
sendo mais comum em homens com idade superior a 40 anos. Na Tabela 10 estão
registados os sintomas iniciais da MS. Com o passar do tempo, os doentes vão
convertendo a fase RR-MS numa esclerose múltipla do tipo secundária progressiva (SP-
MS). Esta mudança ocorre em cerca de 50% dos doentes, 10 anos após o início da
doença. Na fase SP-MS as recaídas diminuem ou cessam, e o grau de deficiência
aumenta. Um pequeno grupo de doentes com MS (cerca de 5%), apresenta ainda uma
fase progressiva-recaída, que é uma fase crónica da doença, que se caracteriza por
surtos. Nesta fase a severidade dos sintomas, a taxa de recaídas e a progressão do grau
de deficiência varia de indivíduo para indivíduo[5]. Os sintomas e prevalência da fase
crónica da doença estão enumerados na Tabela 10.

Catarina Marinho Marques – Mestrado em Análises Clínicas 39
Sintomas Iniciais Prevalência
(%) Sintomas Crónicos
Prevalência
(%)
Sintomas sensoriais 35-40 Distúrbios visuais, Fadiga 90
Fraqueza em um ou mais
membros 25-40
Ataxia, Crises paroxísticas,
Declínio Cognitivo 50-75
Perda da visão 17-29 Depressão -
Diplopia 12 Disfunção sexual -
Alteração do balanço e da
marcha 18
Sintomas intestinais e
incontinência -
Vertigo 5 Disfagia -
Sintomas intestinais e
incontinência 5 Perturbações no sono -
Tabela 10 – Sintomas iniciais e crónicos da MS. Adaptado de Shoenfeld et al [1]
Figura 12 – Padrões de evolução da MS [51]
Diagnóstico
A MS surge na substância branca do SNC com infiltrados de células inflamatórias
(linfócitos T, monócitos/macrófagos, células B e plasmócitos), desmielinização,
redução do número de oligodendrócitos, axónios transectados e proliferação de
astrócitos, resultando em gliose.

Catarina Marinho Marques – Mestrado em Análises Clínicas 40
Estão definidos 4 padrões da doença com base na localização e extensão das placas,
mecanismos imunopatológicos, activação do complemento e padrões de destruição dos
oligodendrócitos. Como podemos ver pela Tabela 11, na maior parte das vezes temos
um padrão de desmielinização com produção de Ac.
Tabela 11 – Heterogeneidade da patologia da MS. Adaptado de Shoenfeld et al [1]
O diagnóstico é feito por: (1) dados clínicos, pela anamnese e pela exclusão de outras
doenças; (2) dados laboratoriais, pelo estudo do LCR; (3) dados imagiológicos, através
da RM.
O estudo do LCR poderá apresentar uma ligeira pleocitose leucocitária, proteínas
normais ou ligeiramente aumentadas, aumento de imunoglobulinas e a presença de
bandas de IgG oligoclonal, o que indica síntese intratecal de imunoglobulinas e
patologia inflamatória. Estas situações ocorrem em cerca de 90% dos doentes, o que
torna a análise do LCR bastante útil para o diagnóstico da MS.[1] [5]
Figura 13 – Presença de bandas oligoclonais em LCR de doentes com MS [50]
No LCR podem ainda ser detectados dois tipos de AAc, que surgem sobretudo no início
da doença:
Padrão I Padrão II Padrão III Padrão IV
Incidência
(%)
12 53 30 4
Possíveis
mediadores
Desmielinização
mediada por
macrófagos e
linfócitos
citolíticos
Desmielinização
mediada por Ac
anti-MOG
Oligodendropatia
distal e apoptose
Isquémia,
toxicidade
induzida por
vírus
Degeneração
oligodendroglia
primária
Defeitos
metabólicos

Catarina Marinho Marques – Mestrado em Análises Clínicas 41
1. O anticorpo anti-proteína básica da mielina (Ac anti-MBP)
A determinação de Ac anti-MBP é sobretudo de classe IgM e são detectados por
IF e ELISA. [17]
Figura 14 – Ac anti-MBP Método: IFI Substrato: Cerebelo e Secção de um nervo [12]
2. O anticorpo anti-glucoproteína mielínica oligodendrocitária (Ac anti-MOG),
pode ser detectado por ELISA ou immunoblot. A MOG localiza-se na superfície
externa da mielina.
Outros dados laboratoriais, para além da detecção de AAc, são úteis para excluir outras
doenças.[1] [4] [5] [45]
O estudo imagiológico evidencia a desmielinização característica da MS: tempos de
condução motora prolongados e latência atrasada dos potenciais visuais,
somatosensoriais e auditivos. A RM é o teste mais sensível para demonstrar as lesões da
MS. Ela permite avaliar a carga da lesão, medir a atrofia do cérebro, fazer o seguimento
da doença, ajudar no prognóstico e auxiliar ensaios clínicos.[33]
Já existiam critérios para o diagnóstico clínico, com base na lesão da substância branca
do SNC, antes de a RM ser usada para auxílio do diagnóstico. No entanto, em 2005, os
critérios de diagnóstico foram revistos. Criaram-se os Critérios de Mcdonald, também
eles revistos mais tarde, juntando os dados imagiológicos, tudo com o objectivo de um
diagnóstico mais precoce e de um seguimento da doença.[1]

Catarina Marinho Marques – Mestrado em Análises Clínicas 42
Figura 15 – Critérios de diagnóstico da MS segundo McDonald [1]
A MS é uma doença multifactorial com uma base genética muito complexa. Pensa-se
que os genes que codificam para moléculas de HLA e citocinas, estejam envolvidos no
desenvolvimento e patogénese da MS. A associação genética mais bem estabelecida
com a MS reside no locus HLA DRB1. Apesar desta associação HLA não ser única, é a
mais frequente.[33] [34]
Tratamento
O tratamento usado depende do estadio da doença.
Para situações agudas o tratamento com CE está indicado, excepto se se tratar de um
ataque severo ao SNC. Nesse caso, recorre-se à PE.

Catarina Marinho Marques – Mestrado em Análises Clínicas 43
Para a manutenção da actividade da doença são usados três interferões β, que atrasam o
desenvolvimento de MS definitiva, o acetato de glatirámero, um fármaco que ilude o SI,
e o natalizumab, um anticorpo monoclonal.
Como tratamento complementar da MS, recorre-se à fisioterapia, dieta específica e a
intervenções sociais e psicológicas, de forma a aliviar os sintomas desta doença.
Menos frequentemente mas também usado no caso dos outros métodos não resultarem,
recorre-se a: IVIg, transplante de células estaminais e administração de citocinas, que
alteram o SI de um estado defeituoso para um estado normal.[1] [3]
No que se refere a esta doença, a medicina tem evoluído no sentido de tratar o doente,
em vez de tratar a doença, pela criação de um tratamento personalizado, atento ao perfil
genético, subtipo e actividade da doença.[1]
Estudos recentes indicam que a utilização das NPC(Neural Progenitor Cells) poderá ter
sucesso no tratamento da MS. As NPC são células multipotentes que existem no SNC
de indivíduos adultos e que têm a capacidade de migrar, proliferar e diferenciar-se em
neurónios e células da glia. Reduzem a inflamação e promovem a remielinização, pela
libertação de factores neurotróficos e citocinas imunoreguladoras em locais lesionados.
No entanto, o seu benefício é limitado na inflamação crónica do SNC devido à
deficiente neurogénese. Apesar dos benefícios, continuam a existir dúvidas de que as
NPC se diferenciem em células neuronais e ajudem à regeneração do tecido nervoso in
vivo. Este facto poderá dever-se ao microambiente inflamatório do SNC estabelecido
pelos linfócitos T CD4+ e CD8+ específicos da mielina, que inibem a neurogénese das
NPC. Assim, para que estas células sejam reconhecidas como uma opção terapêutica, é
preciso que superem o microambiente desfavorável e conduzam à regeneração dos
tecidos nervosos. [56]
Prognóstico
A doença progride mais rápido nos indivíduos que apresentam períodos de RR-MS
(recaída-remissão).[35]
A observação, o diagnóstico precoce e o tratamento médico apropriado evitam
complicações, como por exemplo as infecções de alguns orgãos. Mesmo assim, a
esperança de vida dos doentes é aumentada apenas moderadamente.

Catarina Marinho Marques – Mestrado em Análises Clínicas 44
A idade em que os sintomas tiveram início é o principal factor de prognóstico: quanto
mais precocemente aparece a doença, mais rápida será a sua progressão.
A ordem do aparecimento das manifestações clínicas também é importante na predição
da doença: se em primeiro lugar surgem dificuldades visuais haverá um melhor
prognóstico do que se surgirem inicialmente problemas de coordenação motora dos
membros.
Apesar das terapias que visam melhorar a qualidade de vida do doente, ainda não existe
cura para a MS.

Catarina Marinho Marques – Mestrado em Análises Clínicas 45
ENCEFALITE LÍMBICA
A Encefalite Límbica (LE) é uma encefalopatia autoimune na qual o síndrome
paraneoplásico ocorre secundariamente a uma reacção autoimune, não havendo
participação directa da neoplasia. Caracteriza-se por manifestações neurológicas
atribuídas ao lobo temporal mediano - zona límbica: perda de memória a curto prazo,
depressão, irritabilidade, alterações na personalidade. Na maioria das vezes, as
manifestações clínicas ocorrem antes do diagnóstico do tumor.[28]
Epidemiologia
A LE é uma doença rara, que ao contrário da maior parte das DAI, surge mais nos
homens.
A idade de início da doença é por volta dos 55 anos.
Patogénese
A LE é uma DAI que pode ter ou não origem paraneoplásica. Quando paraneoplásica
aparece associada ao SCLC, a cancro da mama e cancro testicular. Os primeiros estudos
evidenciavam que a doença surgia apenas em mulheres que apresentavam um teratoma.
Mais tarde percebeu-se que afecta igualmente mulheres sem teratoma, homens e
crianças. Em cerca de metade dos casos a LE está associada a neoplasia, e na outra
metade está associada a um processo autoimune.[13] [21] [22]
A LE é uma DAI cuja clínica pode anteceder o diagnóstico da neoplasia até 6 anos. Em
cerca de 50% dos doentes com LE, não se detecta a localização da neoplasia primária
num primeiro diagnóstico.
O tumor localiza-se fora do SNC e apresenta proteínas de superfície específicas do
SNC, que são reconhecidas como Ag. Os Ac produzidos como resposta a estes Ag,
atravessam a barreira hemato-encefálica e reagem com células específicas do SNC ou
SNP.[1] [13]
Manifestações Clínicas
O doente com LE apresenta um quadro inicial com sintomas semelhantes a depressão,
ansiedade, acentuado desinteresse social e apatia.

Catarina Marinho Marques – Mestrado em Análises Clínicas 46
Posteriormente, o doente apresenta défice de memória, perda progressiva de
consciência, agitação psicomotora, associação com sintomas psiquiátricos (psicose,
delírio), crises epilépticas e demência de progressão rápida.[13] [36]
Diagnóstico
O diagnóstico de LE é clínico, imagiológico e laboratorial.
No diagnóstico imagiológico, a RM mostra um sinal intenso em ambos os lobos
temporais, em cerca de 50% dos casos.[1]
A análise laboratorial pode ser feita no soro ou LCR. O LCR está alterado em cerca de
60% dos casos, revelando uma moderada pleocitose, aumento de proteínas e presença
de bandas oligoclonais.[1]
Em 40% dos doentes os AAc são negativos. Nos restantes 60% podem aparecer:
Anticorpos contra Ag paraneoplásicos clássicos: Hu, Ma2, CV2, anfifisina. O
Ag Hu está associado aos casos de SCLC, aparecendo em 90% dos doentes com
LE e neoplasia associada. O Ag Ma2 está associado ao cancro testicular, surge
em 90% dos doentes que apresentam esta neoplasia.[1] [13]
Anticorpos contra Ag da membrana celular: receptores do glutamato (do tipo
NMDA e do tipo AMPA), canais de potássio dependentes da voltagem (VGKC).
Os Ac anti- receptor do glutamato tipo NMDA (NMDAr) aparecem em
indivíduos jovens e estão associados a cancro do ovário.
Figura 16 – Receptor do Glutamato (tipo NMDA) [43]

Catarina Marinho Marques – Mestrado em Análises Clínicas 47
A detecção de Ac anti-NMDAr, quer no soro quer no LCR, é muito útil, já que
aparecem em 59% dos doentes com LE e tumor associado. Os Ac anti-NMDAr são
detectados por IFI no hipocampo de rato. O padrão é característico, mas não é
específico.[22] [28], [43]
Rat Hippocampus Rat Cerebellum
Figura 17 – Ac anti-NMDAr. Método: IFI Substratos: Hipocampo e cerebelo de rato [43]
Os Ac anti-VGKC são detectados em cerca de 50% dos doentes com LE.[13]
Os critérios de diagnóstico sugeridos são:
Síndrome demencial com sintomas límbicos;
Quadro de progressão subaguda;
Confusão mental, alterações dos níveis de consciência, sintomas psiquiátricos;
Um ou mais, dos seguintes: RM compatível, PET compatível, pleocitose com
hiperproteinorraquia ou bandas oligoclonais, anticorpos positivos;
A PET está indicada para o diagnóstico do tumor.
A LE é uma doença subdiagnosticada, sendo muitas vezes tomada por “encefalite de
origem desconhecida”, “psicose induzida por drogas” e “início de epilepsia”.[43]
Tratamento
Após o tratamento da neoplasia de base, os sintomas podem desaparecer por completo.
O tratamento com IVIg e PE parece ser eficaz. A existência de Ac anti-Ma2 necessita de
imunoterapia após o tratamento oncológico.[1]
Na figura 17 é possível ver como a cirurgia e a PE, levam à diminuição do título de Ac.

Catarina Marinho Marques – Mestrado em Análises Clínicas 48
Figura 18 – Monitorização dos Ac anti-NMDAr [43]
Prognóstico
A doença é agressiva, mas potencialmente reversível e tratável. O importante é que seja
feito um diagnóstico precoce, o tratamento adequado e remoção do tumor.
Neoplasias que se manifestem com síndromes paraneoplásicos apresentam melhor
prognóstico e evolução para tratamento definitivo. Mesmo assim, a existência de Ac
anti-Hu, anti-CV2, anti-anfifisina, sugerem um pior prognóstico apesar das terapêuticas
oncológicas e da imunoterapia.
A existência de Ac anti-NMDAr é de bom prognóstico, já que há uma boa resposta à
terapêutica em mais de 90% dos casos.[1] [22] [36]

Catarina Marinho Marques – Mestrado em Análises Clínicas 49
NEUROMIELITE ÓPTICA
A neuromielite óptica (NMO), tendo sido primeiramente descrita por Eugène Devic, é
também conhecida como síndrome de Devic. É uma patologia inflamatória recorrente
que leva à destruição da bainha de mielina, provocando lesões nos nervos ópticos e
espinal medula. Durante muitos anos pensou-se que pertenceria à MS, mas com
critérios laboratoriais, clínicos e imagiológicos, chegou-se à conclusão que é por si só,
uma doença.[1] [28]
Figura 19 - Corte transversal do encéfalo humano [43]
Epidemiologia
A NMO é rara na população caucasiana, representando menos de 1% das doenças
desmielinizantes do SNC. Apresenta alta incidência na população Asiática, Africana e
Sul-americana.
É três a cinco vezes mais frequente no sexo feminino, com início, em média, aos
40 anos de idade.[52]
Patogénese
O quadro clínico, caracteriza-se pela associação simultânea ou sequencial de mielite
transversa, extensa longitudinalmente, e neurite óptica uni ou bilateral.
A doença apresenta duas formas: recorrente e monofásica. As formas recorrentes
apresentam-se com síndromes medulares parciais, e disfunções motoras e sensitivas
leves a moderadas, e sem alterações esfincterianas. No entanto, ao longo da doença
ocorrem eventos de mielites completas em quase a metade dos casos.

Catarina Marinho Marques – Mestrado em Análises Clínicas 50
A forma monofásica caracteriza-se por disfunção motora e esfincteriana, mais grave na
fase aguda da mielite inicial e com mais sequelas. Nesta forma ocorre um único
episódio de mielite transversa e neurite óptica de instalação simultânea ou espaçada por
dias.
Na maioria dos casos, em número superior a 80%, a doença assume a forma recorrente.
Manifestações Clínicas
A NMO causa cegueira, mobilidade condicionada e perda de controlo da bexiga e
intestino. Em tempos foi controverso se a NMO seria por si só uma doença ou se
representaria uma variação da MS. No entanto, hoje é vista como uma patologia isolada,
já que foram encontrados factos que, não se verificam ou raramente se verificam, na
MS:
Envolvimento do nervo óptico;
Zonas necrosadas muito extensas;
Lesões extensivas na espinal medula;
Ligação de Ac Anti-NMO de classe IgG aos vasos sanguíneos no cérebro;
Existência de um autoantigénio nas junções astrócitos-endotélio da barreira
hemato-encefálica – Aquaporina-4.
Diagnóstico
Tal como outras DAI, o diagnóstico é clínico, imagiológico e laboratorial.
Há critérios de diagnóstico para a NMO:
A existência de neurite óptica;
A existência de mielite, e pelo menos 2 dos 3 seguintes:
Evidência, na RM, de uma lesão na espinal medula em 3 ou mais segmentos;
RM demonstra que não é MS;
Existência de Ac anti-NMO IgG.
A mielite é uma reacção autoimune na espinal medula, que pode estar associada a
infecções virais, DAI sistémicas e sarcoidose.

Catarina Marinho Marques – Mestrado em Análises Clínicas 51
A imagiologia, demonstra lesões na espinal medula e uma evolução aguda. A presença
de lesões na RM cerebral, inicialmente considerada como critério diagnóstico de
exclusão, verifica-se em até 60% dos doentes, apesar da maioria não ter tradução
clínica.[52]
A análise do LCR evidencia pleocitose e aumento de proteínas, mas geralmente sem
bandas oligoclonais, contrariamente ao que ocorre na MS.
Os Ac anti-NMO de classe IgG e Ac anti-Aquaporina-4 são marcadores serológicos
muito sensíveis da NMO. O Ac anti-NMO IgG é um anticorpo monoclonal de células B
envolvido na activação da cascata do complemento e recrutamento das células
inflamatórias. A sensibilidade dos Ac anti-NMO IgG ronda os 73% e a especificidade
os 91%.
Os Ac anti-Aquaporina-4 surgem no início da doença e são mais específicos e sensíveis
do que os Ac anti-NMO-IgG, sobretudo quando determinados por IF. A importância
dos Ac anti-Aquaporina-4 reside no facto de ajudarem à distinção entre MS e NMO.[37]
[40] [52]
Figura 20 – Ac anti-Aquaporina 4. Método: IFI Substrato: cerebelo de macaco [6]
Tratamento
O tratamento da NMO é feito essencialmente com terapêuticas imunossupressoras e por
PE.
Como tratamento inicial da fase aguda recorre-se a terapêutica com CE. Em segunda
linha, a PE é utilizada.[1]

Catarina Marinho Marques – Mestrado em Análises Clínicas 52
Para a prevenção de recaídas, os imunossupressores usados são: azatioprina, o
micofenolato de mofetil, a mitoxantrona e o rituximab.[52]
Prognóstico
O prognóstico é reservado, com grave repercussão funcional. A sobrevida após cinco
anos é cerca de 68% para as formas recorrentes, e de 90% para as formas monofásicas,
sendo a principal causa de morte o compromisso respiratório que ocorre na lesão
medular grave.[52]

Catarina Marinho Marques – Mestrado em Análises Clínicas 53
SÍNDROME DE STIFFMAN
O síndrome de Stiffman (SS) foi inicialmente descrito por Moersch e Woltmann em
1956. Moersch e Woltmann identificaram o SS em doentes que apresentavam rigidez
progressiva lenta envolvendo os músculos esqueléticos e espasmos axiais. Os doentes
apresentam fracturas e deformidades.[14]
Epidemiologia
O SS é uma patologia tão rara, que não é possível estabelecer uma prevalência exacta,
embora se calcule que surge em menos de 1 em cada milhão de pessoas.[54]
Afecta sobretudo mulheres, numa proporção de 2:1.
Embora a maioria dos casos estejam descritos em adultos, existem casos descritos em
crianças.[53]
Patogénese
O SS é um PNS que pode surgir associado ao cancro da mama e ao SCLC.
Pode ainda aparecer em conjunto com outras doenças: em 30% dos casos com a
diabetes insulino-dependente, e em 40% dos casos com DAI, como a tiroidite de
Hashimoto, doença de Graves, MG e anemia perniciosa.
Manifestações Clínicas
As manifestações clínicas incluem rigidez muscular progressiva e espasmos,
envolvendo primeiro os músculos axiais e expandindo-se para os músculos proximais.
O doente desenvolve uma hiperlordose, marcha incerta e quedas frequentes. Os
músculos são rígidos à apalpação. Em 10% dos casos verifica-se epilepsia generalizada.
O comprometimento do sistema GABAérgico inibitório pode causar rigidez muscular e
estar implicado na prevalência de epilepsia, instabilidade autonómica, na qual ocorre
taquicardia, pressão arterial lábil e sudorese, e no aparecimento de sintomas
psiquiátricos.[1] [14]
Diagnóstico
O diagnóstico é essencialmente laboratorial. A análise do LCR não apresenta alterações,
embora possam surgir bandas oligoclonais. São detectados dois tipos de AAc:

Catarina Marinho Marques – Mestrado em Análises Clínicas 54
1. Anticorpo anti-anfifisina.
A anfifisina é uma proteína sináptica, expressa nos neurónios, células da retina e
espermatócitos. O Ac anti-anfifisina é detectável por IFI e IB.
Figura 21 – Ac anti-anfifisina. Método: IFI Substrato: cerebelo [12]
2. Anticorpo anti-descarboxilase do ácido glutâmico 67 (Ac anti-GAD67).
O Ac anti-GAD67 surge em cerca de 60% dos doentes com SS. A sua detecção é
possível por EIA, RIA ou IFI.
A descarboxilase do ácido glutâmico é uma proteína que aparece no SNC e SNP,
nos ilhéus pancreáticos, testículos, ovários, timo e estômago. A sua função é a de
catalisar a descarboxilação do ácido glutâmico em ácido gama amino butírico
(GABA). Por sua vez, as funções do GABA, como neurotransmissor inibitório do
cérebro, incluem o controlo e libertação das vesículas de insulina. O GABA tem
duas isoformas, GAD65 e GAD67, que partilham 68% de homologia. O GAD65 é
encontrado nas células β dos ilhéus pancreáticos, e o GAD67 nas células α. Assim
sendo, os Ac anti-GAD65 estão associados com a diabetes, enquanto que os Ac-
anti-GAD67 aparecem no SS.[6]

Catarina Marinho Marques – Mestrado em Análises Clínicas 55
Figura 22 – Ac anti-GAD. Método: IFI Substrato: cerebelo e pâncreas [12]
O exame imagiológico não apresenta alterações, pelo que não se revela muito útil para o
diagnóstico.
Tratamento
Para além dos habituais tratamentos: IVIg, uso de drogas imunossupressoras e PE, são
ainda utilizados:
Benzodiazepínicos, como o diazepam, para cessar a actividade motora;
Baclofeno, que é um relaxante muscular que actua nos receptores GABA, a nível
medular, deprimindo o SNC por meio de uma diminuição dos
neurotransmissores glutamato e aspartato;
Bloqueio dos nervos periféricos;
Anestesia geral;
Sono induzido.
Prognóstico
Os estímulos externos têm um efeito negativo nas melhoras do doente, e alternativas
como anestesia geral e sono induzido, têm um bom prognóstico. A terapêutica
imunossupressora e a PE, também apresentam bons resultados nas melhoras do doente.

Catarina Marinho Marques – Mestrado em Análises Clínicas 56
SÍNDROMES PARANEOPLÁSICOS
Os síndromes paraneoplásicos são complicações provenientes de doenças tumorais, que
não advêm do tumor, nem das suas metástases, nem têm causas infecciosas,
metabólicas, vasculares ou terapêuticas. Os PNS têm uma base autoimune que se
caracteriza pela resposta a Ag onconeuronais que são expressos nas células tumorais e
nas células neuronais. As manifestações clínicas dependem da região do SN afectado.
Um diagnóstico precoce é crucial para o sucesso terapêutico.
Os PNS abrangem muitas patologias, algumas confinadas ao SNC, outras ao SNP, e
outras às junções neuromusculares e músculos. Na tabela seguinte enumeram-se todos
aqueles que são considerados síndromes neurológicos paraneoplásicos.
Síndromes do SNC Síndromes do SNP
Síndromes das junções
neuromusculares e
músculos
Encefalomielite
Encefalite Límbica
Encefalite do tronco
encefálico
Degeneração cerebelar
subaguda
Opsoclonus-mioclonus
Síndrome de Stiffman
Mielopatia Necrosante
Doença neuronal motora
Neuropatia sensorial
subaguda
Neuropatia sensorio-
motora
Neuropatia com vasculite
Neuropatia autonómica
Pseudoobstrução
gastrointestinal crónica
Pandisautonomia aguda
Miastenia Gravis
Síndrome de Lambert-
Eaton
Neuromiotonia aguda
Dermatomiosite
Miopatia necrotizante
aguda
Tabela 12 – Síndromes Paraneoplásicos [1]
Epidemiologia
Os PNS são síndromes raros que afectam menos de 1% de todos os doentes com cancro.
Os cancros mais frequentes são o cancro do pulmão, mama e ovário, timoma e doença
de Hodgkin. A idade a que surge a doença ronda os 55 anos. Regra geral, afectam mais
as mulheres do que os homens numa proporção de 2:1.

Catarina Marinho Marques – Mestrado em Análises Clínicas 57
Patogénese
A doença deve-se mais a uma resposta imune celular, do que a uma acção directa dos
Ac. Pensa-se que os PNS tenham origem na expressão ectópica, de Ag onconeuronais
em células tumorais. Estes Ag são idênticos aos que existem no cérebro. Uma resposta
imune mediada por células B e T citotóxicas resulta em infiltrados de células
inflamatórias, no SN e tecido tumoral, que levam ao aparecimento de Ac anti-neuronais
no soro e LCR. O ataque imunitário começa por ser dirigido contra o tumor, e mais
tarde indevidamente contra os tecidos neuronais, o que dá origem às manifestações
clínicas de acordo com o SN afectado. As células tumorais expressam Ag, que só
existem nos neurónios; são onconeuroproteínas. Estes Ag levam ao aparecimento de Ac
e de células T citotóxicas, ambos envolvidos na degradação dos neurónios.[10] [17]
Manifestações Clínicas
Nos PNS as manifestações clínicas são sobretudo neurológicas e aparecem antes do
diagnóstico do tumor.
Habitualmente os doentes desenvolvem um síndrome subagudo que causa lesões
severas e irreversíveis, na maior parte dos casos.
Um importante indício clínico é que o PNS pode apresentar-se como uma doença
multifocal que envolve zonas distantes e não relacionadas do SN.
Diagnóstico
O diagnóstico é imagiológico e laboratorial.
Os Ac contra Ag neuronais podem ser induzidos pela presença de um tumor. A
identificação de Ac anti-neuronais permite o diagnóstico da doença neurológica e a
localização do tumor. A detecção de Ac é bastante útil, já que estes podem surgir até 5
anos antes do aparecimento do tumor. Estes Ac são de classe IgG, e são detectados por
IF e confirmados por IB. A sua especificidade é elevada e apenas alguns doentes
seropositivos não têm cancro. A sensibilidade varia com os Ac. Embora sejam úteis
para o diagnóstico, é importante referir que não são exclusivos dos PNS, podendo ser
encontrados noutras doenças ou mesmo em indivíduos saudáveis.[1] [5] [17] [18], [28]
Na tabela seguinte evidenciam-se os Ac onconeuronais clássicos e respectivo tumor. Na
presença de qualquer um destes Ac, a probabilidade de existir tumor é superior a
95%.[38]

Catarina Marinho Marques – Mestrado em Análises Clínicas 58
Tabela 13 – Anticorpos onconeuronais e PNS associado [1] [18]
Para a determinação dos Ac é importante seguir uma estratégia de detecção
(sensibilidade) e confirmação (especificidade). Para que tal aconteça, deve combinar-se
tecidos (imunohistoquímica) com o uso de Ag isolados. Os Ac são assim detectados por
IF e posteriormente confirmados por IB. A técnica de IF usa como substrato, tecidos
(cerebelo, testículos, espinal medula, músculo cardíaco, músculo esquelético) de
macaco ou rato.[17] [18]
Posner sugeriu critérios de relevância destes AAc:
1. Um determinado Ac deve estar presente em um ou mais doentes com distúrbios
neurológicos e tumores correspondentes semelhantes, e deve ser raro o
aparecimento de falsos positivos ou de falsos negativos quando se testar o Ac.
2. A concentração de Ac no soro deve ser elevada.
3. Um título superior no LCR comparativamente ao título no soro, deve sugerir
síntese intratecal e assim evidenciar a relevância do Ac.
4. Os Ac devem reagir com a parte sintomática do SN e a natureza do Ag deve ser
identificada por imunohistoquímica e pela técnica de Western blot.

Catarina Marinho Marques – Mestrado em Análises Clínicas 59
O diagnóstico deve basear-se em (1) presença de cancro, (2) no síndrome clínico e (3)
na existência de Ac onconeuronais detectados laboratorialmente, sem suscitar dúvidas.
Os PNS são subdivididos em “definitivos” ou “possíveis”. É mandatório excluir outras
causas para os sintomas neurológicos antes de estabelecer o diagnóstico de PNS. [1]
Critérios de diagnóstico para PNS definitivo:
1. Um síndrome não clássico que melhora após tratamento do cancro sem
imunoterapia simultânea, desde que o síndrome não seja susceptível a remissão
espontânea.
2. Um síndrome não clássico com Ac onconeuronais (bem caracterizados ou não) e
cancro que se desenvolve dentro de 5 anos após o diagnóstico da doença
neurológica.
3. Um síndrome neurológico (clássico ou não) com Ac onconeuronais bem
caracterizados (anti-Hu, Yo, CV2, Ri, Ma2, ou anfifisina), e sem a presença de
cancro.
Critérios de diagnóstico para PNS possível:
1. Um síndrome clássico, sem Ac onconeuronais, sem cancro, mas com elevado
risco de ter um cancro subjacente.
2. Um síndrome neurológico (clássico ou não) com Ac onconeuronais parcialmente
caracterizados, e sem cancro.
3. Um síndrome não clássico, sem Ac onconeuronais, e com a presença de cancro
dentro de 2 anos após o diagnóstico. [1]
Tratamento
O tratamento passa em primeiro lugar, pela remoção do tumor.
As opções de tratamento usadas incluem o uso de CE, a administração de IVIg e a PE,
mas o seu sucesso é indeterminado já que o número de doentes tratados é baixo. [1]
Prognóstico
O importante para um bom prognóstico, é um diagnóstico precoce.

Catarina Marinho Marques – Mestrado em Análises Clínicas 60
Quando se trata um PNS, há que ter em conta o tipo de PNS: na LEMS, por exemplo, o
tratamento é feito com CE mas a resposta passa pelo sucesso do tratamento do tumor.
Noutros PNS, há um grau variável de efeitos neurológicos irreversíveis, portanto o
objectivo de qualquer tratamento deverá passar por estabilizar o doente em vez de
melhorar os sintomas neurológicos. No entanto, em certos casos é possível conseguir
melhoras: verificou-se que doentes com LE, cancro testicular e Ac anti-Ma2 apresentam
melhor prognóstico do que aqueles que, apresentado a mesma patologia, tenham Ac
anti-Hu.[1] [10]

Catarina Marinho Marques – Mestrado em Análises Clínicas 61
CONCLUSÃO
As DAI do SN podem surgir associadas a situações de neoplasia (PNS), ou
isoladamente como patologias autoimunes. Geralmente são pouco prevalentes e surgem
mais associadas ao sexo feminino. O diagnóstico é imagiológico, laboratorial e clínico,
e o prognóstico é na maioria das vezes positivo. São doenças tratáveis ou nas quais é
possível aliviar a sintomatologia e melhorar a qualidade de vida do doente. O tratamento
passa pela remoção do tumor, no caso de neoplasia associada, administração de
imunoglobulinas intravenosas, plasmaferese e toma de medicamentos adequados à
patologia, na maioria das vezes, corticosteróides.
De seguida é apresentado um quadro conclusivo, onde são apresentadas as patologias
abordadas, o respectivo SN afectado, autoanticorpos detectados, principais
manifestações clínicas e tratamento proposto.

Catarina Marinho Marques – Mestrado em Análises Clínicas 62
Patologia SN
afectado
Autoanticorpo
associado
Principais
manifestações
clínicas
Tratamento
Miastenia
Gravis
SNP Ac anti-AChR
Ac anti-MuSK
Ac anti-Músculo
Estriado
Fraqueza, dores
musculares
CE, azatioprina
Síndrome de
Lambert-Eaton
SNP Ac anti-VGCC
Ac anti-AGNA
Fraqueza, xerostomia amifampridina, CE,
azatioprina, PE
Síndrome de
Guillain Barré
SNP Ac anti-
Gangliosídeos
Fraqueza, parestesias,
entropecimento,
IVIg, PE
Esclerose
Múltipla
SNC Ac anti-MBP
Ac anti-MOG
Debilidade muscular,
parestesias, lesão
cerebelosa, diplopia,
visão turva e
desconforto na bexiga
IVIg, CE, PE, IS,
transplante,
fisioterapia,
intervenções
psicológicas
Encefalite
Límbica
SNC Ac anti-NMDAr
Ac anti-neuronais
(Hu, Ma2)
Ac anti-VGKC
Depressão, amnésia,
alucinações
IVIg, PE
Neuromielite
Óptica
SNC Ac anti-
Aquaporina 4
Cegueira, mobilidade
condicionada, perda de
controlo da bexiga e
intestino
PE, CE, IS
Síndrome de
Stiffman
SNC Ac anti-GAD67
Ac anti-ICA
Ac anti-Anfifisina
Rigidez lenta
progressive,
instabilidade
autonómica
IVIg, CE, IS,
Diazepam,
Baclofeno
Sono induzido
Anestesia geral
Bloqueio dos
nervos periféricos
Síndromes
Para-
neoplásicos
SNC ou
SNP
Ac anti-neuronais
(Hu, Ri, Ma2)
Ac anti-células de
Purkinje (Yo)
Ac anti-Anfisina
Ac anti-CV2
Neuropatias,
degeneração cerebelar
IVIg, PE, CE
Tabela 14 – Principais aspectos de cada patologia abordada.

Catarina Marinho Marques – Mestrado em Análises Clínicas 63
BIBLIOGRAFIA
1 Shoenfeld Y, Cervera R, Gershwin M, Editors. Diagnostic criteria in autoimmune
diseases.1st Ed. New Jersey, USA: The Humana Press Inc; 2008
2 Humbel RL, Editor. Autoanticorps et maladies autoimmunes. 2ª Ed. Paris, France:
Edition Scientifiques Elsevier; 1999
3 Shoenfeld Y, Abreu I, Branco J. Doenças autoimunes. 1ª Ed. EUA: Publicações Bio-
Rad Laboratories; 2008.
4 Shoenfeld Y, Gershwin ME, Meroni PL, Editors. Autoantibodies. Amsterdam:
Elsevier; 2007
5 Berrocal BG, Talaván T, Buitrago JM. Manual de Enfermedades autoinmunitarias y
autoanticuerpos. 1ª Ed. Barcelona, Espanha: A. Menarini Diagnostics; 2006.
6 Hughes RG, Surmacz MJ, Karim AR, Bradwell AR. Atlas of Tissue Autoantibodies.
3rd
Ed. Birmingham, UK: The Binding Site; 2008.
7 Gonçalves M. Doenças autoimunes do sistema nervoso. Medicina Interna,
1997;4(2):119-122
8 http://www.afh.bio.br/nervoso/nervoso1.asp [cited 2010June 08]
9 Meyer W, Schneider B, Orazio E, Klotz M, Schlumberger W, Stöcker W. Euroline
Anti-Ganglioside Profile: A serological test for for the diagnosis of inflammatory
peripheral neuropathies. Presented at the 3rd International Congress on Autoimmunity,
February 2002, Geneve, Switzerland.
10 Scheper T, Klotz M, Meyer W, Schlumberger W, Stöcker W. Reliable determination
of anti-neuronal autoantibodies in paraneoplastic neurological syndromes. Euroimmun
AG; Feb 2002.
11 Determination of Autoantibodies for Neurology, Euroimmun AG; Sep 2005
12 Autoantibodies against neuronal antigens. Euroimmun AG; Jun 2009.

Catarina Marinho Marques – Mestrado em Análises Clínicas 64
13 Conrad K, Chan EKL, Fritzler MJ, Sack U, Shoenfeld Y, Wiik AS, Editors. From
Etiopathogenesis to the Prediction of Autoimmune Diseases: Relevance of
Autoantibodies. 1st Ed. Germany: Pabst Science Publishers; 2007.
14 Conrad K, Fritzler MJ, Meurer M, Sack U, Shoenfeld Y, Editors. From Proteomics
to Molecular Epidemiology: Relevance of Autoantibodies. 1st Ed. Germany: Pabst
Science Publishers; 2002.
15 Conrad K, Humbel RL, Meurer M, Shoenfeld Y, Tan EM, Editors. Autoantigens and
Autoantibodies: Diagnostic Tools and Clues to Understanding Autoimmunity, 1st Ed.
Germany: Pabst Science Publishers; 2000.
16 Krüger C. RIA for antibodies diagnosis in myasthenia (ACHRAB, LEMS).
Euroimmun AG.
17 Stöcker W. Autoantibodies against structures of the nervous system paraneoplastic
neurological autoimmune diseases. Euroimmun AG.
18 Meyer W. Investigation of autoantibodies against neuronal antigens using IIFT, RIA
and EUROLINE-WB, Euroimmun AG.
19 Scheper T. Determination of antibodies against gangliosides in the diagnosis of
neurological diseases using the EUROLINE technique. Euroimmun AG.
20 Moll JWB, Henzen-Logmans SC, Splinter TAW, van der Burg MEL, Vecht ChJ.
Diagnostic value of anti-neuronal antibodies for paraneoplastic disorders of the nervous
system. J Neurol Neurosurg Psychiatry. 1990;53(11):940-3.
21 Dalmau J, Gleichman AJ, Hughes EG, Rossi JE, Peng X, Lai M, Dessain S,
Rosenfeld M, Balice-Gordon R, Lynch DR. Anti-NMDA-receptor encephalitis: case
series and analysis of the effects of antibodies. Available at:
www.thelancet.com/neurology Published online October 13, 2008.
22 Wandinger KP, Dalmau J, Borowski K, Probst C, Fechner K, Stöecker W.
Recombinant immunofluorescence assay for the detection of anti-glutamate receptor
(type NMDA) antibodies in the differential diagnosis of autoimmune encephalopathies.
Euroimmun AG.

Catarina Marinho Marques – Mestrado em Análises Clínicas 65
23 Antoine JC, Honnorat J. Anti-neuronal antibodies and central nervous system
diseases: contribution to diagnosis and pathophysiology, Service de Neurologie, Hôpital
de Bellevue, Saint-Etienne. Rev Neurol (Paris). 2000 Jan;156(1):23-33.
24 Humbel RL. Recherche et identification des autoanticorps dans les maladies
autoimmunes. Feuillets de biologie. 1999;40(230):23-8
25 Buskard NA. Plasma Exchange and Plasmapheresis, Can Med Assoc J. 1978;
119(7):681-3.
26 Romi F, Skeie GO, Gilhus NE, Aarli JA. Striational antibodies in myasthenia gravis:
reactivity and possible clinical significance, Arch Neurol. 2005;62(3):442-6.
27 http://fisiologia.med.up.pt/Textos_Apoio/Membranas/calcio.pdf [cited 2011 Feb 17].
28 Karim AR, Hughes RG, Winer JB, Williams AC, Bradwell AR. Paraneoplastic
Neurological Antibodies: A Laboratory Experience. Ann N Y Acad Sci. 2005
Jun;1050:274-85.
29 Catarino, Mª Manuela Beirão. Autoimunidade e Doenças Autoimunes, módulo de
Imunologia Complementar, Mestrado em Análises Clínicas, Faculdade de Farmácia da
Universidade de Lisboa, Novembro de 2009.
30 Abreu Isabel. Autoimmunity, módulo de Imunologia Complementar, Mestrado em
Análises Clínicas, Faculdade de Farmácia da Universidade de Lisboa, Dezembro de
2009.
31 www.wrongdiagnosis.com/a/ai/prevalence.htm [cited 2011 Feb 18]
32 Abreu Isabel, Bases Gerais das Reacções Antigénio-Anticorpo, módulo de
Imunologia Complementar, Mestrado em Análises Clínicas, Faculdade de Farmácia da
Universidade de Lisboa, Dezembro de 2009.
33 http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2994805/?tool=pubmed [cited 2011-
03-17]
34 Shoenfeld Y, Youinou P, Gershwin M, Editors. The environment geoepidemiology
and autoimmune diseases. 1st Ed. Oxford, UK: Elsevier; 2010.
35 Sindic, C. Prognosis in Multiple Sclerosis. Brussels, Belgium: Elsevier; 2006.

Catarina Marinho Marques – Mestrado em Análises Clínicas 66
36 http://rnp.fmrp.usp.br/aulas/Francisco/Encefalite_Limbica_ag.pdf [cited 2011 Mar 3]
37 Jarius S, Wandinger KP. 9th Autoantibody-Symposium, Dresden 2009
38 Graus F, Delattre J Y, Voltz R. Paraneoplastic Syndromes (PNS), J Neurol
Neurosurg Psychiatry 2004;75:1135
39 www.xa.yimg.com/kq/groups/22082565/ .../Sindromes+Paraneoplasicas.ppt, [cited
2011 Mar 7]
40 Paul F, Jarius S, Aktas O, Bluthner M, Bauer O, Appelhans H, Franciotta D,
Bergamaschi R, Littleton E, Palace J, Seelig HP, Hohlfeld R, Vincent A, Zipp F.
Antibody to aquaporin 4 in the diagnosis of neuromyelitis optica. PLoS Med.
2007;4(4):133
41Vincent A. Unravelling the pathogenesis of myasthenia gravis. Nature Reviews
Immunology 2002.Oct 2, 797-804 Available at: http://www.nature.com/nri/journal/v2/
n10 /full/nri916.html [cited 2011 Mar 3]
42 www.riversideonline.com [cited 2011 Mar 15]
43 Wandinger, Peter, Novel Antigenic Targets in Autoimmune Encephalitis:
NMDAR, LGI1 and more, Euroimmun AG, Congresso Medicina Interna, Porto, Fev
2011.
44 Dalmau J, Anti-glial nuclear antibody: marker of lung cancer-related paraneoplastic
neurological syndromes, J Neuroimmunol, 2005; 165(1-2):166-71.
45 Lima E, Guimarães J, Pereira A, Bodas A, Delgado L, Sá MJ. Determinação de
Anticorpos Anti-Mielina na Esclerose Múltipla. Porto: Arquivos de Medicina, 2008
22(4/5):107-11 Available at: http://www.scielo.oces.mctes.pt/pdf/am/v22n4-5/22n4-
5a01.pdf [cited 2011 Mar 3]
46 http://www.ema.europa.eu/docs/pt_PT/document_library/EPAR_-_Product_
Information /human/ 000262/WC500027361.pdf [cited 2011 Mar 14].
47 http://www.ema.europa.eu/docs/pt_PT/document_library/EPAR_-_Product_
Information /human /001032/WC500069915.pdf [cited 2011 Mar 15]
48 neuromed92.blogspot.com [cited 2011 Mar 15]

Catarina Marinho Marques – Mestrado em Análises Clínicas 67
49 www.bio.davidson.edu/courses/immunology/Students/spring2006/Blumer/GBS.html
[cited 2011 Mar 15]
50 esclerosemultipla.wordpress.com [cited 2011 Mar 16]
51 sistemanervoso.com [cited 2011 Mar 16]
52 Peixoto I, Ermida V, Torres A, Aparício I, André R, Caldas J. Doença de Devic,
Acta Med Port. 2010; 23(2):263-266
53 emedicine.medscape.com/article/1172135-overview [cited 2011 Mar 17]
54 www.hopkinsmedicine.org/neurology_neurosurgery/conditions_main/old/ stiff
_person _syndrome.html [cited 2011 Mar 17]
55 Sabater L, Titulaer M, Saiz A, Verschuuren J, Güre AO, Graus F, SOX1 antibodies
are markers of paraneoplastic Lambert–Eaton myasthenic syndrome. Neurology 2008;
70:924-928
56 Pluchino S, Martino G, The therapeutic plasticity of neural stem/precursor cells in
multiple sclerosis. J Neurol Sci. 2008; 15;265(1-2):105-10
57 Juszczak M, Głabiński A., Th17 cells in the pathogenesis of multiple sclerosis.
Postepy Hig Med Dosw. 2009; 63:492-501