ESTUDO DIRIGIDO-radioatividade
-
Upload
joao-rodrigues -
Category
Documents
-
view
142 -
download
1
Transcript of ESTUDO DIRIGIDO-radioatividade

ESTUDO DIRIGIDO RADIOATIVIDADE(TEXTO + EXERCÍCIOS)
No final do século XIX, um minério de urânio foi esquecido em cima de um filme fotográfico. Dias depois, o filme foi verificado e visualizaram uma marca derivada de "alguma coisa" que saia do minério de urânio. Na época, denominaram "essas coisas" de raios ou radiações. O fenômeno de liberação de radiações foi denominado de radioatividade e os elementos químicos que apresentavam esta propriedade foram chamados de elementos radioativos. São eles:
Rádio (Ra) = número atômico (Z) 88, massa atômica 226,0. Descoberto em 1898 por M.Curie, é dotado de intensa
radioatividade. O rádio é um metal alcalino terroso, que funde a 700 °C. Muito raro na natureza, é extraído da pechblenda. Desintegra-se com uma vida média de 1620 anos, produzindo uma emanação gasosa de hélio e de radônio. As radiações e emitidas pelo rádio são dotadas de grande poder bactericida e sua ação fisiológica acarreta a destruição dos tecidos e a suspensão da mitose, donde diversas aplicações terapêuticas (curieterapia).
Tório (Th) = número atômico 90, massa atômica 232,0. Densidade 12,1 g/cm3, e que funde a 1700 °C, aproximadamente, extraído da torita.
Urânio (U) = número atômico 92, massa atômica 238,0. Densidade de 18,7 g/cm3, extraído do óxido de urânio. Último elemento natural da classificação periódica, o urânio foi isolado em 1841 por Péligot. Trata-se de um sólido cinza-ferro, que funde a 1800 °C e se oxida facilmente. O óxido uranoso, ou urano, UO2, é um sólido negro, de propriedades básicas, a que correspondem os sais uranosos, verdes.
O minério de urânio mais importante é a pechblenda, ou uraninita, U3O8. Existem, todavia, muitos outros, que vêm sendo ativamente extraídos. Foi no urânio que Henri Becquerel descobriu a radioatividade. Em virtude da baixa concentração do urânio em seus diversos minérios (em geral menos de 1%), os tratamentos metalúrgicos compreendem inicialmente uma concentração física e, depois, uma concentração química dos sais de urânio. O urânio é utilizado, sobretudo como combustível nos reatores nucleares (barras, tubos, anéis). Pode também ser enriquecido num isótopo físsil, principalmente pelo processo seletivo da difusão gasosa do hexafluoreto através de paredes porosas, ou pelo processo de ultracentrifugação.
OBS: O dióxido de urânio (UO2) é a matéria-prima para fabricação do combustível nuclear nos reatores nucleares. Este óxido é muito pobre em urânio físsil (235U92), isto é, aquele que pode sofrer fissão nuclear. Apenas 0,7% dos átomos de urânio presentes nesse óxido são 235U92, os 99,3% restantes são de 238U92 (forma não-físsil). Assim, é necessário um novo tratamento para separar o isótopo físsil do isótopo não-físsil. Este tratamento é conhecido como enriquecimento do urânio.
Um dos processos para realizá-lo consiste em transformar o dióxido de urânio no gás hexafluoreto de urânio (UF6) e fazer este gás difundir-se por placas porosas. Com isso, consegue-se separar o (235UF6) do (238UF6). Em seguida, o gás hexafluoreto de urânio enriquecido volta a ser convertido em dióxido de urânio. Este óxido é o que constituirá finalmente o combustível nuclear.
Polônio (Po) = radioativo, de número atômico 84, massa atômica 210, que acompanha geralmente o rádio.
Os Perigos da Radiação
A radiação danifica os tecidos vivos. A radiação em excesso pode causar mudanças biológicas nos seres humanos ou em quem está em contato com esse tipo de radiação, por isso que as pessoas que trabalham com material radioativo devem se proteger. Os efeitos biológicos da radiação são diversos, entre eles o desenvolvimento de tumores, leucemia, queda de cabelo, redução na expectativa de vida, indução às mutações genéticas, má formação fetal, lesões de pele, olhos, glândulas e órgãos do sistema reprodutivo.
Materiais radioativos que escapam para o meio ambiente podem ser transportados por vários processos diferentes, um exemplo é o material radioativo que escapou do acidente na usina nuclear Chernobyl, o qual foi carregado por longas distâncias pelos ventos e contaminou parte da Europa (Figura 1).
Outro exemplo de contaminação por radiação é descartar material radioativo como lixo comum, porque chega a um aterro sanitário, e os elementos radioativos podem ser carregados pela água de chuvas para o solo de áreas cultivadas ou para reservatórios de água potável.
Um exemplo muito próximo a nossa realidade foi o acidente radiológico de Goiânia. A contaminação teve início em setembro de 1987, quando um aparelho utilizado em radioterapias das instalações de um hospital abandonado foi encontrado, na zona central de Goiânia. O instrumento, irresponsavelmente deixado no hospital, foi encontrado por catadores de papel, que entenderam

tratar-se de sucata. Foi desmontado e repassado para terceiros, gerando um rastro de contaminação, o qual afetou seriamente a saúde de centenas de pessoas.
Existem três tipos de radiação: alfa, beta e gama. Becquerel, Ernest Rutherford, da Nova Zelândia, e Marie e Pierre Curie, da França, foram os responsáveis pela sua identificação. A emissão que sofre pequeno desvio para o lado da placa negativa foi denominada emissão alfa (a), a que sofre desvio maior para o lado da placa positiva foi denominada emissão beta (b) e a que não sofre desvio foi chamada de emissão gama (g).
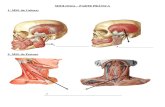
PARTÍCULA ALFA (): PARTÍCULA BETA () RADIAÇÃO GAMA 1- As partículas alfa são núcleos de hélio. Consistem em dois prótons e dois nêutrons. 2- O núcleo do rádio, no qual prótons e nêutrons se unem para formar uma partícula alfa. 3- A partícula alfa é emitida pelo núcleo. 4 - Partícula pesada.5 - Baixo poder de penetração.6 - Constituída de 2 prótons e 2 nêutrons, que se comportam como uma partícula única.
1- As partículas beta são elétrons em alta velocidade emitidos por certos átomos radioativos. 2- Os elétrons negativos formam-se pela desintegração de um nêutron. Os elétrons positivos formam-se pela desintegração de um próton. 3- A partícula beta é arremessada no instante em que se forma. Um neutrino, uma partícula quase sem peso, também é emitido.4 - 7000 vezes mais leve do que a partícula , portanto, mais rápida.5 - Maior poder de penetração e danificação do que a alfa.6 - Constituída por cargas negativas e, praticamente, em massa.
1- Os raios gama são partículas, ou fótons, de energia eletromagnética. 2- Núcleo do radio. 3- Os raios gama são liberados quando um núcleo, após uma desintegração radioativa, fica num estado de alta energia.4 - Ondas eletromagnéticas.5 - Velocidade próxima à da luz.6 - É a mais perigosa e ofensiva das três. Pode causar danos irreparáveis aos seres humanos.
Representação:
A radioatividade é regida por leis que estão ligadas as emissões radioativas com a decorrente conversão de um radionuclídeo (núcleo radioativo) em outro elemento químico. Essa conversão tem por objetivo transformar um átomo instável em outro mais estável. As leis da radioatividade são:
1ª Lei da Radioatividade (lei de Soddy): "Quando um núcleo emite uma partícula alfa (), seu número atômico diminui de duas unidades e seu
número de massa diminui de quatro unidades."
ZXA 24 + Z-2YA-4
Ex: 92U235 24 + 90Th231
2ª Lei da Radioatividade (lei de Soddy-Fajans-Russel): "Quando um núcleo emite uma partícula beta (), seu número atômico aumenta de uma unidade e seu
número de massa permanece constante."
ZXA -10 + Z+1YA
Ex: 83Bi210 -10 + 84Po210
Tempo de meia-vida
Cada elemento radioativo, seja natural ou obtido artificialmente, se transmuta (se desintegra ou decai) a uma velocidade que lhe é característica. Para se acompanhar a duração (ou a “vida”) de um elemento radioativo foi preciso estabelecer uma forma de comparação. Por exemplo, quanto tempo leva para um elemento radioativo ter sua atividade reduzida à metade da atividade inicial? Esse tempo foi denominado meia-vida do elemento.

Isso significa que, para cada meia-vida que passa, a atividade vai sendo reduzida à metade da anterior, até atingir um valor insignificante, que não permite mais distinguir suas radiações das do meio ambiente. Vejamos o caso do iodo-131, utilizado em Medicina Nuclear para exames de tireóide, que possui a meia-vida de oito dias. Isso significa que, decorridos 8 dias, atividade ingerida pelo paciente será reduzida à metade. Passados mais 8 dias, cairá à metade desse valor, ou seja, ¼ da atividade inicial e assim sucessivamente. Após 80 dias (10 meias-vidas), atingirá um valor cerca de 1000 vezes menor.
No caso do carbono-14 a meia-vida é de 5.730 anos, ou seja, este é o tempo necessário para uma determinada massa de este isótopo instável decair para a metade da sua massa, transformando-se em nitrogênio-14 pela emissão de uma partícula beta. Esta medida da meia-vida é utilizada para a datação de fósseis.
Como calcular meia-vida (radioatividade)?
O cobalto-60 (27Co60), usado em hospitais, tem meia-vida de 5 anos. Calcule quantos mols de cobalto-60 restarão após 20 anos em uma amostra que inicialmente continha 10 g desse isótopo.
RESOLUÇÃO: Em 20 anos se passam 4 meias-vidas. O tempo de meia-vida é aquele em que a metade de uma amostra inicialmente dada acaba sofrendo Decaimento radioativo, restando apenas a metade da amostra. Logo:
1 mol Co ---- 59 gramas X -------------- 0,625g X = 0,010 mols
Reações nucleares
Fissão nuclear: “É a partição de um núcleo atômico pesado e instável através do bombardeamento esse núcleo com
nêutrons moderados, originando 2 núcleos médios, liberando uma elevada quantidade de energia.”
Fusão nuclear: “Corresponde à união de dois ou mais núcleos atômicos leves, originando um único
núcleo atômico, liberando uma quantidade gigantesca de energia.”
Exercícios:
1. Relacione as radiações naturais (1ª coluna) com suas respectivas características (2ª coluna).
1ª Coluna 2ª Coluna1. alfa ( ) possuem alto poder de penetração, podendo causar danos irreparáveis ao ser humano.2. beta ( ) são partículas leves com carga elétrica negativa e massa desprezível. 3. gama
( ) são radiações eletromagnéticas semelhantes aos raios X, não possuem carga elétrica nem massa.
( ) são partículas pesadas de carga elétrica positiva que, ao incidirem sobre o corpo humano, causam apenas queimaduras leves.
Resposta: A seqüência correta é: 3 - 2 - 3 - 1.

2. O processo de irradiação pode ser utilizado para aumentar o tempo de conservação dos alimentos, por meio da eliminação de microrganismos patogênicos e de insetos. A irradiação geralmente é feita com raios gama originados do cobalto-60. A cerca da radiação, julgue os itens abaixo.(1) A radiação gama é originada de uma transformação química.(2) Se um átomo de cobalto-60 emite apenas radiação gama, isso significa que ele não sofre uma transmutação.(3) Um alimento irradiado contém átomos de cobalto-60 que foram adicionados ao mesmo no processo de tratamento.(4) No processo de irradiação, o feixe de raios gama pode ser direcionado aos alimentos por meio de placas elétricas devidamente polarizadas que desviam tais raios.Resposta: E C E E
3. Ao acessar a rede Internet, procurando algum texto a respeito do tema radioatividade no "Cade?"(http://www.cade.com.br), um jovem deparou-se com a seguinte figura, representativa do poder de penetração de diferentes tipos de radiação.
Com o auxílio da figura, julgue os itens que se seguem:
(0) A radiação esquematizada em II representa o poder de penetração das partículas beta.(1) A radiação esquematizada em III representa o poder de penetração das partículas alfa.(2) As partículas alfa e beta são neutras.(3) Quando um núcleo radioativo emite uma radiação do tipo I, o numero atômico fica inalterado.Resposta: Item correto: 0 e Itens errados: 1, 2 e 3
4. Um dos isótopos do Amerício 95Am241 quando bombardeado com partículas(2He4), forma um elemento novo e dois nêutrons 0n1, como indicado pela equação:
95Am241 + 2He4 elemento novo + 20n1
Os números atômicos e de massa do novo elemento serão respectivamente:a) 95 e 245b) 96 e 244c) 96 e 243d) 97 e 243e) 97 e 245Resposta: D
5. Uma substância radiativa tem meia-vida de 8 h. Partindo de 100 g do material radiativo, que massa da substância radiativa restará após 32 h? a) 32 g.b) 6,25 g.c) 12,5 g.d) 25 g.e) 50 g.Resposta: B
6. Calcular a vida-média dos átomos de uma amostra radioativa, sabendo que, em 64 h de desintegração, 80 g dessa amostra se reduzem a 5 g?Resposta: 16h
7. A meia-vida de um isótopo radioativo é de 12 h. Após 48 h de observação, sua massa torna-se 12,5 g. Determine a massa desse isótopo no início da contagem do tempo?Resposta: 200g
8. Após 15 min de observação, a massa da amostra de um isótopo radiativo, que era de 72 mg, torna-se 9 mg. Determine a meia-vida desse isótopo.Resposta: 5 min
9. A BOMBA ATÔMICA“O núcleo de um átomo pesado, como o urânio-235 ou o plutônio-239, é bombardeado por ........... livres que causam o processo de .............. do átomo,
o que gera intensa liberação de energia e mais nêutrons, causando uma reação em cadeia.” (Galileu, janeiro de 2003, nº 138, com adaptações.)
A alternativa que melhor completa as lacunas do enunciado na reportagem se encontra em:a) prótons, fusão.b) nêutrons, fissão.c) nêutrons, fusão.d) prótons, fissão.e) elétrons, fissão.Resposta: B
Sites e bibliografias interessantes:
- http://atomico.no.sapo.pt/02.html- http://www.cnen.gov.br/ensino/apostilas/radio.pdf- http://www.nuctec.com.br/educacional/acidentes.html- Livro texto FELTRE - página 364.