Geometria Molecular e TLV
Transcript of Geometria Molecular e TLV

Geometria molecular e Teoria d Li ã d V lê ide Ligação de Valência
DanielThiele

Formas espaciais molecularesp
•Significado:•Significado:São determinadas pelos ângulos de ligação entre núcleos e pelo comprimento entre elasentre núcleos e pelo comprimento entre elas

Formas espaciais molecularesmoleculares

Modelo de Lewis• Proposto por Gilbert Newton Lewis
íRepresentação pontual das ligações químicas
R t ã d átRepresentação de átomos:
H He Cl
Representação de moléculasF FF F+ F F Ou F F

M d l d L iModelo de LewisFalha na teoria da ligação de Lewis: Descreve a ligação química como o emparelhamento de dois g ç q pelétrons, não justificando as diferenças nos comprimentos de ligação e nas energias de dissociação;ex: H-H, 74 pm, 436,4 KJ/mol;
F-F, 142 pm, 142 KJ/mol
Radicais livres não têm seu octeto completo

O modelo VSEPR O modelo VSEPR –Geometria MolecularGeometria Molecular

O modelo VSEPR•Significado:
éModelo da repulsão do par de elétrons na camada de valência
Os elétrons:•Os elétrons:Apresentam-se como elétrons não ligantes, uma
ligação simples ou uma ligação múltiplaligação simples ou uma ligação múltipla•Disposição espacial:
A melhor disposição de determinado número de A melhor disposição de determinado número de pares de elétrons, é a que minimiza as repulsões entre eles ao mesmo tempo que apresenta a maior i t isimetria

O modelo VSEPR•Geometria molecular:
É di t ib i ã d át É a distribuição dos átomos no espaço
•Arranjo molecular: É a distribuição dos pares de elétrons ao redor pdo átomo central
•Tipos de arranjos moleculares:



O modelo VSEPR•Procedimentos para determinação da geometria molecular usando o modelo VSEPR:molecular usando o modelo VSEPR:
1 D h t t d L i d lé l í 1. Desenhe a estrutura de Lewis da molécula ou íon e conte o número total de pares de elétrons ao redor do átomo centralátomo central
2. Determine o arranjo do número total pares de elétrons de tal forma que as repulsões entre eles sejam elétrons de tal forma que as repulsões entre eles sejam minimizada
3. Use a distribuição dos átomos ligados para ç g pdeterminar a geometria molecular

N áti (NO )Na prática.... (NO2-)
1. Contar o número total de elétrons de valência; no exemplo são 5+2x6+1 = 18.
2. Definir o átomo central, que é usualmente o menos eletronegativo; no exemplo é
o N.
3. Determinar o número total de elétrons dos átomos periféricos, considerando que
têm a sua camada de valência completamente preenchida; no exemplo é 2x8 =
16.
4. Calcula-se o número de elétrons não compartilhados pertencentes ao átomo
central que corresponde à diferença entre o número total de elétrons de valênciacentral, que corresponde à diferença entre o número total de elétrons de valência
presentes na molécula (1) e o número de elétrons dos átomos periféricos (3); no
exemplo 18-16 = 2, isto é tem 1 par eletrônico não ligante, ou um domínio não
ligante.
5. Usa-se o Modelo de Repulsão dos Pares Eletrônicos da Camada de Valência; no
exemplo a molécula tem geometria angular.

N áti (NO )Na prática.... (NO2-)
Associam-se equitativamente os elétrons de valência ainda não distribuídos, pelos
átomos periféricos; (18-6 = 12 elétrons pelos 2 átomos de oxigênio);
Determinam-se as cargas formais de todos os átomos presentes na molécula;
Minimiza-se a carga formal do átomo central, estabelecendo ligações duplas.

E d lE d â
Estruturas de lewisEstruturas de ressonância

Ligações múltiplasLigações múltiplas
•Ligações sigma (σ):C d id d l ô i i i Concentram a densidade eletrônica simetricamente ao
redor do eixo que une os núcleos
•Ligações pi (π):Resultam da superposição entre dois orbitais p Resultam da superposição entre dois orbitais p posicionados perpendicularmente ao eixo internuclear. São mais fracas que as ligações σ.f q g ç
•Ligações
Simples: σ Dupla: σ π Tripla: σ π π

Ligações múltiplasLigações múltiplas

Ligações múltiplasLigações múltiplas•Ligações π deslocalizadas:Ligações π deslocalizadas
Ocorrem em moléculas com ressonância
Exemplo: benzeno

Ligações múltiplasLigações múltiplas
C d C b li t t bit l 2 ã hib idi d Cada Carbono ligante tem um orbital 2p não hibridizado (perpendicular ao eixo). Estes seis orbitais superpõem-se formando um orbital π que fica espalhado deslocalizado formando um orbital π que fica espalhado, deslocalizado, ou seja, estendido por mais de dois átomos ligados.

O modelo RPENV•Procedimentos para determinação da geometria molecular usando o modelo RPENV:molecular usando o modelo RPENV:
1 D h t t d L i d lé l í 1. Desenhe a estrutura de Lewis da molécula ou íon e conte o número total de domínios de elétrons ao redor do átomo centralátomo central
2. Determine o arranjo o número total de domínios de tal forma que as repulsões entre eles seja minimizadade tal forma que as repulsões entre eles seja minimizada
3. Use a distribuição dos átomos ligados para determinar a geometria molecularg

O modelo RPENV•Procedimentos para determinação da geometria molecular usando o modelo RPENV:molecular usando o modelo RPENV:
1 D h t t d L i d lé l í 1. Desenhe a estrutura de Lewis da molécula ou íon e conte o número total de domínios de elétrons ao redor do átomo centralátomo central
2. Determine o arranjo o número total de domínios de tal forma que as repulsões entre eles seja minimizadade tal forma que as repulsões entre eles seja minimizada
3. Use a distribuição dos átomos ligados para determinar a geometria molecularg

O modelo VSEPR•Exemplo:

O modelo VSEPR•Efeitos dos elétrons não ligantes e ligações múltiplas g n g ç mú pnos ângulos de ligação:
O d lét ã Os pares de elétrons não ligantes exercem forças repulsivas maiores nos pares de repulsivas maiores nos pares de elétrons ligantes, e portanto tendem a comprimir os ângulos de p gligação

Moléculas em que o átomo central tem pares isoladosMoléculas em que o átomo central tem pares isolados
Repulsão par isolado‐ par isolado‐ par ligante‐‐par isolado ‐par ligante ‐par ligante

O modelo VSEPR•Moléculas com níveis de valência expandidos
•5 pares de elétrons:
Arranjo mais estável: Arranjo mais estável:
Bipiramidal trigonal
•6 pares de elétrons:
A j i tá lArranjo mais estável:
Octaedro

O modelo RPENV

O modelo RPENV

O modelo VSEPR•Formas espaciais de moléculas maioresm u m
Podemos utilizar o modelo VSEPR para determinar suas VSEPR para determinar suas geometrias, bastando para isso, a análise de cada átomo central individualmente

Eletronegatividadege polaridade molecular

Forma espacial molecular l id d l le polaridade molecular
•Polaridade molecular:Polaridade molecularMede a densidade eletrônica em uma eletrônica em uma molécula e é dada com base na somacom base na somavetorial dos dipolosde ligaçãode ligação

Forma espacial molecular Forma espacial molecular e polaridade moleculare polaridade molecular

Forma espacial molecular Forma espacial molecular e polaridade moleculare polaridade molecular



Teoria da Ligação de Valência (TLV)• Primeiro modelo mecânico-quântico de ligação• Conceitos de Lewis expressos em termos deCo ce tos de e s e p essos e te os de• funções de onda• Conceitos importantes, mas as técnicas computacionais utilizam
d l d OMmodelo de OM.• Interação entre orbitais de valência das espécies consideradas• Inicialmente era usada para explicar a existência de moléculasInicialmente era usada para explicar a existência de moléculas
simples• Considera que os orbitais atômicos sofram hibridização• Os orbitais híbridos formados possuem a simetria do composto;• Esse modelo mostra porque os átomos se dirigem para posições
fixas no espaçop ç• Fundamental conhecer as propriedades magnéticas dos
compostos;• Não é capaz de prever propriedades magnéticas eNão é capaz de prever propriedades magnéticas e
espectroscópicas.• Não explica radicais livres

Ligação Covalente
A ligação covalente ocorre quando 2 elétrons são compartilhados, em um orbital, por dois átomos, reduzindo‐se assim a energia total ddo sistema.
Os pares de elétrons compartilhados são chamados de elétrons de ligação. Para fins de regra do octeto, o par de elétron conta para os 2 átomos envolvidos na
Os pares de elétrons não compartilhados são chamados de elétrons não ligantes e referem‐se relacionam‐se com a configuração eletrônica de apenas um átomo.eletrônica de apenas um átomo.
Ordem de Ligação é o número de ligações que são feitas entre osOrdem de Ligação‐ é o número de ligações que são feitas entre os átomos e m análise.

Forças atrativas e repulsivas nas ligações covalentes

Formação da ligação covalente do H2.

Distribuição da densidade eletrônica para H2.

Distribuição da densidade eletrônica para H2, F2, e HF.




Formação da ligação covalente e Formação da ligação covalente e sobreposição de orbitaissobreposição de orbitais

Teoria de Ligação de ValênciaTeoria de Ligação de Valência
1 s 2 p
Formação da molécula de ácido fluorídrico+ + +
C O A L E S C Ê N C IA
H F H - F
Formação da molécula de fluor (F2)
2 p2 p
+
FF
44F -F

Orbitais híbridosOrbitais híbridos

Possíveis maneiras de formar ligações químicas a partir d bit i 2 2 d B d 1 d át ddos orbitais 2s e 2px do Be e de 1s dos átomos de hidrogênio.

Perfil energético da formação da ligação químicaPerfil energético da formação da ligação química no composto BeH2 de acordo com a TLV.

Orbitais híbridossp (Linear)

Orbitais híbridossp (Linear)

Orbitais híbridossp² (trigonal plana)

Orbitais híbridossp² (trigonal plana)

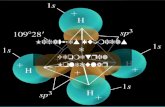
Orbitais híbridosOrbitais híbridossp³ (tetraédrica)

Orbitais híbridosOrbitais híbridossp3d (bipiramidal trigonal)

Orbitais híbridosOrbitais híbridossp3d (bipiramidal trigonal)

Orbitais híbridosOrbitais híbridossp3d (bipiramidal trigonal)

Orbitais híbridosOrbitais híbridossp3d2 (octaédrico)


Comprimento de Ligação Em geral elétrons mais próximosComprimento de Ligação‐ Em geral, elétrons mais próximos do núcleo resultam em ligações mais curtas e fortes
Multiplas ligações resultam em liações mais curtas e fortesp g ç ç

Bond length and covalent radius.
Internuclear distance(bond length)
Internuclear distance(bond length)
Covalent radius
Covalent radius
72 pm 114 pm
Internuclear distance(bond length)
Internuclear distance(bond length)
Covalent radius
Covalent radius
133 pm100 pm