Proteínas
-
Upload
estude-mais -
Category
Education
-
view
551 -
download
0
description
Transcript of Proteínas

PROF. YGOR MICHEL
DESIGN: NATAN CARDOSO


DEFINIÇÃO
São macromoléculas, de elevado peso molecular, constituídas pela união de vários aminoácidos, associados entre si através de ligações peptídicas.
Portanto, as proteínas são polímeros, onde os monômeros ( unidades constituintes ) são os aminoácidos.

AMINOÁCIDOS
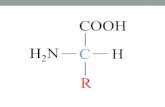
Estrutura química :
Apresentam um grupo Amina ( NH2 ) e um grupo carboxila ( grupo ácido ).
R representa um radical, sendo o fator que diferencia um aminoácido de outro.

LIGAÇÃO PEPTÍDICA
Ocorre entre o Grupo amina de um aminoácido + grupo carboxila do aminoácido seguinte
Reação de desidratação (liberação de molécula de água)

CLASSIFICAÇÃO DOS AMINOÁCIDOS
Naturais – o organismo é capaz de sintetizar
Ex: glicina, glutamina, etc.
Essenciais – o organismo não é capaz de sintetizar, mas obtido na alimentação.
Ex: lisina e isoleucina (feijão)
Leucina e valina (arroz)

FENILCETONÚRIA
Doença genética caracterizada pela deficiência de produção da enzima fenilalanina-hidroxilase, que é responsável pela conversão do aminoácido essencial fenilalanina em tirosina ( outro aminoácido).
O acúmulo do aminoácido fenilalanina no sangue e no líquor ( líquido cérebro-espinhal ou céfalorraquiano ) leva a lesões no sistema nervoso central.
O acúmulo de fenilalanina pode ser detectado pelo teste do pezinho.

PROTEÍNAS
As proteínas diferem uma das outras pela:
Ordem dos aminoácidos
Tipo dos aminoácidos
Número do aminoácidos

FUNÇÕES
Estrutural
Formar alguns hormônios
Formar anticorpos
Contração muscular
Transporte de oxigênio
(hemoglobina = proteína + ferro);
Enzimática (acelerar reações químicas)

ESTRUTURA PRIMÁRIA
É a sequência de aminoácidos em uma proteína.

ESTRUTURA SECUNDÁRIA
Surgem as pontes de hidrogênio que conferem a forma helicoidal para a “fita de aminoácidos”.

ESTRUTURA TERCIÁRIA
A hélice dobra-se nas três direções do espaço devido a atração entre as cargas elétricas dos aminoácidos que podem forma pontes bissulfeto (dois átomos de enxofre), ficando com forma enovelada.

ESTRUTURA QUATERNÁRIA
Em algumas proteínas os ‘novelos’ se associam formando o que chamamos de estrutura quaternária.

DESNATURAÇÃO DE PROTEÍNAS
Como você viu, a forma da proteína é importante para a sua função. Mas alguns fatores como calor, acidez, radiação, substâncias químicas, etc. podem romper as ligações que mantém a forma da proteína, alterando a sua estrutura secundária e terciária.
Quando a estrutura da proteína desmancha, dizemos que ocorreu a desnaturação.
Uma leve desnaturação é reversível, mas uma desnaturação acentuada é irreversível. Neste caso a proteína perde sua forma e função.

PROTEÍNAS CONJUGADAS
São proteínas que se associam a outras substâncias.
Ex. Glicoproteínas (proteínas + glicídios)
Nucleoproteínas (proteínas + ácidos nucleicos)
(encontramos nos cromossomos, ribossomos).