Proteínas
-
Upload
mariana-lopes -
Category
Health & Medicine
-
view
12.448 -
download
9
description
Transcript of Proteínas

Proteínas

PROTEÍNAS EM ALIMENTOS
As proteínas são os maiores constituintes
de toda célula viva;
Nos alimentos, além da função nutricional,
as proteínas têm propriedades
organolépticas e de textura.

PROTEÍNAS EM ALIMENTOS
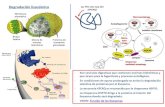
→ Apesar da complexidade estrutural, as proteínas podem ser quebradas em aminoácidos pela ação de enzimas ou fervura com ácidos e álcalis, sob certas condições.
→ Nos alimentos, tendem a decompor à temperatura ambiente, auxiliada pela ação bacteriana, podem formar produtos tóxicos para o corpo, necessitando de uma boa conservação.
→ Proteína animal X Proteína vegetal X Proteína não convêncional
→ Funções biológicas: catalisadoras, regeneradoras, imunologia, energia, reguladores, reprodução e etc.

CONCEITO, COMPOSIÇÃO E NATUREZA
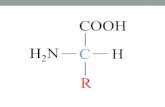
CONCEITO: Quimicamente são polímeros,
cujas unidades básicas são os aminoácidos
ligados por ligações peptídicas formando
cadeias, em várias estruturas geométricas e
combinações químicas para formar as
proteínas especificas.

CONCEITO, COMPOSIÇÃO E NATUREZA
Proteína de alto valor biológico(VB): proteína completa porque apresenta os aminoácidos em teores necessários a manutenção da vida e crescimento dos novos tecidos.
Proteína de baixo valor biológico: não tem os aminoácidos em teores adequados. Ex.: frutas e hortaliças.
Proteínas parcialmente completas: apresenta um ou mais aminoácidos limitante. EX: cereais (deficientes em lisina, triptofano e treonina) e leguminosa (deficiente em metionina).


SIMPLES
São aquelas que por hidrólise nos fornecem aminoácidos como únicos produtos.
AlbuminasAlbuminas: altamente solúvel em água : clara do ovo; leite; ervilha;
GlobulinasGlobulinas: insolúveis em água: músculos; ervilha; GlutelinasGlutelinas: somente em vegetais: trigo; arroz ProlaminasProlaminas: somente em vegetais: trigo, centeio, milho,
cevada ProtaminasProtaminas: produtos de peixes HistonasHistonas: ácidos nucléicos EscleroproteínasEscleroproteínas: queratina, colágeno

CONJUGADAS
Proteínas combinadas com substâncias não protéicas, chamada grupo prostético.
CromoproteínaCromoproteína lipoproteínalipoproteína NucleoproteínasNucleoproteínas GlicoproteínasGlicoproteínas FosfoproteínasFosfoproteínas Metaloproteínas Metaloproteínas

DERIVADAS
Não são encontradas na natureza, mas obtidas da hidrólise das simples e/ou conjugadas pela ação
de ácidos, bases ou enzimas.
Derivadas primárias: Derivadas primárias: obtidos por processos brandos de decomposição
Derivados secundáriosDerivados secundários: mistura complexa de uma moléculas de diferentes tamanhos e diferente composição de aminoácidos e diferentes propriedades.

ALGUMAS PROTEINAS IMPORTANTES EM ALIMENTOS
Proteínas da carne: Proteínas da carne: miosina; actina; colágeno; tripsina
Proteínas do leite: Proteínas do leite: caseína; lactoalbumina; lactoglobulina
Proteína do ovo: Proteína do ovo: Clara - (ovalbumina (50%); canalbumina; glicoproteina;
avidina/biotina).Gema - (lipovitelina, fosfovitina, livitina)
Proteínas do trigo:Proteínas do trigo: prolamina (gliadina); glutelina (glutenina).

REAÇÕES QUÍMICAS
Hidrólise
Desnaturação

PROTEÍNAS IMPORTANTES
a)Proteínas da carne:Proteínas da carne: miosina; actina; colágeno; tripsina.
b)Proteínas do leite:Proteínas do leite: caseína; lactoalbumina; lactoglobulina.
c) Proteína do ovo: Proteína do ovo: clara (ovalbumina (50%);
canalbumina; glicoproteina; avidina/biotina). gema (lipovitelina, fosfovitina,
livitina)
d)Proteínas do trigoProteínas do trigo: prolamina (gliadina); glutelina (glutenina). Formam com água uma substância elástica e aderente insolúvel em água.

PROTEÍNAS
Proteases

Introdução
São enzimas comumente utilizadas na indústria alimentícia.
A ação das proteases sobre as proteínas, antes do consumo, favorece a digestão e absorção das proteínas pelo organismo.

Grupo Hidrolases
Peptidases ou ProteinasesPeptidases ou Proteinases
Catalisam a reação de hidrólise das ligações peptídicas das proteínas.
Hidrólise de proteínas = Digestão, ativação de enzimas, coagulação do sangue e no transporte de proteínas através de membranas.
A posição da ligação na cadeia polipeptídica e o tamanho da cadeia
podem influenciar a atividade das proteases.

Características gerais
São classificadas basicamente de acordo com dois critérios:
Modo de ação
Natureza química do sei sítio catalítico.

Modo de ação das proteases
Exopeptidases
Atuam nas extremidades da cadeia polipeptídica.
Endopeptidases (ou proteinases)
Agem nas ligações no interior da cadeia protéica.

Exopeptidases
AMINOPEPTIDASESProteases que agem na extremidade N-
terminal da cadeia polipeptídica; liberam aminoácidos livres, dipeptídicos ou tripeptídicos.
CARBOXIPEPTIDASESProteases que agem na extremidade C-terminal
da cadeia polipeptídica; liberam aminoácidos livres dipeptídios .


Endopeptidases
Serina-proteases
São caracterizadas pela presença do aminoácido serina no sítio ativo.
O principal grupo desse tipo de proteases é formado pelas serina-proteases alcalinas, como tripsina, quimotripsina e subtilisina, que apresentam baixa especificidade de
substrato.

Endopeptidases
Cisteína-proteases sulfidrílicas
Apresentam em seu sítio ativo cisteína conjugada com histidina.
São normalmente, mais ativas em meios de pH neutro, podendo apresentar atividade em valores de pH ácidos.

Endopeptidases
Proteases aspárticas ou ácidas
Contém ácido aspártico em seu sítio ativo.
Apresentam maior atividade em valores de pH ácido e têm maior afinidade por ligações que envolvem aminoácidos apolares e aromáticos.
Principais proteases ácidas: Pepsina e renina e aquelas produzidas pelos fungos Aspergillus, Penicillium, Rhizopus, Neurospora, Endothia e Rhizomucor.

Endopeptidases
Metalo-proteases
São enzimas que dependem de íons metálicos divalentes para sua atividade.
Entre as neutras encontra-se por exemplo as colagenases de Clostridium hystoliticum e elastases de Pseudomonas aeruginosa.

Classe de proteases
CLASSE EXEMPLO AA DO SÍTIO ATIVO
Serina-protease QuimotripsinaSubtilisina
HistidinaÁc. aspárticoSerina
Cisteína-protease
Papaína CisteinaHistidinaÁc. aspártico
Protease aspártica
Pepsina de Penicillium sp.
Ác. aspártico
Metalo-protease Carboxipeptidase A bovina
ZincoGlutaminaTriptofano

Proteases vegetais
Estão entre as proteases mais empregadas na indústria de alimentos.
A atividade destas é maior nos vegetais verdes.
A papaína, a bromelina e a ficina estão entre as mais importantes cisteina-proteases.

Proteases vegetais
Papaína
Extraída do latex dos frutos do mamoeiro
QP-A: PapaínaQP-B: Quimopapaína
Ambas possuem características bastante semelhantes e que variam de acordo com o clima e manejo durante a extração e concentração do extrato.

Proteases vegetais
Bromelina
Extraída do pedúnculo ou do fruto do abacaxizeiro.
Perde sua atividade rapidamente em temperaturas superiores a 70°C.

Proteases vegetais
Ficina
Extraída do latex de diversas espécies do gênero Ficus.
Hidrolisa ligações que envolvem diversos aminoácidos.

Proteases animais
São as mais estudadas e importantes comercialmente devido à sua importância da área da saúde.
- As mais importantes são as proteases gástricas (renina e pepsina) e as pancreáticas (tripsina e quimotripsina).

Proteases animais
Renina ou quimosina
Protease aspártica extraída do quarto estômago de bezzerros não desmamados.
É extraída na forma inativa, e convertida por hidrólise parcial que liera um peptídio de sua
cadeia protéica.

Proteases animais
Pepsina
Protease aspártica produzida pela mucosa do estômago na forma inativa de pepsinogênio.
Também extraída na forma inativa, tirna-se ativa por autólise.
Sua atividade é influenciada pelo substrato, prefere ligações peptídicas que envolvam aminoácidos hidrofóbicos.

Proteases animais
Tripsina
Serina protease secretada pelo pâncreas, é uma das enzimas digestivas mais importantes.
Sintetizada de forma inativa de tripsinogênio no pâncreas de animais superiores e é ativada por hidróliseno duodeno.
Inibidores de tripsina são peptídios produzidos pelo pâncreas, mas estão também presentes na soja e trigo; o que impede a digestão de proteínas presentes nestes.

Proteases animais
Quimotripsina
Serina-protease semelhante à tripsina e também é sintetizada como zimogênio pelo pâncreas.
Hidrolisa preferencialmente ligações que envolvem aminoácidos aromáticos (tirosina,
fenilalanina e triptofano), mas pode hidrolisar também ligações ente todos os aminoácidos
hidrofóbicos.

Proteases animais
Catepsinas e calpaínas
Cisteína-proteases intracelulares relacionadas à resolução do rigor mortis.
Estão envolvidas com a bioquímica da carne.

Proteases microbianas
De origem bacteriana
Maior parte produzidas pelas bactérias dos gêneros Bacillus e Geobacillus.
Embora tenham preferência por ligações entre aminoácidos hidrofóbicos, o grau de hidrólise pode ser controlado por alterações no pH e
na temperatura da reação protelítica.

Proteases microbianas
De origem fúngica
Uma única espécie de fungo pode produzir diferentes proteases ( alcalinas, neutras e ácidas).
Aspergillus oryzae produz três proteases extracelulares,o extrato é obtido por
fermentação.

Aplicação Industrial
Clarificação de cerveja
As proteases hidrolisam os peptídeos e impedem que eles se insolubilizem, evitando a turvação (papaína).
A presença de proteínas é vital para a formação da espuma.

Aplicação Industrial
Amaciamento da carne
Processo normal: 10 dias a 4 semanas.Processo acelerado: Proteases que hidrolisam
as proteínas da carne (papaína)
Evita hidrólise durante o armazenamento a frio, e alta estabilidade térmica, o que
garante o amaciamento durante o cozimento.

Aplicação Industrial
Método clássico para amaciamento da carne:Método clássico para amaciamento da carne:Aplicação superficial da enzima em véiculo de sal.
Método de imersão para amaciamento da carne:Método de imersão para amaciamento da carne:Os cortes da carne são submersos na solução de enzima.
Método de injeção para amaciamento da carne:Método de injeção para amaciamento da carne:Uso de seringas ou pistolas para aplicação de solução
enzimática.
Método de injeção no animal vivo para amaciamento da carne:Método de injeção no animal vivo para amaciamento da carne:Injeção feita na jugular do animal, 10 a 30 min antes do abate.
-enzima purificada e inativada.

Aplicação Industrial
Coagulação do leite
A produção do leite de queijos baseia-se na separação de caseínas e gordura do leite da fração que constitui o soro.
O soro é formado em maior parte por água, lactose, sais e outras proteínas não caseínas.

Aplicação Industrial
Coagulação do leite
Caseína – Mistura de fosfoproteínas muito semelhantes:
α s1- / α s2- / β - / κ- caseína

Micela caseína

Cadeia peptídica
Região hidrofóbica
Fosfato de cálcio
Superfície rica em К - caseína

Aplicação Industrial
Coagulação do leite
Precipitação isoelétricaPrecipitação isoelétrica
Ao atingir pH 4,6 alcança o ponto isoelétrico da caseína bruta do leite, ocorre a
insolubilização dessas proteínas, que precipitam.

Aplicação industrial
Coagulação do leite
Proteólise limitadaProteólise limitada1.κ – caseína sofre hidrólise
2. Íons de cálcio do leite ligam-se às frações fosfatadas da caseína
3.Formam-se ligações cruzadas e precipitação em forma de coágulos.
4.Se a hidrólise não for limitada haverá destruição do coágulo e solubilização de pequenos peptídios, o que
afetará na textura e rendimento do queijo.5.A hidrólise excessiva pode ocasionar a liberação de peptídeos que contêm aa hidrofóbicos na extremidade
c-terminal. Estes apresentam sabor amargo.

Aplicação industrial
Enzimas utilizadas na coagulação do leite:
Renina ou quimosina
Proteases ácidas de Rhizomucor miehei; Rhizomucor pusillus, Aspergillus oryzae e
Endothia parasitica.

Aplicação industrial
Maturação acelerada de queijos
A proteólise é um dos mais importantes processos de maturação de queijos, pois
peptídeos e aminoácidos livres, gerados pela ação de proteases, são precursores de sabor, além de serem fontes de nitrogênio para a
microbiota secundária.

Aplicação industrial
Panificação
A fração protéica do trigo, chamada glúten, dá à farinha a propriedade de formar uma massa viscoelástica capaz de reter ar.
Sem ar, a massa não reage com o fermento químico que resultará em um pão duro.

Aplicação industrial
Panificação Proteases podem ser aplicadas no controle da
força do glúten, garantindo menor tempo de trabalho da massa na produção de pães (enzimas fúngicas) e redução de teor de
glúten para a produção de bolos e biscoitos (enzimas vegetais e/ou bactéiras).

Aplicação industrial
Modificação de proteínas
HidróliseHidrólise
Hidrolisados protéicos são obtidos pela ação de proteases específicas sobre diversas fontes protéicas com a finalidade de gerar compostos com diferentes funcionalidades: Aromatizantes, espumantes e emulsificantes.

Aplicação industrial
Modificação de proteínas
Síntese
A síntese de proteínas pode ser realizada de três formas destintas: Síntese química, síntese enzimática e síntese via DNA recombinante.
- Plasteína é o nome dado a moléculas semelhantes às proteínas naturais, cuja origem é a síntese catalisada
por protease.

Aplicação industrial
Modificação de proteínas
A reação de síntese pode ser usada na incorporação de aa essenciais a proteínas de baixo valor nutricional, na remoção de sabor amargo de peptídeos com a hidrofóbico c-terminal e na modificação de proteínas com o objetivo de melhorar propriedades funcionais.

Aplicação industrial
Modificação de proteínas
Reestruturação
Importante no desenvolvimento de produtos cárneos e derivados reestruturados, promovendo a melhora tecnológica na textura, aparência, aroma e sabor.
- A Transaminase é uma enzima que atua na síntese de ligações cruzadas entre proteínas, mas não é uma protease.
Streptoverticillium mobataenseStreptoverticillium mobataense

Modificação de proteínas
Síntese de aspartame
Síntese de aspartame – edulcorante não-calórico formado pelo ácido L-aspártico e pela L-fenilalanina. Esta síntese garante a formação do sabor doce.
Bacillus thermoproteolyticus