QUI 163 Química do Meio Ambiente§ão... · Em um local distante da fonte dos poluentes primários...
Transcript of QUI 163 Química do Meio Ambiente§ão... · Em um local distante da fonte dos poluentes primários...

Aula 6 – Poluição Atmosférica Parte I
Prof. Julio C. J. Silva
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas
Depto. de Química
Juiz de Fora, 2019
QUI 163 – Química do Meio Ambiente

Introdução • Poluentes partículas maiores concentram-
se próximo ao solo (gravidade).
• No caso de gases maior complexidade
• Material particulado diminui a penetração da luz afetando o clima por meios físicos
• Gases: afetam o clima por reações químicas

Atmosfera Dispersão atmosférica de contaminantes
– O termo dispersão atmosférica é usado para referir-se ao espalhamento de poluentes gasosos devido aos efeitos convectivos e turbulentos do escoamento atmosférico.
– A dispersão é resultado de mecanismos de transporte rápidos e irregulares.
– Os contaminantes quando introduzidos no ar, são transportados pelo vento e simultaneamente se misturam na atmosfera turbulenta.
– Durante a dispersão, os contaminantes podem sofrer reações químicas que os transformam de contaminantes primários (procedentes diretamente das fontes de emissão) em contaminantes secundários (originados por reações químicas entre os contaminantes primários e os componentes normais presentes na atmosfera) ou podem ser depositados no solo por via seca ou úmida. Os contaminantes do ar podem ser removidos da atmosfera por três mecanismos a saber:

Dispersão atmosférica de contaminantes
• Deposição úmida
• Deposição seca
• Reação química de partículas ou gases

Principais Fontes de Poluição
• Origem natural vulcões, marinhas, pólen, queimadas, microorganismos (últimas: acentuadas pela ação humana)
• Origem antropogênica processos industriais diversos (químicos, de combustão, refinamento...) nucleares ou atômicos, atividades agrárias e minerárias, etc.

Combustão • Processos de combustão São as grandes fontes de
energia e emissão de compostos para atmosfera
• Centros urbanos: – Maior consumo de energia – Países ricos – Alta tecnologia combustão (forma antiga de fornecer
energia)
• Aumento dos processos de combustão: – Alteração da composição da atmosfera Receptor – Química atmosférica previsão – Energia Produção, conservação e minimização do uso – Resíduos lixo nuclear

Combustão

Combustão
partículas maiores concentram-se próximo ao solo
partículas maiores concentram-se próximo ao solo
partículas maiores concentram-se próximo ao solo

Combustão

Combustão

Lixo Nuclear

Combustão
• Processos de combustão:
• Combustível + ar (N2+O2) gases (NO + SO2 + CO2) + MPTS
– MPTS
– Gases depende do material (C, H, O, S)
– NOx Independe do material
Fumaça (visíveis)
PM10, PM2,5 (invisíveis)

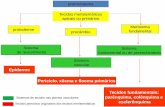
Poluentes Primários • Material Particulado partículas e líquidos emitidos para a
atmosfera por fontes diversas (fábricas, plantas, veículos, construções, etc.). Inclui fumaças, cinzas, poeiras, pólen, esporos... Reduz a visibilidade e as menores se alojam nos pulmões e outros tecidos
• Dióxido Sulfúrico (SO2) gás incolor e corrosivo originário de processos de combustão. No ar: SO3 que, em contato com a água H2SO4 (ácido sulfúrico)
• Óxido nitroso (N2O) Emitido por fontes naturais (bactérias) e pela reação entre N2 e O3. Gás de efeito estufa
• Óxido nítrico (NO) Emitido por fontes naturais (microorganismos) e pela combustão. Na atmosfera é oxidado a NO2 pelo O3 e O2.
• Óxido de Nitrogênio (NO2) gás avermelhado, odor irritante, reduz a visibilidade. Formado quando há oxidação de componentes nitrosos (NO e NO2); altas concentrações: problemas no coração e pulmões. Em presença de umidade: HNO3 (ácido nítrico)

Poluentes Primários
• Monóxido de Carbono (CO) gás incolor, inodoro e altamente venenoso causa enjôos, reflexos retardados e compromete o transporte de oxigênio pelo sangue, podendo levar à morte.
• Intoxicação – Minha namorada morreu por causa de uma churrasqueira - BBC.com
– Intoxicação por inalação de monóxido de carbono mata família em Sabrosa
– Último Segundo - iG @ https://ultimosegundo.ig.com.br/mundo/2018-02-19/casal-morre-carro-sexo.html
“Um casal morreu sufocado enquanto fazia sexo, dentro de um carro na cidade de Bottrop, na Alemanha. De acordo com o portal Metro , os corpos do homem,
de 39 anos, e da mulher, de 44, foram encontrados, nus, na última terça-feira (13), em um veículo estacionado em uma garagem no oeste do país europeu”

Poluentes Secundários
• Produzidos na atmosfera quando ocorrem certas reações químicas poluentes primários em contato com a luz solar geram centenas de componentes químicos danosos reações fotoquímicas – Ozônio (O3) na troposfera é altamente danoso. Formado a
partir de hidrocarbonetos inexistentes na estratosfera (assim como o átomo O inexiste na troposfera).
– Piores episódios de concentração de O3 verão e de dia (luz). Causa irritação nos olhos, pulmões e câncer. Compromete o crescimento de culturas agrícolas, danifica materiais (borracha, pintura, plástico), ...
– Ácidos diversos: comprometem a saúde e causam corrosões em diversos materiais
• HNO3 (ácido nítrico)
• H2SO4 (ácido sulfúrico), ...

Formação dos NOx
• NOx (NO + NO2) Presentes em locais onde ocorreu combustão
• Reação: N2 (78%) + O2 (21%) → 2NO
• Exercício
• A) Demonstre matematicamente que a quantidade NO formado a partir de N2 e O2 é insignificante.
• Dados: • Go NO = 86,7 kJ, 25oC
• R = 8,314 JK-1
• Resposta 3,2 x 10 kPa
• B) Se um combustível queima no ar, algum NO é formado. Calcule a concentração de NO em equilíbrio (ao nível do mar) a uma temperatura de 1.727 oC. • Resposta 0,223 kPa

Reações fotoquímicas
• Reações químicas energia térmica
• Reações fotoquímicas Radiação (E = h.)
NO2 + h. NO + O
NOx e a formação de poluentes secundários
NO + O3 → NO2 + O2
NO + RO2* → NO2 + RO* (alcoxila)
NO2 + h ( 430 nm) → NO + O
O + O2 → O3
(Estado fotoestacionário)
O3 = 40 ppb (sem poluição)
O3 = 500 ppb (com poluição)




Exercício • Porque um gás como o CO2 tem sua emissão controlada por
acordos internacionais, ao passo que o gás NO2 depende da legislação de cada país emissor?

Smog Fotoquímico

Smog fotoquímico (smoke + fog)
• Smog fotoquímico é a poluição do ar, sobretudo em áreas urbanas, por ozônio e outros compostos originados por reações fotoquímicas, reações químicas causadas pela luz solar. O efeito visível disto é uma camada roxa acinzentada na atmosfera.
• Descobiu-se esse tipo de smog pela primeira vez em Los Angeles, na década de 1940, e costuma-se acontecer em cidades com uma grande movimentação de veículos, que causam grande acumulação de óxido nítrico (NO) e compostos orgânicos voláteis (COVs).
• A mistura de poluentes no ar, no Smog fotoquímico, pode conter:
• Óxidos de nitrogênio, como o dióxido de nitrogênio
• Ozônio troposférico
• Compostos orgânicos voláteis (VOCs)
• Nitrato de peroxilacetila (PAN)
• Aldeídos

Smog fotoquímico
• Condições Muito sol e pouco vento
• Efeitos desconforto visual (oxidantes, aldeídos, PAN)
• Período inverno
– Período crítico para dispersão de poluentes
– Pouco vento
– Dias claros com poucas nuvens (insolação)
• O smog fotoquímico é resultado da quebra do estado fotoestacionário

• Reações:
– NO2 + h → NO + O
– O + O2 → O3
– NO + O3 → NO2 + O2
• Acumulo de O3 e NO2:
– NO + RO2. → NO2 + RO.
• Formação de peróxidos:
– Compostos orgânicos voláteis (COV) emitidos por organismos vivos e atividades humanas
– Peróxidos COV(hidrocarbonetos, aldeídos, cetonas) + Oxidante (O2, HO., PAN, H2O2, O, etc.)

Smog fotoquímico

Inversão Térmica

Chuva Ácida
Um dos problemas ambientais mais graves que muitas regiões do mundo vêm enfrentando atualmente é a chuva ácida.
O fenômeno da chuva ácida foi descoberto por Argus Smith, na Grã-Bretanha, em meados de 1800, mas permaneceu esquecido até os anos 50. Ele refere-se à precipitação mais ácida que a chuva natural ligeiramente ácida devido à presença de dióxido de carbono atmosférico dissolvido, que forma ácido carbônico:
CO2(g) + H2O(aq) H2CO3(aq)
Em seguida, o H2CO3 se ioniza parcialmente liberando íon hidrogênio com a resultante redução no pH do sistema:
H2CO3(aq) H+ + HCO3-

Chuva Ácida
Devido a essa fonte de acidez, o pH da chuva “natural”, não poluída, é de cerca de 5,6 Apenas a chuva que é apreciavelmente mais ácida que isso, com pH menor que 5 é considerada chuva “ácida”.
Tendo em vista a presença de quantidades de traço de ácidos fortes naturais
O que leva a acidez da chuva em ar puro a um nível um pouco mais alto que aqueles existentes pela presença apenas de dióxido de carbono
Ácidos fortes, como o HCl, liberados por erupções vulcânicas podem produzir temporariamente chuva ácida “natural” em regiões como o Alasca e
a Nova Zelândia

Chuva Ácida
Os dois ácidos predominantes na chuva ácida são os ácidos sulfúrico, H2SO4, e o ácido nítrico, HNO3. Em termos gerais, a chuva ácida precipita-se segundo a direção do vento
Em um local distante da fonte dos poluentes primários (SO2 e NOx)
Os ácidos são gerados durante o transporte da massa de ar que contém os poluentes.
A chuva ácida é um problema de poluição que não respeita nem estados nem fronteiras nacionais em razão do deslocamento de longa distância
que sofrem com frequência os poluentes atmosféricos

Chuva Ácida • Reações do nitrogênio
– Dia:
• NO2 + HO. → HNO3
– Noite:
• NO2 + O3 → NO3. + O2
• NO2 + NO3. → N2O5
• N2O5 + H2O → 2HNO3
• Reações do enxofre
• SO2 + HO. → HSO3
• HSO3 + O2 → HO2 + SO3
• SO3 + H2O → H2SO4
• Reações do enxofre (aquoso)
• SO2(g) + H2O(aq) → H2SO3(aq)
• 2H2SO3 + O2 → 2H2SO4(aq) (Catalizador: MPTS –
Fe(III), Mn(II))

Chuva Ácida

Efeitos da Chuva Ácida
Nas Florestas
Tem sido percebido pelos cientistas ao longo dos anos, que em muitas
florestas as árvores não crescem como deveriam e as folhas, em vez de estarem verdes e normais, ficam castanhas e acabam caindo
Os investigadores acreditam que o principal fator responsável pelos danos causados às plantas e a morte de muitas florestas é a chuva ácida
A chuva ácida não é responsável direta da morte das árvores O que ocorre geralmente é que a árvore enfraquece e as suas folhas
morrem, limitando assim os nutrientes de que precisa ou envenenando o solo com substâncias tóxicas
De acordo com os cientistas, a água acidificada dissolve os nutrientes que estão no solo e arrasta-os rapidamente antes que as plantas os possam utilizar para crescer

Efeitos da Chuva Ácida
A chuva ácida pode causar ainda a liberação de algumas substâncias tóxicas como o alumínio no solo, prejudicando sua fertilidade As proteções das folhas são destruídas quando são banhadas por nuvens ácidas, e suas folhas acabam ficando danificadas e com manchas castanhas Uma vez que as árvores estejam enfraquecidas serão mais
facilmente atacadas por doenças e insetos

Efeito da precipitação ácida sobre uma floresta (Alemanha, 1970 - 1983)
Efeitos da Chuva Ácida

Efeitos da Chuva Ácida
Nas Águas A maioria dos rios e lagos possuem um pH entre 6 e 8 O pH dos lagos no entanto pode atingir valores aproximados a 5 quando
os solos e a água não têm a capacidade de neutralizar a chuva ácida
Todos os organismos que vivem em meios aquáticos poderão morrer por consequência deste fenômeno
Os sapos suportam as variações de pH maiores e poderiam resistir, mas se o seu alimento também desaparecer acabarão morrendo.
À medida que a acidez dos lagos aumenta os peixes vão desaparecendo
Mesmo que alguns mais resistentes consigam sobreviver, é muito
difícil que a sua continuidade esteja assegurada uma vez que os seus ovos não têm hipóteses de eclodir

Efeitos da Chuva Ácida
Diagrama mostrando a tolerância à acidez de algumas espécies

Em construções
Efeitos da Chuva Ácida
A chuva ácida pode ser responsável pela corrosão de pedra, metal ou tinta
Praticamente todos os materiais se degradam gradualmente quando expostos à chuva e ao vento
A chuva ácida acelera esse processo, destruindo estátuas, prédios ou monumentos
O principal constituinte dos mármores, os quais são utilizados na construção de prédios e monumentos, é o calcário (Carbonato de cálcio) reage com os
ácidos contribuintes da acidez da chuva ácida como na reação a seguir:

Efeito da precipitação ácida numa estátua em calcário
Efeitos da Chuva Ácida

Chuva Ácida (Efeitos Globais)

Referências • Google
• Wikipedia
• Rocha, J. C; Rosa, A. H. e Cardoso, A. A, Introdução à Química Ambiental, Porto Alegre Bookman, 2004.
• Baird, C. Química Ambiental; Tradução Maria Angeles Lobo Recio e Liz Carlos M. Carrera, 2 ed, Porto Alegre, Bookman, 2002.
• Maioli, O.L.G., Nascimento, G.N. Composição da Atmosfera, Ciclos Globais e
Tempo de Vida. Notas de aula. UFES
• Maioli, O.L.G., Nascimento, G.N. Composição da Atmosfera, Ciclos Globais e
Tempo de Vida. Monografia. UFES
• Mozeto, A. Química Atmosférica: A química sobre nossas cabeças. Cadernos
Temáticos de Química Nova na Escola. 2001
• Freire, P.S.R. A Atmosfera e sua Dinâmica – O Tempo e o Clima. Notas de Aula.
• Atmosferas Planetárias. Observatório Nacional (google)
• Nunes, L.H. lima e Poluição Atmosférica. Notas de Aula. 2002
• Damineli, A. Habitabilidade. Notas de Aula. IAGUSP
• Tolentino, M., Filho, R.C. . A Química no efeito estufa. Cadernos Temáticos de Química Nova na Escola. 1998.
• Andrade, M.F. poluição atmosférica. Artigo