Química Orgânica Experimental I‡ÕES ANOS... · A cristalização é o processo (natural ou...
Transcript of Química Orgânica Experimental I‡ÕES ANOS... · A cristalização é o processo (natural ou...

Aline Varella Rodrigues
Mônica Sumie Okuda
Raquel Mariano de Almeida
Unesp – Araraquara – Instituto de Química
Química OrgânicaExperimental I

Extração da Cafeína do Chá

Fórmula C8H10N4O2 (1,3,7-trimetilxantina)alcalóide do grupo das xantinas
Plantas que contêm o princípio ativo da Cafeína: chá mate, café, cacau, guaraná e cola
Usado em bebidas como estimulanteApresenta-se sob a forma de um pó branco ou
pequenas agulhasÉ extremamente solúvel em água quente, não
tem cheiro e apresenta sabor amargoAtua sobre o sistema nervoso central, sobre o
metabolismo basal e aumenta a produção de suco gástrico
Cafeína

FunçãoTóxico CarcinogênicoHistória do processo de
descafeinação
DiclorometanoCH2Cl2

História do processo de descafeinação
Descafeinação feita com CH2Cl2 até 1980
Acetato de etila substituiu o CH2Cl2 até o começo dos anos 90
A partir de 1990 o fluido supercrítico CO2 é usado para dissolver cafeína
Sob alta pressão o CO2 supercrítico lava os grãos de café e dissolve cerca de 99% da cafeína presente
Cafeína retirada: vendida para a indústria farmacêutica

Substâncias presentes na folhado chá
Celulose
Clorofila
Taninos
Flavonóides glicosilados

Celulose
O O
O
O H
O H
O H
O HO H
O H
O H
O H
HH
H
H
H
H
H
H
H
H

Clorofila
N
N
Mg
N
N
O
OO
CH2
CH3
O
CH3
O
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3CH3
HH

Taninos
Taninos são grupos de compostos químicos polifenólicos, de alto peso molecular, de
origem vegetal, não nitrogenadas

Flavonóides glicosilados
OO O
O
OHOH
OH
OH
OH
OH
OHOH

EfusãoBanho de resfriamento Extração com porções de diclorometano (CH2Cl2)EmulsãoLavagemSecagem pela adição de Na2SO4DecantaçãoEvaporação em banho-mariaCristalizaçãoSublimação
Processos envolvidos

Efusão
Extração descontínua Extração líquido-líquido contínua

Extração sólido-líquido é chamada de efusão
Componentes que estavam na fase sólidapassam para a fase líquida (água)
Extração descontínua: quando a solubilidade emágua dos componentes sólidos é grande
Extração contínua: quando a solubilidade dos solutos em água é pequena

Banho de resfriamentoEquilíbrio heterogêneo entre o solvente puro, sólido e a solução com soluto, na fração molar xB:
u*A(s) = u*
A(l) +RTlnxA
Temperatura de congelação normal do solvente passa de T* para T*c na solução.
k´=(RT*2 )/∆Hfusão
∆T = k´xB

Emulsão
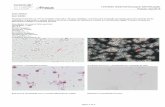
A.. Dois líquidos imiscíveis separados em duas fases (I e II). B. Emulsão da fase II dispersa na fase I. C. A emulsão instável progressivamente retorna ao seu estado inicial de fases separadas. D. O surfactante se posiciona na interface entre as fases I e II, estabilizando a emulsão

Emulsão é a mistura entre dois líquidos imiscíveis em que um deles (a fase dispersa) encontra-se na forma de finos glóbulos no seio do outro líquido (a fase contínua).
Eliminação da emulsão:
Agitação da solução c/ bagueta
Utilização de NaCl
Emulsão

Lavagem

Após a remoção do líquido sobrenadante, o precipitado deve ser lavado, pois uma pequena quantidade da solução será retida e poderá causar problemas nas etapas subseqüentes da análise. Normalmente, usa-se água destilada como água de lavagem, mas muitas vezes deve-se usar uma solução diluída do próprio reagente usado na precipitação.
A lavagem é realizada mediante a adição do líquido de lavagem sobre o precipitado. A seguir, agita-se para dispersar o sólido, centrifuga-se e decanta-se líquido. O volume do líquido de lavagem vai depender da quantidade do sólido.
Geralmente, faz-se duas ou três lavagens com 0,5 mL do líquido.
Lavagem

Secagem
Na2SO4 como agente secante

Utiliza-se um secante inorgânico
Considerações sobre o secante:
não combinar quimicamente com o composto orgânico
secagem rápida e efetiva
não dissolver apreciavelmente no líquido
econômico
não ter efeito catalizador. Não promover, por exemplo, polimerização, reações de condensação e auto-oxidação
Na2SO4 como agente secante
Secagem

Sulfato de sódio anidro:
Agente secante neutro
Barato
Grande capacidade de absorção da água (abaixo de 32,4oC)
Ineficiente para solventes como benzeno e tolueno, cuja solubilidade emágua é pequena (neste caso, usar sulfato de cobre anidro)
Não usado acima de 32,4oC, temperatura de decomposição do decahidrato
Na2SO4 + 10H2O Na2SO4.10H2O
Na2SO4

Decantação
Processo utilizado para separar misturas heterogêneas dos tipos líquido-sólido e líquido-líquido. Ex: água barrenta.

Se a água é o solvente e a substância não é volátil: evaporação simples sobreum banho de vapor ou de água
Se a evaporação deve ser rápida ou se o solvente for orgânico:
(A): balão contendo a solução a concentrar éaquecido em banho-maria e sofre rotação durante todo o processo de evaporação, o que assegura
uma boa homogeinização e evita ebulição tumultuosa
(T): torneira que permite a entrada de ar ou o abastecimento do balão com novas porções da solução
Seu funcionamento se baseia no princípio da destilação à pressão reduzida
(M): motor que permite que o balão (A) gire a uma velocidade controlada
Evaporação

A cristalização é o processo (natural ou artificial) da formação de cristais sólidos de uma solução uniforme.
Ela consiste de dois principais eventos, a nucleação e o crescimento dos cristais.
A nucleação é a etapa em que as moléculas do soluto dispersas no solvente começam a se juntar em clusters, em escala nanométrica.
O crescimento do cristal é o subseqüente crescimento do núcleo que atingiu o tamanho crítico do cluster. A nucleação e o crescimento continuam a ocorrer simultaneamente enquanto a supersaturação existir.
Cristalização

Sublimação

Substância passa do estado sólido diretamente para o estadogasoso
Exemplo: gelo seco (sublima a -78oC)
No laboratório é utilizada como método de purificação dos compostos orgânicos que sublimam. É um ótimo método de purificação
Finalidades preparativas: pressão atmosférica sobre o composto é reduzida com uma bomba ou uma trompa de vácuo. Resultado: a pressão de vapor do sólido é igualada àpressão atmosférica à temperaturas menores
Sublimação

S
V
W
T
TW: curva de equilíbrio líquido-vapor
TS: curva de equilíbrio sólido-vapor
T: ponto tríplice (coexistência de sólido, líquido e vapor)
TV: curva de equilíbrio sólido-líquido

Cânfora
Iodo sólido, à pressão normal
Naftalina, à pressão normal
Gelo seco (CO2)

Fluxograma

100mL H2O destilada (57-59ºC)+ 3 saquinhos de chá preto
(béquer B1)
-colocar os saquinhos imersos na água quente por 1 minuto
-pressionar os saquinhos entre dois vidros de relógio
-recolher o excesso no béquer B1
-descartar os saquinhos
-resfriar a solução em banho de gelo atéatingir temperatura ambiente
-colocar a solução em um funil de separação

-adicionar 20 mL de CH2Cl2 à solução
-agitar cuidadosamente para evitar a formação de emulsão
-separar fases
-repetir este processo mais duas vezes
FASE ORGÂNICA (Inferior)
CH2Cl2, cafeína, taninos e flavonóides glicosilados
P.Q.: H2O e clorofila
FASE AQUOSA (Superior)
Clorofila
P.Q.: CH2Cl2, cafeína, taninos e flavonóides glicosilados
-recolher em béquer B2 as três
extrações
-transferir para funil de separação
-lavar com 20 mL de NaOH 6M (fria)

FASE ORGÂNICA (Inferior)
CH2Cl2, cafeína, clorofila
P.Q.: sais de taninos e de flavonóides, H2O e açúcares
FASE AQUOSA (Superior)
Sais de taninos e de flavonóides, clorofila e açúcares
P.Q.: CH2Cl2 e cafeína
-descartar adequadamente
-recolher no béquer B3
-transferir para funil de separação
Descartado
-resultados da fase aquosa após as duas extrações subseqüentes
-recolher a fase orgânica no béquer B2

-lavar com 20 mL de NaOH 6M (fria)
-recolher fase inferior no béquer B3
-descartar a fase superior adequadamente
-transferir para funil de separação
-lavar com 20 mL de água fria
FASE ORGÂNICA (Inferior)
CH2Cl2 e cafeína
P.Q.: água e clorofila
FASE AQUOSA (Superior)
Sais de taninos e de flavonóides, clorofila, açúcares e Na+OH-
P.Q.: CH2Cl2 e cafeína
-transferir para erlenmeyer
-adicionar Na2SO4
-agitar e deixar em repouso
-filtrar
-descartar adequadamente
Descartado

SOBRENADANTE
CH2Cl2 e cafeína
P.Q.: clorofila
PRECIPITADO
Na2SO4 hidratado
P.Q.: clorofila, CH2CL2, cafeína
-descartar adequadamente
Descartado-transferir para béquer B4
-evaporar o solvente em banho de água até cerca de 3 mL
-transferir para um vidro de relógio
-evaporar completamente atéobtenção de cristais

SÓLIDO
Cristais de cafeína
P.Q.: clorofila
RESÍDUO
CH2Cl2 evaporado
(p.e. = 39,75°C)
-determinar a massa da cafeína impura e ponto de fusão
-purificar por sublimação
SUBLIMADO
Cristais de Cafeína
purificados
RESÍDUO
Clorofila

-determinar a massa de cafeína purificada
-determinar ponto de fusão
-calcular o rendimento
Cálculos
Rendimento: m do sólido puro x 100%
m do sólido impuro

Característica e toxidadeCOMPOSTO CARCTERÍSTICAS TOXIDADES
Diclorometano
Líquido incolor, com vapores não inflamáveis .
Pode causar fadiga, sonolência, náuseas, aversão à luz, irritação da pele e dos olhos. Possível agente carcinogênico
Cafeína Sólido cristalino branco , inodoro e de gosto amargo
Estimulante do SNC, diurético, apresenta ação vaso-constritora e bronco-dilatadora.
ÁguaLíquido, incolor, inodoro e insípido Substância essencial para a vida
Sulfato de sódioSólido cristalino, inodoro, eflorescente
Ação purgativa
Hidróxido de sódioSólido cristalino opaco absorve rapidamente H2O e CO2do ar.
Causa irritação das vias aéreas, queimaduras nos olhos e pele, perda temporária de cabelo. Sustância muito corrosiva.

ConstantesCOMPOSTO FÓRMULA MF
(g/mol)p.f.(°C)
p.e.(°C)
DENSIDADE (g/mL)
SOLUBILIDADE(g/ mL)
DiclorometanoCH2Cl2 84,93 -95 39,7
51,3255 1/50
CafeínaC8H10N4O2 194,19 238 1,23 1/46
ÁguaH2O 18,02 0 100 0,997 ---
Sulfato de sódioNa2SO4 142,04 800 --- 2,7 1/3,6
Hidróxido de sódioNaOH 40,00 318 --- 2,13 1/0,9

•Diclorometano:
Inalação:
I.remover o indivíduo do local e levá-lo para o ar fresco;II.Se a respiração for dificultada ou parar, dar oxigênio ou fazer respiração artificial.
Contato com olhos e pele:
I.remover roupas e sapatos contaminados e enxagüar com muita água;II.Manter as pálpebras abertas e enxagüar com muita água.
Primeiros Socorros

• Hidróxido de Sódio
Inalação:I.remover o indivíduo ao ar livre; II.se não estiver respirando, fazer respiração artificial; III.se respirar com dificuldade, dar oxigênio;IV.e procurar ajuda médica.
Ingestão:I.não induzir ao vômito; II.dar grandes quantidades de água ou leite; III.não dar algo pela boca ao indivíduo inconsciente.

Contato com a pele:I. lavar imediatamente em água corrente por, pelo
menos, 15 minutos;II. remover a roupa contaminada e os sapatos;III. lavar a roupa e os sapatos antes de reutilizá-los;IV. procurar ajuda médica.
Contato com os olhos:
I. lavar imediatamente com água corrente por pelo menos 15 minutos, abrindo e fechando ocasionalmente as pálpebras;
II. procurar ajuda médica imediatamente.

BibliografiasLivros:
• Vogel, A. I., Química Orgânica – Análise Orgânica Qualitativa – Volume 1, Costa, C.A.C., Santos, O.F., Neves, C.E.M., Rio de Janeiro, Livro Técnico S.A., 3a edição, 1981, páginas 40, 41, 67, 68, 150, 154, 156
Baccan, N., Introdução à Semimicroanálise Qualitativa, Editora da UniversidadeEstadual de Campinas – Unicamp, 6ª edição, página 103.
Sites:
www.faenquil.br
www.qmc.ufsc.br
www.estudantenet.hpg.ig.com.br
http://labjeduardo.iq.unesp.br
www.gluon.com.br/fq/imagens.htm
www.qca.ibilce.unesp.brwww.cetesb.sp.gov.brhttp://pt.wikipedia.orgwww.geocities.com/gutsantos/qui/fisqui/pro
col.htm

Alcalóide ( de álcali, básico, com o sufixo -oide, "-semelhante a" ) é uma substância de caráter básico derivada de plantas que contêm, em sua fórmula, basicamente nitrogênio, oxigênio, hidrogênio e carbono.
Seus nomes comuns e que estamos mais habituados a ver, geralmente terminam com o sufixo ina: cafeína (do café), cocaína (da coca), pilocarpina (do jaborandi), papaverina/morfina/heroína/codeína (da papoula), bromelina (do abacaxi), papaína (do mamão) etc.
São geralmente sólidos brancos (com exceção da nicotina). Nas plantas podem existir no estado livre, como sais ou como óxidos. Eles também correspondem aos principais terapêuticos naturais com ação: anestésica, analgésica, psico-estimulantes, neuro-depressores, etc. Os alcalóides podem ser classificados quanto à sua atividade biológica; quanto à sua estrutura química; e quanto à sua origem biosintética (maneira de produção na planta). Podem ser divididos em três grupos:
•Alcalóides verdadeiros, que possuem anel heterocíclico com um átomo de nitrogênio e sua biosíntese se dá através de um aminoácido;
•Protoalcalóides, átomo de nitrogênio que se originam de um aminoácido (exemplo: cocaína); e
•Pseudo-alcalóides, são derivados de terpenos ou esteróides e não de aminoácidos.

Xantina é uma base purínica, composto orgânico existente no músculo, na urina, em vários orgãos e em algumas plantas.
Estrutura química do alcalóide codeína, um derivado do ópio.

A celulose é um polímero de "cadeia longa" composto de um só monômero, carboidratado, classificado como polissacarídeo. É o componente estrutural primário das plantas e não é digerível pelo homem. Alguns animais, particularmente os ruminantes, podem digerir celulose com a ajuda de microrganismos simbióticas. Écomum nas paredes celulares de plantas, tendo sido assim notado pela primeira vez em 1838. Ela está naturalmente na maioria das fibras puras de algodão, sendo encontrado em toda planta na combinação de lignina com qualquer hemicelulose.
A estrutura da celulose se forma pela união de moléculas de β-glucose através de ligações β-1,4-glucosídico, o que a faz ser insolúvel em água. É uma hexasona por hidrólise da glicose da glucosa. A celulose é um polímero de cadeia longa de peso molecular variável, com fórmula empírica (C6H1005)n, com um valor mínimo de n=200.
A celulose tem uma estrutura linear ou fibrosa, na qual se estabelecem múltiplas pontes de hidrogênio entre os grupos hidroxilas das distintas cadeias juntapostas de glicose, fazendo-as impenetráveis a água, e originando fibras compactas que constituem a parede celular dos vegetais.

Clorofila é a designação de um grupo de pigmentos fotossintéticos presente nos cloroplastos das plantas(em sentido geral, incluindo também as algas, cianofíceas e diversos protistas anteriormente considerados "algas" ou "plantas", como as algas vermelhas ou castanhas).
A intensa cor verde da clorofila se deve a suas fortes absorções das regiões azuis e vermelhas do espectro eletromagnético, e por causa destas absorções a luz que ela reflete e transmite parece verde. Ela é capaz de canalizar a energia da luz solar em energia química através do processo de fotossíntese. Neste processo a energia absorvida pela clorofila transforma dióxido de carbono e água em carboidratos e oxigênio.
As moléculas de clorofila encontram-se especificamente em complexos proteicos denominados fotossistemas, que se encontram integrados nos tilacóides de cloroplastos. A maioria das moléculas de clorofila absorve luz e transmite a energia luminosa através de um fenómeno designado por "transferência de energia por ressonância" a um par de moléculas de clorofila específico que se encontra no centro reaccional dos fotossistemas.
A clorofila é um pigmento clorínico com quatro anéis pirrolo ligados por metinas, e um quinto anel ausente em outras porfirinas, grupo de compostos ao qual pertence e que inclui compostos como o grupo heme. No centro do anel há um íon de magnésio (Mg2+) coordenado por quatro átomos de azoto. O composto édenominado feofitina quando não se encontra magnésio (ou outro íon metálico) no seu centro. As cadeias laterais variam em certo nível entre as diferentes formas de clorofila encontradas em diferentes organismos, mas todas possuem uma cadeia fitol (um terpeno) ligada por uma ligação éster a um carboxilo do anel IV
A clorofila não é solúvel em água e é mais instável em pH ácido. Mas, é muito mais solúveis em água do que em diclorometano.

Taninos são grupos de compostos químicos polifenólicos, de alto peso molecular, de origem vegetal, não nitrogenadas, provocando na pele íntegra a sensação de adstringência e na pele sem vida um fenômeno conhecido porcurtimento, que a transforma em couro. Propriedades gerais:- são solúveis em água, álcool e acetona.- são precipitados por sais de metais pesados (azul , negro, verde).- são insolúveis no éter puro, clorofórmio e benzeno.
Flavonóide é o nome dado a um grande grupo de fitoquímicos ou fitonutrientes, que são polifenóis de baixa massa molecular, encontrados em diversas plantas. É encontrado em várias frutas e vegetais em geral, assim como em alimentosprocessados como chá e vinho.
Os benefícios do consumo de frutas e outros vegetais é geralmente atribuído mais aos compostos flavonóides, do que aos outros conhecidos nutrientes, devido ao vasto leque de efeitos biológicos que incluem entre outros: ação anti-inflamatória, anti-alérgica e anti-câncer.
Os taninos e os flavonóides são duas classes de compostos que apresentam caráter ácido. Ambos são mais solúveis em diclorometano que em água.