B SC PONTO DE EBULIÇÃO. QUANDO UMA SUBSTÂNCIA ENTRA EM EBULIÇÃO, HÁ UM AFASTAMENTO DAS...
Transcript of B SC PONTO DE EBULIÇÃO. QUANDO UMA SUBSTÂNCIA ENTRA EM EBULIÇÃO, HÁ UM AFASTAMENTO DAS...

B SCPONTO DE EBULIÇÃO


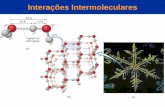
QUANDO UMA SUBSTÂNCIA ENTRA EM EBULIÇÃO, HÁ UM AFASTAMENTO DAS MOLÉCULAS, COM ROMPIMENTO DAS FORÇAS INTERMOLECULARES, ENTÃO, QUANTO MAIOR A INTENSIDADE DAS FORÇAS INTERMOLECULARES, MAIOR O PONTO DE EBULIÇÃO (PE) DA SUBSTÂNCIA, MENOS VOLÁTIL É A SUBSTÂNCIA.


PARA SUBSTÂNCIAS COM MASSAS MOLECULARES PRÓXIMAS:
FDI < FDP < PONTE DE HIDROGÊNIO
AUMENTA A INTENSIDADE DA FORÇA INTERMOLECULAR E AUMENTA O PE

2. SUBSTÂNCIAS APOLARES
MAIOR A SUPERFÍCIE DE CONTATO(MAIOR MASSA MOLECULAR)MAIOR A INTENSIDADE DAS FORÇAS
DE LONDON E PORTANTO, MAIOR O PONTO DE EBULIÇÃO.

+ +
- -FORÇA DE VAN DER WAALS MENOR
FORÇA DE VAN DER WAALS MAIOR
+ +
- -
+ + + + + +
- - - - - -
+ + + + + + - - - - - -

PARA OS HALOGÊNIOS, O AUMENTO DA MASSA MOLECULAR FAZ AUMENTAR O PONTO DE EBULIÇÃO.
F2(g)< Cℓ2(g) < Br2(ℓ)< I2(s)

3. RAMIFICAÇÃO E PONTO DE EBULIÇÃO
PARA SUBSTÂNCIAS DE MASSAS MOLECULARES PRÓXIMAS, A DE CADEIA CARBÔNICA RAMIFICADA TEM MENOR PONTO DE EBULIÇÃO.
A RAMIFICAÇÃO DIMINUI A SUPERFÍCIE DE CONTACTO ENTRE AS MOLÉCULAS, DIMINUINDO A INTENSIDADE DAS FORÇAS INTERMOLECULARES.

DIMETILPROPANO
M.M. = 72 u
PE = 9°C
PENTANO M.M. = 72u PE=36°C
H3C-CH2-CH2-CH2-CH3
CH3
CH3 C CH3
CH3


4. POLARIDADE E PONTO DE EBULIÇÃO
PARA SUBSTÂNCIAS COMMASSAS MOLECULARES
PRÓXIMAS,A MAIS POLAR TEM MAIOR PONTODE EBULIÇÃO.

H3C – CH2- CH3 μtotal = 0 (APOLAR)
M.M. = 44u PE = -42°C
H3C-C = N μtotal ≠ 0 (POLAR)
M.M. = 41u PE = 82°C

5. PONTE DE HIDROGÊNIO E PONTO DE EBULIÇÃO
COMPOSTOS QUE ESTABELECEM PONTES DE HIDROGÊNIO TÊM O PONTO DE EBULIÇÃO ANORMALMENTE ELEVADO.

H – O ................... O – H
H H
PONTE DE H M.M. = 18u PE = 100°C
H
H C H
H
H
H C H
H
LONDON
M.M. = 16u PE = -161°C


H2O
H2SH2Se
H2Te















![Ligação química - Ligações intermoleculares...Ligação química - Ligações intermoleculares [Imagem: ]13 Miscibilidade É possível prever a miscibilidade ou não entre duas](https://static.fdocumentos.com/doc/165x107/5f97f6c1a9d3785b3b504013/ligao-qumica-ligaes-ligao-qumica-ligaes-intermoleculares.jpg)

