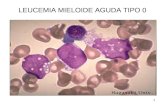
1 LEUCEMIA MIELOIDE AGUDA TIPO 0. 2 LEUCEMIA MIELOIDE AGUDA TIPO 1.
Leucemia MielomonocíticaJuvenil (1996) · PDF file1 DIAGNÓSTICO E TRATAMENTO...
Transcript of Leucemia MielomonocíticaJuvenil (1996) · PDF file1 DIAGNÓSTICO E TRATAMENTO...

1
DIAGNÓSTICO E TRATAMENTO
Maria Lucia de Martino Lee
Leucemia Mielomonocítica Juvenil (1996)
�Desordem do grupo pediátrico previamente denominada leucemia mielóide crônica juvenil (LMCJ) ou LMMC (equivalente a classificação FAB) ou síndrome da monossomia do 7.
�É uma patologia hematopoiética clonal com características mieloproliferativas e displásicas.
SMDSMD SMD/SMPSMD/SMP SMPSMP
ARAR LMMJLMMJ LMC Ph+LMC Ph+
ARSAARSA LMMCLMMC TETE
CRCR LMC ATIPLMC ATIP PVPV
AREBAREBInclassificávelInclassificável
MIMILEoC
MastocitoseInclassificável
Epidemiologia
�Representa 2 – 3 % das leucemias infantis (1,2
casos/milhão ccas/ano)
�Faixa etária: 95% dos casos entre 0 – 6 anos (média 1a8m). *8% casos em maiores de 6 anos.
�Sexo: predomínio masculino (2:1)
�25 – 30% dos casos ocorrem em crianças com diagnóstico clínico de neurofibromatose tipo I (NF1).
(risco 200 – 350 vezes maior que não portadores NF1).
�Síndrome Noonan (mut PTPN11): associação com LMMJ (remissão espontânea)
Advances in Hematology 2012;12:1-7

2
Diagnóstico
Características clínicas
Características laboratoriais
Características clínicas:
% pacientes
Palidez 64
Febre 54
Sangramento cutâneo 46
Infecções 45
Tosse (seca) 40
Dor abdominal 7
Dor óssea <4
Esplenomegalia 97
Hepatomegalia 97
Linfadenopatia 76
Lesões ou rashcutâneo/sangramento pele
36
Blood 1997;89:3534-3543
Taquipnéia;RX c/infitrado intersticial
Características Laboratoriais
�Sangue periférico
– Tem aspectos característicos, sendo frequentemente mais útil e importanteque a MO para o diagnóstico
Achados no sangue periférico:
�Leucocitose (↑10 x109/L) com precursores mielóides
++++�Monocitose (↑ 1x109/L)
++++�Plaquetopenia
++++�Anemia

3
Leucócitos (x109/L)<50 70%50 – 99 22%>100 8%
Hemograma
Hb (g/dL):<8 34%>8 – 12 66%
(<11)
(25 – 35)
Hemograma
� Monócitos (x109/L) <5 35%5 – 9 32%>10 33%
(>1 x 109/L)
� Plaquetas (x109/L)<50 47%50 – 99 30%>100 23%
(~14% <20.000)
Avaliação do esfregaço
– Leucócitos:– Neutrofilia, com desvio escalonado até promielócitos
– Basofilia e/ou eosinofilia (não proeminentes)
– Sinais de displasia (pseudo-Pelger, hipogranulação em NT, núcleo em anel)
–Monócitos:�Em geral maduros, promonocitos.
�Sinais de displasia: vacuolização citoplasmática
�Núcleo com: aumento na basofilia e na hipersegmentação
�Forma bizarra
Avaliação do esfregaço
–Blastos:
�Em geral com mediana inferior a 2% e raramente excedendo a 20%.
Avaliação do esfregaço

4
–Eritrócitos:
�Normocitose (mais comum)�Macrocitose�Microcitose�Hipocromia�Dismorfismo�Eritroblastos (freqüentes)
Avaliação do esfregaço
–Plaquetas:
�Plaquetas gigantes�Em geral: diminuídas
Avaliação do esfregaço
Mielograma
�A avaliação isolada da MO não é diagnóstica. Os achados devem ser correlacionados com os demais aspectos clínicos e laboratoriais.
Achados morfológicos em MO
Celularidade: Hiper/normocelular
� Setor eritrocítico:
– Em geral diminuído
– Precursores eritróides megaloblásticos
– Displasias (assincronismo maturativo, cariorrexis, pontes intercelulares, ...)
� Setor granulocítico:
– Hiperplásico
– Predomínio de formas mielóides imaturas (promielócitos e mielócitos)
– Assincronismo maturativo
– Granulócitos maduros com hipogranularidade e hipolobulação (pelgeróides)

5
� Setor monocítico:
– Monocitose menos evidente que no SP (em geral 5 – 10% células medulares)
� Setor megacariocítico:
– Megacariócitos reduzidos ou ausentes em cerca 75% casos.
– Sinais de displasia eventuais: micromegacariócitos, hipolobulação.
�Blastos:– menos de 20% das células medulares (eventualmente entre 20 – 30%).
– Ausência de B. Auer.
Blastos MO
0 – 9 64%
10 – 20 26%
>20 10%

6
BIOPSIA DE MEDULA ÓSSEA :
• Pode ser descartada na maioria dos casos
• Fibrose reticulínica pode ser observada em alguns pacientes.
�Análise citogenética:
�Normal 65%�Monossomia 7 25%*�Outros 10%
* Menores leucometrias, maior numero de monócitos no diferencial, hemaceasmacrocíticas, HbF normal ou moderadamente elevada.
� Eletroforese de Hb:
– Hemoglobina Fetal:elevada para idade –maioria dos casos (característico dos casos com cariótipo normal.)
– Em níveis ≥10%: prognóstico desfavorável (idade, plaquetas)
Critérios diagnósticos recomendados
Características clínicas sugestivas
Hepatoesplenomegalia
Linfadenopatia
Palidez
Rash cutâneo
Critérios laboratoriais mínimos(todos os 3 devem estar presentes)
Monócitos em SP>1 x109/L
MO com <20% blastos
Ausência cromossomo Ph ou rearranjo bcr-abl
Outros critérios diagnósticos(no mínimo 2)
Hb fetal aumentada para idade
Precursores mielóides no SP
Leucometria >10 x109/L
Anormalidade clonal
Crescimento espontâneo in vitrode progenitores GM
Atuais critérios diagnósticos de LMMJ - OMS

7
TRATAMENTO TRATAMENTO = TMO
SMD
LMA
LMMJ
Sobrevida Global após TMO em Crianças Brasileiras
Tratamento = TMO
� Objetivos:
• Alívio dos sintomas
• Redução da dependência transfusional e
complicações associadas
• Melhorar as citopenias
• Melhorar a qualidade de vida
• Retardo na progressão para LMA
• Prolongar a sobrevida
O que fazer antes do TMO?
Leucemia Mielomonocítica Juvenil
Panorama geral do tratamento
TMODoador aparentado Doador Não aparentado
O que fazer Pré TMO?QT convencional
QT em baixas doses Inibidor farnesil transferase - Tipifarnib
Hipometilantes?
Interferon
Isotretinoina
Esplenectomia
� Tratamento de suporte � Transfusões, antibióticos, quelantes de ferro
� Agentes imunomoduladores � Lenalidomida, talidomida, ATG, ciclosporina
� Agentes diferenciadoresácido 13-cis- retinóico, ATRA, arsenico
� Quimioterapia em baixas doses (ara-c, 6MP, Hy,...)
� Quimioterapia intensiva (~LMA)
� Terapia modificadora da transcrição genética� Agentes hipometilantes (azacitidina)
� Inibidores da histona deacetilase
Inúmeras Opções
Nimer SD.Blood 2008

8
Leuk Res 2004
�Objetivo: Reduzir o “bulk” de doença pré TMO
�Diferentes fatores podem influenciar
�A decisão final deve ser baseada em múltiplos paramêtros
�Requer análise individual
�Baixos índices de remissão
�Benefício discutível
Quimioterapia
�Estudo atual EWOG – MDS: NÃO recomenda para grande maioria dos pacientes.
�Em pacientes em transformação blástica ou infiltração pulmonar de grande impacto clínico: Fludarabina e HDAra-c
(esquema citorredução proposto COG – LMMJ study) pode proporcionar melhora temporária.
Quimioterapia Intensiva
Pui CH – Childhood Leukemias 2012
Quimioterapia em Baixas doses
5/11 pts : novo clone 1 – 14 m após 6 MP
Aparentemente há uma sensibilidade aumentada da células LMMJ ao INF
Estudo fase 2 POG : interrompido por toxicidade.
Mas:
Interferon
Bone Marrow Transpl 2000 ; 26:681
�Pode inibir in vitro o crescimento espontâneo das células da LMMJ
�Estudo POG (fase II): 5/22 crianças tratadas com Isotretinoina - tiveram RCC e 4 RP.
Isotretinoína

9
Valor da Isotretinoína ainda a ser determinado
5 pcts LMMJ – vivos, mediana 27 m
Terapia Alvo – Inibidores da Farnesiltransferase
(Tipifarnib)
-Protocolo COG para pacientes com LMMJ avaliou a eficácia do uso do Tipifarnib como janela terapeutica no estudo ( dose de 200 ou 300 mg/m²/mês a casa 21 dias.-Não foi observado impacto no aumento da sobrevida ou no tempo de duração das respostas.
Advances in Hematology 2012;12:1-7
Terapia Epigenética: Agentes Hipometilantes
JCO 2006
Número de pacientes: 268Dose : 75 mg/m²/d x 7 dias, a cada 28 dias
Quesnel et al. Blood 1998;91:2985–90
Sobrevida SMD de acordo com estado de metilaçãoDo gene p15INK4b
�Metilação aberrante tem sido amplamente estudada em adultos com SMD�Poucos estudos em crianças�Estudo grupo brasileiro (Daniel Vidal, Luiz Fernando Lopes et al):
- Metilação de 13 genes foram estudados- 21 pacientes pediátricos com SMD (AREB ou AREBt)- Gene CALCA estava metilado em 85,7% - Gene CDKN2B estava metilado em 50%
�Conclusão do estudo:- Metilação aberrante está presente nas crianças com SMD, sugerindo ser similar aos adultos- Tratamento com agentes hipometilantes pode ser benéfico- Outros estudos serão importantes para identificação de outros genes metilados envolvidos na iniciação e progressão da SMD em crianças

10
Terapia Epigenética: Agentes Hipometilantes
Parecem ter importante papel na citorredução pré - TMO
Estudo fase I/II de azacitidina em pacientes pdiátricos portadores de SMD avançadas/LMMJ
�Objetivos Primários: Estabeler a dose recomendada e eficácia preliminares em crianças com SMD avançada ( AREB/AREB-t) e LMMJ em 4 diferentes grupos
�Dose : 75 – 100 mg/m²/d x 7 d a cada 28 dias
�Número de ciclos mínimos pré TMO : 3 ciclos
Grupo EWOG-MDS
PROPOSTA: Protocolo com Azacitidina pré TMO para pacientes pediátricos com síndromes mielodisplásicas avançadas (areb, arebt) e leucemia mielomonocítica juvenil
Dr Luiz Fernando Lopes
Dra Roseane Vasconcelos Gouveia
Dra Adriana Seber
Dra Maria Lúcia de Martino Lee
Dr Daniel Vidal
Dra Neysimélia Costa Villela
Grupo Cooperativo Brasileiro de Síndromes
Mielodisplásicas e Mieloproliferativas
Estudo piloto multi–institucional, não randomizado, fase II
� Objetivos primários: � Estabelecer resultados preliminares da eficácia da
azacitidina na dose de 75mg/m²/dia, pré TMO (min 3 ciclos)
� Objetivos secundários: � Avaliar segurança e efeitos adversos
� Determinar prelinarmente respostas hematológicas e citogenéticas
� Avaliar o padrão de metilação antes de cada ciclo
Agradecimento Especial:
Dra Roseane Vasconcelos Gouveia
Dra Adriana Seber