LUCIANA SOUZA JORGE - fcmsantacasasp.edu.br · recaída de uma infecção que foi tratada...
Transcript of LUCIANA SOUZA JORGE - fcmsantacasasp.edu.br · recaída de uma infecção que foi tratada...
LUCIANASOUZAJORGE
AvaliaçãodasInfecçõesÓsseasPós-cirúrgicasocorridasemumhospitaluniversitário
Tese apresentada ao Curso de Pós Graduação da Faculdade deCiênciasMédicasdaSantaCasadeSãoPauloparaobtençãodoTitulodeDoutoremCiênciasdaSaúde.
SÃOPAULO
2017
LUCIANASOUZAJORGE
AvaliaçãodasInfecçõesÓsseasPós-cirúrgicasocorridasemumhospitaluniversitário
Tese apresentada ao Curso de Pós Graduação da Faculdade deCiênciasMédicasdaSantaCasadeSãoPauloparaobtençãodoTitulodeDoutoremCiênciasdaSaúde.
ÁreadeConcentração:CiênciasdaSaúde
Orientador:MauroJoséCostaSalles
SÃOPAULO
2017
DEDICATÓRIA
Aos meus pais, Farid Jorge (in memorian) e Nair Jorge, pelo exemplo de vida e por
acreditarem nos meus sonhos.
Aos meus pacientes, cuja esperança e confiança incondicional me fizeram entender a importância da
minha postura na vida deles
AGRADECIMENTOS
A Deus, pela oportunidade da vida e do conhecimento. À Faculdade de Medicina (FAMERP) e ao Hospital de Base de São José do Rio Preto (FUNFARME), pela graduação, residência médica e experiência de vida. Ao Serviço de Infectologia do Hospital de Base de São José do Rio Preto, pela oportunidade de trabalho. Aos eternos mestres Prof Dr Irineu Luiz Maia e Prof Célia Franco, pela seriedade, comprometimento, conhecimento e profissionalismo, que moldaram minha personalidade e desenharam minha postura médica. Ao Serviço de Ortopedia e Traumatologia do Hospital de Base de São José do Rio Preto, pelo respeito profissional e, em especial, ao Prof Dr Alceu Gomes Chueire, pelo apoio e divulgação do meu trabalho. Aos médicos residentes de Ortopedia e Traumatologia, pela dedicação aos pacientes. Ao diretor do Hospital de Base, Prof Jorge Fares, pelo incentivo inicial e permanente. Aos médicos e enfermeiros do Serviço de Controle de Infecção Hospitalar, pela fidelidade e companheirismo de trabalho. Ao meu orientador de doutorado, Prof Dr Mauro José Costa Salles, pelo interesse, incentivo, ensinamentos e amizade em todos os momentos. À Prof Dra Patrícia da Silva Fucuta, pela amizade, paciência, disponibilidade e ensinamentos em estatística. Ao médico Marcelo Arruda Nakazone, pelo apoio em todas as fases do processo de tese. Ao Serviço de Enfermagem do Hospital de Base de São José do Rio Preto, especialmente na enfermaria do sexto andar, pelo amor e dedicação aos pacientes.
À Pós-Graduação da Faculdade de Ciências Médicas de São Paulo, pela oportunidade de aquisição de
conhecimentos que me levaram a concluir a Tese de Doutorado.
ABREVIATURAS
ASA - American Society of Anesthesiologists
BD – Becton, Dickinson and Company
BGP – Bacilos Gram-positivos
BHI - brain-heart infusion
CDC – Centers for Disease Control and Prevention
CGP – Cocos Gram-positivos
DP – Desvio Padrão
DRS – Divisão Regional de Saúde
ECN – Estafilococos Coagulase-negativo
FIG – Figure
HR – Hazard Ratio
IC – Intervalo de Confiança
ISC – Infecção de Sítio Cirúrgico
MRSA – Methicillin Resistant Staphylococcus aureus
NSHN - National Healthcare Safety Network
PMMA - Polimetilmetacrilato
OMM – Osteomielite Monomicrobina
OPM – Osteomielite Polimicrobiana
OPT – Osteomielite Pós-traumática
OR - Odds Ratio
SPSS® Statistics Base – Software de Base Estatística
USA – United States of America
VS - Versus
1. Introdução
A osteomielite é uma doença heterogênea em relação à fisiopatologia, à apresentação clínica e ao tratamento. No
entanto, existem características comuns que a definem, como a presença de pus, que se dissemina pelos canais vasculares
do osso acometido e aumenta a pressão intra-óssea, prejudicando o fluxo sanguíneo e consequente formação de
fragmento não vascularizado, denominados sequestro, que resultam em necrose tecidual óssea.1,2 Uma das classificações
mais utilizada contempla parâmetros como duração da doença, sendo reconhecida como aguda ou crônica, e mecanismo
de infecção, seja hematogênica ou contígua, além da presença ou não de insuficiência vascular associada.3
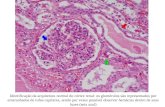
Histologicamente, a osteomielite aguda é definida como infecção óssea recente e caracteriza-se pela presença de
micro-organismos, infiltrados de neutrófilos, trombose e congestão vascular.1,3 A osteomielite crônica é definida como a
recaída de uma infecção que foi tratada previamente ou não, com importante necrose tecidual. Nesses casos, o quadro
clínico evolui por um período que pode se estender por meses ou até mesmo anos. É também caracterizado por
inflamação de longo curso, pela presença de pus, de micro-organismos e de sequestros; além do comprometimento de
partes moles circunvizinhas e, em algumas vezes, por fístulas.3,4
A osteomielite associada à insuficiência vascular tem o pé diabético infectado como o principal exemplo e acomete
15% dos pacientes em algum momento da vida. No desenvolvimento da doença, a insuficiência vascular, a neuropatia e a
hiperglicemia têm papel crucial na formação da úlcera de perna e da osteomielite subsequente.5,6
A infecção óssea hematogênica é ocorrência rara e pode afetar qualquer osso. A forma aguda acomete, geralmente,
crianças e idosos, usuários de drogas injetáveis e portadores de cateter venoso central. Um exemplo deste tipo de
osteomielite e de difícil resolução é aquela que acomete a coluna vertebral, dado o difícil acesso para desbridamento
cirúrgico e a consequente dependência quase exclusiva da terapia antimicrobiana.1,5 Já, as infecções ósseas por
disseminação contígua são causadas pela inoculação direta de micro-organismos, e podem resultar de fraturas fechadas e
expostas ou de procedimentos cirúrgicos ortopédicos, em especial, aqueles ligados ao implante de próteses.1
As fraturas expostas geralmente acometem os homens jovens, principalmente em ossos dos membros inferiores
como o fêmur, a tíbia e a fíbula.1 Infecções tratadas inadequadamente ou não tratadas comprometem a consolidação dos
locais de fratura e resultam em osteomielite crônica e/ou amputação do membro acometido. De fato, em 25% das
infecções ósseas crônicas, os agentes são os mesmos previamente detectados como colonizantes nas culturas efetuadas
imediatamente após o trauma.1 Inúmeros são os fatores que modulam o risco de infecção da fratura exposta e, dentre os
mais relevantes, estão a energia do trauma, a extensão da ferida, com a presença ou não de lesão vascular, em graus I, II e
III, segundo definido por Gustilo e Anderson em 1976.7
Gustilo e Anderson dividiram as fraturas expostas em três tipos de acordo com a gravidade da lesão (Tipo I:
ferimento cutâneo menor que 1 cm, ferida limpa ou com contaminação mínima, sem cominuição da fratura e mínima
lesão de partes moles; Tipo II: ferimento maior que 1 cm, sem lesão extensa de partes moles, contaminação moderada,
cominuição moderada da fratura; e Tipo III, que foi posteriormente subdividida IIIA: ferimento maior que 10 cm, com
contaminação e lesão grave de partes moles, mas com possível cobertura óssea, além das fraturas fechadas cominuídas;
Tipo IIIB: perda muito grave de partes moles com exigência de cirurgia reconstrutiva, e Tipo IIIC: lesão vascular que
exige reparo cirúrgico e alto risco de amputação).7
A ocorrência de infecção pós-fratura varia de 3% a 25% dos casos, dependendo de fatores relacionados ao trauma.
Dentre eles, a energia do trauma, as condições da ferida cirúrgica, o tipo de estabilização esquelética imediata; o tempo
de exposição do osso fraturado, desde o trauma até a estabilização esquelética e a infusão antimicrobiana; a gravidade do
paciente, incluindo o volume de sangue transfundido e o tempo cirúrgico.1,8
Um outro fator, que acrescenta gravidade à infecção pós-traumática e dificulta seu diagnóstico e tratamento, é o
aparecimento tardio de seus sinais e sintomas.2 Anualmente, milhões de pacientes em todo o mundo têm sido submetidos
a implantes articulares, permitindo a restauração da função dos membros devido a doenças degenerativas
osteoarticulares, processos infecciosos graves e/ou fraturas.9 Entretanto, a infecção pós-artroplastia, uma das
complicações deste procedimento e que geralmente exige reintervenções cirúrgicas para uma boa evolução, apresenta
taxas variando de 1% a 5%, de acordo com o serviço e a equipe médica correlacionada, representando cerca de 4000 a
8000 próteses articulares infectadas anualmente, com alta morbimortalidade.10
Na metade do século XX, foram publicados os primeiros estudos sobre a utilização de material de síntese nas
cirurgias ortopédicas e, desde então, o polimetilmetacrilato (PMMA) tem sido o composto mais utilizado nos cimentos
ósseos.11,12 No entanto, o cimento de PMMA tende a inibir as funções fagocíticas, linfocíticas e do complemento in
vitro.13,14 Além disso, compartilha com os demais biomateriais, a propriedade de adesão de micro-organismos infectantes
e subsequente infecção, que geralmente inicia-se na interface entre o cimento e o osso e pode comprometer o espaço
articular.15
Interpretados como corpos estranhos, as sínteses usadas na estabilização óssea pós-traumática, tais como, hastes,
placas, pinos, parafusos e próteses, e o cimento com PMMA predispõem o tecido ósseo e o espaço articular ao processo
séptico, ao justificar que, mesmo uma reduzida carga microbiana estabeleça a infecção e permaneça na superfície
avascular do dispositivo, protegida das defesas imunológicas circulantes do hospedeiro e dos antimicrobianos de uso
sistêmico.16
Adicionalmente, a necrose isquêmica dos tecidos de partes moles, o hematoma da ferida operatória, a celulite e os
abscessos de sutura são fatores que precedem comumente as infecções peri-protéticas.9
A microbiota normal da pele, a população bacteriana do solo e os micro-organismos que colonizam o ambiente
hospitalar podem participar ativamente da etiologia da osteomielite. Por sua vez, a identificação microbiana na
osteomielite é crucial, pois a terapia sistêmica específica com antimicrobianos baseia-se no agente isolado e em seu perfil
de sensibilidade aos antimicrobianos.1
A história de fratura está associada com uma ampla extensão de micro-organismos que abrande aqueles associados
a infecções relacionadas à assistência à saúde, tais como, Staphylococcus aureus resistente à oxacilina, bacilos gram-
negativos da microbiota intestinal e estafilococos coagulase-negativo.17 Entretanto, Jones ME et al relatou que S. aureus,
seja suscetível ou resistente à oxacilina, ainda foi a bactéria mais isolada nas infecções ósseas (32%), apesar desta
porcentagem representar um resultado menor de casos em relação a outros estudos.18 Segundo Sheehy SH et al, as
infecções ósseas polimicrobianas foram detectadas em 29% dos casos.17 Um agravante da presença de micro-organismos
potencialmente infectantes nas sínteses ósseas é o fato das mesmas servirem como sítio de colonização para agentes
formadores do biofilme.10
O biofilme caracteriza-se por microcolônias permeadas por matriz polimérica extracelular protetora que, por sua
vez, pode aderir a superfícies artificiais e aos tecidos adjacentes ao implante.10,19,20 Constitui comunidades complexas
cooperativas de uma ou mais espécies de bactérias e/ou fungos, e exibe discreta organização temporal e espacial e ampla
extensão de mecanismos ambientais ligados às respostas adaptativas a nível populacional.19,20 Após estabelecido, é quase
impossível erradicar o biofilme, mesmo no paciente imunocompetente e/ou submetido a altas doses de
antimicrobianos.10,19,20
Atualmente, não há consenso sobre a terapia antimicrobiana para a osteomielite relacionada ao trauma ou para as
infecções peri-protéticas.21 Tal deficiência reflete em agravos para o paciente, como a cronicidade e a recorrência, que
associadamente ao uso inadequado dos antibióticos, podem contribuir com a seleção de cepas bacterianas resistentes e
consequente aumento da morbidade.22 Além disso, não existem protocolos universais validados, acerca de qual(is)
espécime(s) clínico(s) deva(m) ser coletado(s) (biópsia de fragmento ósseo ou outros) ou ainda por meio de qual(is)
procedimento(s) (punção aspirativa, swab, fistulectomia).23 Ademais, o isolamento e a identificação de bactérias
anaeróbias, potencialmente importantes nesses casos, são de difícil execução.24 Neste contexto, justifica-se a vigilância
epidemiológica de cada serviço de traumatologia e ortopedia, a fim de buscar o conhecimento dos micro-organismos
implicados na infecção óssea, bem como o seu perfil de sensibilidade aos antimicrobianos. Igualmente, é fundamental
avaliar a prevalência, a incidência e os fatores de risco associados às osteomielites pós-taumáticas e os preditores do
insucesso terapêutico.17
A despeito dos problemas decorrentes das infecções ósseas, tais como, a morbidade e os custos gerados ao Sistema
Único de Saúde, publicações relativas à epidemiologia, particularidades microbiológicas, tratamento e prevenção das
mesmas são escassas na literatura nacional, restritas a poucos serviços. Por sua vez, na região Noroeste paulista, não
existem serviços de vigilância epidemiológica e equipes multidisciplinares para o diagnóstico, tratamento e/ou
acompanhamento dessas infecções, ao contrário da realidade observada nos países desenvolvidos.
Hospital de Base de Rio Preto consta de 874 leitos e é centro de referência direta para uma região que compreende
102 municípios e mais de 2 milhões de habitantes, sob a administração da Delegacia Regional de Saúde XV (DRS XV),
sediada em São José do Rio Preto e também referência em alta complexidade para todos os estados brasileiros e recebe
todos os anos, pacientes de todos as regiões do Brasil. Serviço de Ortopedia e Traumatologia representa o maior número
de pacientes atendidos em relação às outras especialidades na região do Noroeste Paulista e é dividido em
subespecialidades, tais como, membro superior, incluindo cintura escapular e ombro; quadril, incluindo cintura pélvica e
fêmur; joelho; membros inferiores e cirurgia do pé; e ainda possui, na sua equipe, uma médica infectologista e uma
enfermeira específicas que trabalham no Serviço de Controle de Infecção Hospitalar, que realizam visitas semanais na
enfermaria de Ortopedia e Traumatologia, atendimento diário por telefone e dois atendimentos ambulatoriais por semana
em conjunto com os ortopedistas, além de realizarem os treinamentos direcionados a essa equipe.
2. Objetivos
Objetivo Primário
Avaliar a taxa de cura e os fatores preditores do insucesso terapêutico na osteomielite pós-traumática.
Objetivos Secundários
Identificar as taxas de infecções ósseas pós-traumáticas, os fatores preditores para infecção polimicrobiana, a taxa
de sucesso da terapia antimicrobiana empírica, baseada no perfil de sensibilidade microbiana, e a relação entre a
antibioticoterapia específica e a evolução para remissão
3. Casuística e Método
Trata-se de um estudo retrospectivo observacional e longitudinal, com análise dos prontuários de todos os
pacientes admitidos por fraturas de diversas modalidades e que, por este motivo, foram submetidos a procedimentos
cirúrgicos ortopédicos pelo Serviço de Ortopedia e Traumatologia no Hospital de Base de São José de Rio Preto e que
evoluíram com infecção da ferida operatória, no período de agosto de 2007 a agosto de 2012.
Os pacientes foram atendidos inicialmente pelo Serviço de Ortopedia e Traumatologia no setor de emergências
desse hospital e tratados cirurgicamente de acordo com as fraturas sofridas. Posteriormente, ainda durante a internação na
enfermaria ou em retorno precoce no ambulatório de Ortopedia e Traumatologia e na presença de critérios definidos
previamente para infecção de sítio cirúrgico, os pacientes eram avaliados pelo Serviço de \infectologia.
Critérios de Inclusão:
Todos os pacientes com idade superior a 12 anos e que sofreram fratura pós-traumática e que foram submetidos à
cirurgia ortopédica pelo Serviço de Ortopedia e Traumatologia no Hospital de Base de São José de Rio Preto.
Critérios de Exclusão:
Indivíduos que abandonaram o tratamento e o acompanhamento neste período.
Análise Microbiológica
As amostras microbiológicas foram constituídas por fragmentos ósseos e de partes moles coletados no ato
cirúrgico, a partir dos locais anatômicos infectados após o desbridamento, com o auxílio de cureta, segundo rotina pré-
estabelecida. Em seguida, os mesmos foram acondicionados em frasco estéril e encaminhados ao Laboratório Central do
HB onde foram processados.
As amostras teciduais foram separadamente incubadas em tubo contendo caldo BHI (OXOID) por 12 horas em
estufa bacteriológica a 36,5 °C. A seguir, nova incubação sob as mesmas condições ocorreu após semeadura para
posterior isolamento em Agar sangue, Agar chocolate e Agar McConkey (OXOID). Após essa primeira incubação, caso
não houvesse isolamento bacteriano, uma nova incubação por 12 horas a 36 °C foi efetuada. Os micro-organismos
isolados forma submetidos à coloração de Gram e, posteriormente, às séries bioquímicas e imunológicas específicas, a
saber: provas da catalase, coagulase e DNAse, resposta à novobiocina (CECON), kit de látex para hemaglutinação
(BioMerieux) e, por fim, kit EPM-Milli (PROBAC). As espécies bacterianas não prontamente determinadas seguiram à
identificação automatizada com o uso do Microscan (Dade-Boehringer) e placas específicas para gram-positivas e gram-
negativas (Dade-Boehringer). Todos os isolados foram submetidos ao antibiograma por disco-difusão com discos
contendo os antimicrobianos específicos para cada um dos agentes infectantes. As mostras de culturas foram inseridas no
aparelho de identificação microbiana e antibiograma VITEK.
Análise Estatística
Variáveis contínuas com distribuição normal serão apresentadas como média ± desvio padrão, ao passo que as
variáveis contínuas sem distribuição Gaussiana serão atribuídas como mediana e interquartis. As variáveis categóricas
serão apresentadas como números e proporções (%). O teste t será utilizado para comparar variáveis contínuas entre
pacientes com osteomielite, enquanto o teste χ2 ou o teste exato de Fisher será aplicado para comparação de variáveis
categóricas entre os grupos. O modelo de regressão logística Stepwise será utilizado para estabelecer preditores
independentes de infecção polimicrobiana e de recorrência no tratamento de osteomielite póstraumática. Variáveis com
reconhecida significância prognóstica serão incluídas na análise univariada e apenas aquelas associadas aos referidos
desfechos serão consideradas para a análise multivariada. Variáveis destacadas no modelo multivariado serão
consideradas como preditores independentes destes desfechos nesta população. As análises serão realizadas em Software
IBM SPSS Statistics versão 21.0. Em todas as circunstâncias, um valor de P < 0,05 será considerado estatisticamente
relevante.
Referências
1. Berbari EF, Steckelberg JM, Osmon DR. Osteomyelitis. In: Mandell GL, Bennett JE, Dolin R. Principles and Practice of Infectious Diseases. 6th Ed. Phyladelphia: Churchill Livingstone; 2005:1322-32.
2. Ciampolini J, Harding KG. Pathophysiology of chronic bacterial osteomyelitis. Why do antibiotics fail so often? Postgrad Med J 2000;76:479-83.
3. Lew DP, Waldvogel FA. Osteomyelitis. N Engl J Med 1997; 336:999-1007. 4. Waldvogel FA, Medoff G, Swartz MN. Osteomyelitis: a review of clinical features, therapeutic considerations
and unusual aspects. N Engl J Med 1970;282(4):198-206. 5. Lipsky BA, Berendt AR, Deery HG, Embil JM, Joseph WS, Karchmer AW et al. Diagnosis and Treatment of
Diabetic Foot Infections. CID 2004; 39:885–910. 6. Frykberg RG, Zgonis T, Armstrong DG, Driver VR, Giurini JM, Kravitz SR et al. Diabetic Foot Disorders: A
Clinical Practice Guideline (2006 revision). J Foot Ankle Surg 2006:45(5):S1-66. 7. Gustilo R, Anderson J. Prevention of infection in the treatment of one thousand and twenty-five open fractures of
long bones. J Bone Joint Surg Am 1976;58: 453-8. 8. Lima ALLM, Zumiotti AV, Uip DE, Silva JS. Fatores preditivos de infecção em 9. pacientes com fraturas expostas nos membros inferiores. Acta Ortop Bras 2004;12(1):32-9. 10. Brause BD. Infections with Prostheses in Bonés and Joints. In: Mandell GL, Bennett JE, Dolin R. Principles and
Practice of Infectious Diseases. 6th Ed. Phyladelphia: Churchill Livingstone; 2005:1332-7. 11. Ehrlich GD, Stoodley P, Kathju S, Zhao Y, McLeod BR, Balaban N et al. Engineering Approaches for the
Detection and Control of Orthopaedic Biofilm Infections. Clin Orthop Relat Res 2005;437:59–66. 12. Scales J F, Herschell W. Perspex (methylmethacrylate) in orthopaedics. Brit Med J 1945;2:245-9. 13. Judet J, Judet R. Use of artificial femoral head for arthroplasty of hip joint. J Bone Joint Surg (Br) 1950;32:166-
71. 14. Petty W. The effect of methylmethacrylate on bacterial inhibiting properties of normal human serum. Clin
Orthop 1978;132:266-77. 15. Petty W. The effect of methylmethacrylate on bacterial phagocytosis and killing by human polymorphonuclear
leukocytes. J Bone Joint Surg Am 1978;60:752-7. 16. 15. Gristina A G. Biomaterial-centered infection; microbial adhesion versus tissue integration. Science
1987;237:1588-95. 17. Van de Belt H, Neut D, Schenk W, van Horn JR, van der Mei HC, Busscher HJ. Infection of orthopedic implants
and the use of antibiotic-loaded bone cements. Acta Orthop Scand 2001;72(6):557–71. 18. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA ET el. The Microbiology of chronic
osteomyelitis: Prevalence of resistance to common empirical anti-microbial regimes. J Infect 2010;60:338-43. 19. Tice AD, Pamela A, Hoaglund PA, Shoultz DA. Outcomes of osteomyelitis among patients treated with
outpatient parenteral antimicrobial therapy. Am J Med 2003;114:723-8.
20. Donlan RM, Costerton JW. Biofilms: Survival Mechanisms of Clinically Relevant Microorganisms. Clin Microbiol Rev 2002;15(2):167–93.
21. 20. Dunne Jr WM. Bacterial Adhesion: Seen Any Good Biofilms Lately? Clin Microbiol Rev 2002;15(2):155–66.
22. Zimmerli W, Trampuz A, Ochsner PE. Prosthetic-Joint Infections. N Engl J Med 2004;351:1645-54. 23. Darley ESR, MacGowan AP. Antibiotic treatment of Gram-positive bone and joint infections. JAC 2004;53:928–
35. 24. Zuluaga AF, Galvis W, Jaimes F, Vesga O. Lack of microbiological concordance between bone and non-bone
specimens in chronic osteomyelitis: an observational study. BMC Infectious Diseases 2002:1-7. [citado ano mês dia]. Disponível em: URL: http://www.biomedcentral.com/1471-2334/2/8.
25. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in Long Bones. J Bone Joint Surg 2004;86(10):2305-18.
4. Resultados
Artigo 1
Archives of Orthopaedic and Trauma Surgery Outcome and Risk Factors for Polymicrobial Posttraumatic Osteomyelitis
--Manuscript Draft--
Manuscript Number: AOTS-D-16-01127
Full Title: Outcome and Risk Factors for Polymicrobial Posttraumatic Osteomyelitis
Article Type: Original Article
Section/Category: Orthopaedic Surgery
Keywords: Chronic osteomyelitis; polymicrobial; monomicrobial; trauma; risk factors; Staphylococcus aureus.
Corresponding Author: Mauro Jose Salles, M.D., MSc, Ph.D. Faculdade de Ciencias Medicas da Santa Casa de Sao Paulo BRAZIL
Corresponding Author Secondary Information:
Corresponding Author's Institution: Faculdade de Ciencias Medicas da Santa Casa de Sao Paulo
Corresponding Author's Secondary Institution:
First Author: Luciana Souza Jorge, M.D., MSc.
First Author Secondary Information:
Order of Authors: Luciana Souza Jorge, M.D., MSc.
Alceu G Chueire, M.D., MSc, PhD
Patricia S Fucuta, M.D., MSc., PhD
Maria Gabriele Oliveira, M.D.
Marcelo A Nakazone, M.D.
Mauro Jose Salles, M.D., MSc, Ph.D.
Order of Authors Secondary Information:
Funding Information:
Abstract: Purpose: We hypothesized that polymicrobial posttraumatic osteomyelitis (PMO) may be associated with worse outcome when compared to monomicrobial posttraumatic osteomyelitis (PTO). We therefore, attempted to show the outcome and predisposing factors associated to PMO. Methods: A single-center prospective cohort study was carried out from August 2007 to 2012. Outcome variables analyzed were extra need for surgical and antibiotic treatments, higher rates of amputation and mortality associated to infection. Univariate and multivariable analyses using multiple logistic regression were performed to identify risk factors associated to PMO, and p < 0.05 was considered significant. Results: Among 193 patients PTO was diagnosed in 37.8%. Compared to monomicrobial osteomyelitis, PMO was significantly associated with supplementary surgical debridement (56.1% vs. 31%; p < 0.01) and higher consumption of antibiotics; and more amputations (6.5% vs 1.3%; p < 0.01. Factors associated to PMO in the multivariable analysis were older age (odds ratio [OR] = 1.02, 95% confidence interval [CI] = 1.01 to 1.03, p = 0.04), farmers (OR = 2.86, 95% CI = 1.05 to 7.79, p = 0.04), open fracture Gustilo type III (OR = 2.38, 95% CI = 1.02 to 5.56, p = 0.04), need for blood transfusion (OR = 2.15, 95% CI = 1.07 to 4.32, p = 0.03), and need for supplementary debridement (OR = 2.58, 95% CI = 1.29 to 5.16, p = 0.01). Conclusions: PTO is polymicrobial in more than one-third of patients, and is associated with extra surgical and clinical treatment, and worse outcome including higher rates of amputation.
Powered by Editorial Manager® and ProduXion Manager® from Aries Systems Corporation
Osteomielie Pós-traumática: Evolução e Fatores de Risco na Infecção Polimicrobiana
Abstract
Proposta: Osteomielite pós-traumática polimicrobiana (OPM) pode estar associada com
pior evolução quando comparada com osteomielite pós-traumática monomicrobiana
(OMM). O estudo presente mostrou a evolução e os fatores predisponentes para OPM.
Métodos: Um estudo de coorte retrospectivo e longitudinal em um único centro, foi
realizado de agosto de 2007 a agosto de 2012. Variáveis de desfecho analisadas foram a
necessidade de terapia cirúrgica e antimicrobiana adicional, taxas mais elevadas de
amputação e mortalidade associada à infecção. Análises univariada e multivariada usando
regressão logística foram realizadas para identificar fatores de risco associados com
OPM, e p < 0,05 foi considerado significante.
Resultados: Dos 193 pacientes, osteomielite pós-traumática (OPT) foi diagnosticado em
37,8%. Comparativamente à OMM, OPM foi significantemente associada com
desbridamento cirúrgico suplementar (56,1% vs. 31%; p < 0,01) e alto consumo de
antimicrobianos; amputações (6,5% vs 1,3%; p < 0,01). Fatores associados com OPM na
análise multivariada foram idade avançada (odds ratio [OR] = 1,.02, intervalo de
confiança (IC) de 95% = 1,01 a 1,03, p = 0,04), ocupação na agricultura (OR = 2,86, IC
95% = 1,05 a 7,79, p = 0,04), fratura exposta grau III de Gustilo (OR = 2,38, IC 95% =
1,02 a 5,56, p = 0,04), necessidade de transfusão intra-operatória de concentrado de
hemácias (OR = 2,15, IC 95% = 1,07 a 4,32, p = 0,03), e necessidade de desbridamento
cirúrgico adicional (OR = 2,58, IC 95% = 1,29 a 5,16, p = 0,01).
Conclusões: OPT é polimicrobiana em mais de um terço dos pacientes, e está associada
ao tratamento clínico e cirúrgico suplementar, e com pior evolução, incluindo taxas mais
elevadas de amputação.
PALAVRAS-CHAVE: Osteomielite crônica; polimicrobiana; monomicrobiana; trauma;
fatores de risco; Staphylococcus aureus.
Introdução Osteomielite pós-traumática (OPT) tem sido diagnosticado frequentemente e especialmente nas
populações de países de baixa e média, nos quais as taxas de trauma associado à queda, auto-
mutilação, violência interpessoal e acidentes de tráfego estão em ascensão [1]. Apesar do início
precoce da terapia antimicrobiana sistêmica após o trauma, infecção associada à fratura exposta
pode ser ocorrer de forma precoce ou tardiamente após o procedimento cirúrgico, dependendo da
complexidade e da gravidade da lesão óssea e de partes moles [2-4]. Infelizmente, poucas
publicações a respeito da epidemiologia e do desfecho clínico após infecção óssea e de partes
moles pós-traumas não fatais são encontradas, embora o custo médio de tratamento clínico e
cirúrgico combinado para OPT seja estimado em US$15,000 [5]. Em estudo retrospectivo de centro
único, infecção de sítio cirúrgico (ISC) precoce após tratamento de trauma foi o único fator de risco na
análise multivariada associada à readmissão hospital em 30 dias [6].
Inoculação de micro-organismos no osso pode acontecer logo após o trauma, pela contaminação
de partes moles adjacentes ou mesmo no pré-operatório ou durante o procedimento ortopédico [7-
9]. Vinte por cento das osteomielites pós-traumáticas polimicrobianas (OPM) foram descritas
previamente em poucas séries de casos [2-3]. Yano MH et al descreveram 20,8% de infecção
polimicrobiana associada à osteossíntese após trauma e procedimentos ortopédicos em população
brasileira jovem (principalmente acidentes de moto) [2]. Similarmente, em um estudo chinês
retrospectivo sobre osteomielite crônica de difícil tratamento, 66,5% das infecções foram
secundárias a trauma, com OPM em, pelo menos, 20% dos casos [3]. Além disso, estudo de
coorte histórico populacional realizado nos Estados Unidos identificou 35% de OPM de foco
contíguo após trauma ou cirurgia [10].
Fatores predisponentes para OPT foram classicamente divididos em aqueles relacionados ao
paciente (idade avançada e comorbidades, incluindo diabetes mellitus, obesidade, desnutrição,
malignidades e tabagismo), relacionados ao trauma (grau de energia, gravidade de lesão de partes
moles, contaminação da ferida e complexidade da fratura), e relacionados à cirurgia (intervalo
entre trauma e cirurgia, duração da cirurgia, necessidade de transfusão intra-operatória de
concentrado de hemácias, e terapia antimicrobiana empírica) [11-13]. Além disso, fatores
relacionados aos micro-organismos, incluindo a presença de múltiplos patógenos isolados no
osso e em partes moles, devem ser avaliados em estudos clínicos. Para conhecimento, poucos
estudos descritivos mostraram taxa de incidência de OPM de 20% a 35% sem a descrição de
fatores de risco específicos e do desfecho da OPM [2-3, 10- 11]. Portanto, o presente estudo sugere
que OPM pode estar associada a uma evolução desfavorável quando comparado com osteomielite
pós-traumática monomicrobiana (OMM), incluindo a necessidade de procedimentos ortopédicos
adicionais, prescrição de antimicrobianos de amplo espectro, maior número de amputações e
taxas de mortalidade mais elevadas, além de tentar identificar fatores de risco predisponentes para
infecção profunda polimicrobiana após Identificação dos fatores de risco pode auxiliar a
padronizar medidas de controle eficientes e custo-efetivas a fim de reduzir a frequência da OPM.
Pacientes e Métodos
DelineamentodoEstudo
Estudo de coorte retrospectivo, observacional e longitudinal, de centro único foi realizado de
agosto de 2007 a agosto de 2012, com 193 pacientes portadores de osteomielite após cirurgia
ortopédica para correção de fraturas fechadas e expostas. Realizado no Serviço de Ortopedia e
Traumatologia do Hospital de Base, um hospital de ensino, público e terciário localizado em São
José do Rio Preto, São Paulo, Brasil. O estudo incluiu pacientes que assinaram consentimento
informado prévio para inclusão, com idade superior a 12 anos e com, pelo menos, um ano de
seguimento após procedimento cirúrgico. Protocolo ortopédico padronizado para fratura exposta
e fechada sugere fixação externa para estabilização óssea nas fraturas expostas grau II e III de
Gustilo e fixação interna com placa, pino, parafuso ou haste intramedular, respectivamente.
Sujeitos nos quais o procedimento cirúrgico ortopédico fora realizado primariamente em outro
hospital, com prontuário médico indisponível, seguimento médico menor do que 12 meses, com
amputação pós-traumática imediata e história prévia de OPT foram excluídos. O estudo foi
revisado e aprovado pelo Comitê de Ética local.
Identificaçãodeosteomielitepós-traumática(OPT)
Osteomielite pós-traumática foi definida de acordo com os critérios dos Centers for Diseases
Control and Prevention (CDC)/National Healthcare Safety Network (NHSN), em que, pelo
menos, um dos critérios esteve presente: qualquer crescimento de micro-organismo proveniente
de cultura óssea e de partes moles; evidência de osteomielite em exame anatômico ou
histopatológico; e, pelo menos, dois dos seguintes sinais e sintomas de inflamação: febre
(>38.0°C), edema, dor, calor, secreção e deiscência ou cicatrização incompleta da ferida, com
exposição óssea ou da osteosssíntese; e, pelo menos, um dos seguintes: a) micro-organismos
identificados de cultura de sangue ou por outros testes microbiológicos em um paciente com
exame de imagem sugestiva de infecção; b) exame de imagem sugestiva de infecção [14].
Osteomielite aguda foi definida quando o diagnóstico foi realizado, pelo menos, 30 dias após
cirurgia para fratura [15]. Diagnóstico de OPM foi realizado quando cultura óssea ou de partes moles
identificou, pelo menos, dois micro-organismos diferentes. Micro-organismos de baixa virulência, tais
como, estafilococos coagulase-negativo (ECN), foram considerados infectantes quando a mesma bactéria
foi isolada em, pelo menos, duas amostras teciduais diferentes e quando, pelo menos, um critério adicional
para OPT foi também preenchido.
Potenciaisfatoresderisco
Variáveis associadas ao paciente, trauma e cirurgia foram identificadas pela revisão dos registros
médicos, intra-operatórios e microbiológicos, a fim de identificar fatores de risco em potencial
para OPM. Variáveis demográficas (idade, gênero, ocupação, nível educacional), comorbidades
(tabagismo, alcoolismo e diabete), e a classificação da American Society of Anesthesiologists
(ASA) foram avaliadas. Variáveis associadas ao trauma foram intervalo entre admissão e a
primeira dose do antimicrobiano e entre a cirurgia, local anatômico da fratura, mecanismo do
trauma em relação ao baixo grau de energia (queda da própria altura) ou alta energia (acidentes
de carro, motocicleta ou bicicleta) ou também queda de altura menor que um metro), e a
classificação de Gustilo para fratura exposta. Fatores relacionados à cirurgia foram tipo de cirurgia
(redução aberta e fixação interna ou fixação externa temporária em dois tempos), duração de
cirurgia, e necessidade de transfusão intra-operatória de hemácias. Além disso, a necessidade de
desbridamento cirúrgico suplementar para ferida cirúrgica infectada também foi avaliada.
Coletadasamostrasemicrobiologia
No centro cirúrgico, pelo menos, três amostras de tecido provenientes do osso e de partes moles
infectadas foram coletadas após desbridamento cirúrgico e então processadas para microbiologia
e histopatologia. Tecido sofreu homogeneização em 3 ml de caldo de meio de “brain-heart infusion”
BHI) por 1 minuto e foi inoculado em agar sangue de carneiro aeróbico, agar chocolate e agar
sangue anaeróbico, e em caldo de Tioglicolato (BD Diagnostic Systems, Sparks, MD). O limite
de tempo para processamento das amostras foi de 6 horas. Placas aeróbica e anaeróbica foram
incubadas de forma aeróbica a 35° - 37°C em 5 a 7% CO2 por 7 dias e anaerobicamente a 37°C
por 14 dias, respectivamente. Além disso, 0,5 ml de tecido homogeneizado foi inoculado em
caldo de Tioglicolato, incubado por 14 dias, e o caldo de Tioglicolato turvo foi cultivado
novamente em placas de Agar sangue. Colônias de micro-organismos que cresceram nas placas
foram identificadas e suscetibilidade aos antimicrobianos foi testada de acordo com as técnicas
microbiológicas padronizadas.
Análiseestatística
Para análise estatística, a amostra global e os grupos nomeados como OMM e OPM foram
descritos como média e porcentagem para variável qualitativa, e mediana e desvio padrão (DP)
para variável quantitativa. A associação entre as variáveis qualitativas foi realizada pelo teste qui-
quadrado e pelo teste exato de Fisher. Para associações entre variáveis quantitativas, regressão
logística foi utilizada. Estimativas de risco foram calculadas para variáveis associadas com
fatores de risco para OPM e reportadas como odds ratio com intervalo de confiança (IC) 95%.
Regressão logística foi utilizada para selecionar variáveis quando os níveis de significância forma
menores que 0,20 (p < 0,20) e que permaneceram, no modelo final, somente as variáveis com
nível de significância menor que 0,5 (p < 0,05). Programa da Versão Epi-Info® 3.22 com
tabulação dos dados e versão SPSS 20.0 (SPSS, Chicago, IL, USA) foram usados para análise
estatística.
Resultados Populaçãodoestudoeaspectosdotrauma
No período de estudo de 2007-2012, 205 pacientes com OPT foram incluídos, dos quais 12
(5,9%) sujeitos foram excluídos devido à história prévia de OPT (7), ou por informação médica
incompleta (5). Assim, 193 OPT foram analisadas, em que 110 (57%) e 73 (37,8%) apresentaram
MMO e OPM, respectivamente. Osteomielite com cultura negativa foi detectada em 10 (5,2%)
pacientes e foram incluídas na descrição clínica e epidemiológica. Em geral, a taxa de OPT foi
2,5%. Idade média dos pacientes foi 50 (± 16-88) anos e 68,9% eram homens, e 34,7% tinham
baixo nível educacional (nível de escolaridade <8 anos). Tanto quanto 30% dos pacientes
referiram tabagismo, 22,8% e 30,5% trabalhavam em construções e atividades domésticas,
respectivamente. Trauma de alta energia por acidente de tráfego ocorreu na maioria (57%) da
população do estudo, e consequentemente, fratura de fêmur (30,5%) e tíbia (29%) foi mais
freqüente. Além disso, 9,3% dos pacientes submetidos à estabilização da fratura apresentaram
classificação ASA maior que II, e 34,2% receberam transfusão intra-operatória de concentrado de
hemácias. Fraturas expostas tipo II e III de Gustilo foram diagnosticadas em 11,9% e 18,6% dos
pacientes, respectivamente. As características clínicas e as comorbidades são relatadas na Tabela
1.
Desfecho clínico e potenciais fatores de risco para osteomielite pós-traumática polimicrobiana(OPM)
Comparativamente à OMM, OPM foi significantemente associada com desbridamento cirúrgico
adicional (31,0% vs. 56,1; p < 0,001) e maior consumo de antimicrobianos de amplo espectro,
incluindo quinolonas (39,7% vs. 24,3; p = 0,029), cefalosporinas (21,9% vs. 4,9; p < 0,001),
carbapenens (31,5% vs. 3,9; p < 0,001) e glicopeptídeos (49,3% vs. 27,2; p = 0,003). OPM e
amputações foram estatisticamente significantes (6,5% vs 1,3%; p < 0,001) com OR = 11,5 ( IC
95% = 1,3-96,1). A taxa de sobrevida acumulativa em 2 anos das OPM e OMM foi 84,5% e
91,8%, respectivamente (p = 0,115) (Fig. 1). Oitenta óbitos foram decorrentes de OPM e um de
OMM.
Fig 1 Curva de Kaplan-Meier para taxa acumulativa de sobrevida sem diferenças na taxa de sobrevida em dois anos entre osteomielite monomicrobiana (OMM) e osteomielite polimicrobiana (OPM).
Fatores relacionados ao paciente, trauma e cirurgia investigados para possível associação com
risco aumentado para OPM em análise univariada são descritos na Tabela 2. Gênero,
comorbidades, tais como tabagismo ou imunossupressão, politrauma, intervalo entre admissão e
primeira dose do antimicrobiano e em relação à cirurgia, hiperglicemia intra-operatória,
prescrição apropriada de antimicrobiano e momento de início da profilaxia, intervalo entre
trauma e cirurgia, e escolha do primeiro procedimento cirúrgico (fixação interna ou externa) não
aumentaram o risco de OPM.
Variáveis que mostraram significância estatística e importância clínica na análise univariada
foram adicionadas ao modelo multivariado (tabela 3). Fatores predisponentes associados à OPM
na análise multivariada foram idade avançada (OR = 1,02, IC 95% = 1,01 – 1,03, p = 0,040),
fratura exposta Gustilo tipo III (OR = 2,38, IC 95% = 1,02 – 5,56, p = 0,044), necessidade de
transfusão intra-operatória de concentrado de hemácias (OR = 2,15, IC 95% = 1,07 – 4,32, p =
0,031), ocupação na agricultura (OR = 2,86, IC 95% = 1,05 – 7,79, p = 0,040) e necessidade de
desbridamento cirúrgico suplementar (OR = 2,58, IC 95% = 1,29 – 5,16, p = 0,007).
Identificaçãomicrobiana
Diagnóstico microbiológico da OPT a partir das culturas ósseas e de partes moles intra-operatórias
identificaram bácterias em94,8%. Culturas isolaram bacilos Gram-negativos (BGN) e cocos Gram-
positivos (CGP) em 51,8% e 48,2%, respectivamente. Não obstante, 34,7% (104/300) de todos os
micro-organismos cultivados nas 183 OPT foram Staphylococcus aureus, dos quais 12,3% (37/300) e
22,3% (67/300) foram S. aureus resistentes à meticilina (MRSA) e S. aureus sensíveis à meticilina
(MSSA), respectivamente. Culturas isolaram ECN em somente 6,3% (19/300). Os três principais
BG) identificados foram Pseudomonas aeruginosa (10,3%), Acinetobacter baumannii (7,6%), e
Citrobacter sp. (7%). Além disso, as culturas teciduais identificaram Candida tropicalis em dois
pacientes com OPT. Tabela 4 mostra a frequência dos micro-organismos isolados nas culturas
ósseas e de tecido de partes moles entre pacientes com OPM e OMM.
Discussão
A epidemiologia atual da osteomielite nos países desenvolvidos parece estar associada
principalmente à idade avançada e a doenças crônicas não controladas, incluindo insufuciência
vascular periférica e diabete melito [10, 16]. Por outro lado, nos países em desenvolvimento, tais
como China e Brasil, a doença afeta adultos mais jovens, previamente saudáveis e
economicamente ativos, devido a todo tipo de trauma, incluindo acidentes de tráfego, quedas e
violência interpessoal [1-3]. Taxa de OPT após fixação interna para estabilização óssea de fratura
fechada deveria ser baixa, enquanto, na fratura exposta, a taxa de infecção pode ser tão alta
quanto 50% [7-8]. Nessa circunstância, a OPM pode atingir ainda taxas mais elevadas,
dependendo da complexidade e do local da fratura, e do grau de contaminação de partes moles no
período pré-operatório e durante o procedimento cirúrgico [2, 3, 9, 17-18].
Assim, um estudo de coorte retorspectivo de cinco anos em um hospital brasileiro terciário,
referência em trauma, foi realizado, e OPT foi diagnosticada em somente 2,5%, mas OPM
correspondeu a 37,8%. Esses resultados alarmantes tentam esclarecer o desfecho e a
epidemiologia da OPM, e gerar consequentemente estratégias eficientes de tratamento e
prevenção. Além disso, para melhor entendimento, nenhum estudo avaliou fatores predisponentes
para OPM pós-traumática. O presente estudo sugeriu a presença de diferenças a respeito das
condutas clínicas e cirúrgicas, taxas de amputação, e a taxa de sobrevida livre de doença
acumulativa de dois anos entre OPM e OMM. De fato, OPM esteve estatisticamente associada
com procedimentos ortopédicos adicionais para desbridamento ósseo e de partes moles além da
maior prescrição de antimicrobianos de amplo espectro, incluindo terapia combinada.
Infelizmente, dados sobre desfecho e fatores de risco para OPM são escassos. Poucas séries de
casos associadas à OPM entre pacientes com doença crônica não controlada (diabete melito)
mostraram desfecho pior e falência de tratamento [10, 19]. Além disso, taxa mais alta de
amputação foi estatisticamente associada com OPM, com OR de 11,5 (IC 95 % = 1,3-96,1). O
presente estudo avaliou se a presença de tecido ósseo e de partes moles desvitalizado após fratura
fechada e exposta, com contaminação local por um inóculo com múltiplas espécies de micro-
organismos pudesse potencializar a resposta inflamatória sistêmica e local, e influenciar a taxa de
amputação. Entretanto, a taxa de sobrevida acumulativa de dois anos dos casos de OPM e OMM
foi similar.
Vários fatores de risco independentemente associados com OPM foram identificados no presente
estudo. Idade avançada, profissionais da agricultura que apresentaram fratura exposta de Gustilo
III complexa de membro inferior, necessidade de transfusão de concentrado de hemácias no intra-
operatório e necessidade de desbridamento cirúrgico adicional foram associados
significantemente com OPM na análise multivariada. De modo interessante, a agricultura como
ocupação mostrou um risco potente de 2,86 vezes maior para OPM, atingindo significância
estatística na análise multivariada. Mir et al. mostraram previamente forte associação entre lesões
agrícolas expostas de extremidade inferior e OPM (18,7%), das quais 37,5% foram infecção
polimicrobiana [20]. Fratura exposta Gustilo grau III de membro inferior é potencialmente fatal, e
a inoculação dos micro-organismos no osso ocorre comumente logo após trauma, decorrente da
contaminação de partes moles, ou durante cirurgia [7-9]. Presença de transfusão de concentrado
de hemácias no intra-operatório mostrou risco de 2,15 vezes na aquisição de OPM. Necessidade
de transfusão de concentrado de hemácias no intra-operatório pode refletir a gravidade do trauma
por si só, com extensa lesão de partes moles e sangramento importante devido ao trauma de alta
energia. Investigações prévias evidenciaram aumento no risco para infecção bacteriana após
transfusão de concentrado globular, possivelmente em decorrência do efeito imunomodulador da
transfusão [21]. Em estudo de coorte retrospectivo em pacientes submetidos à correção de fratura de
quadril, transfusão de concentrado de hemácias foi associada a um risco de 35% e 52% maior
pata infecção bacteriana grave e pneumonia, respectivamente [22].
O espectro de micro-organismos isolados em amostras de osso e de partes moles de pacientes
com OPT foi diferente de outros relatos [23-24]. De fato, achados microbiológicos do presente
estudo adicionaram nova informação à epidemiologia da OPT, pois BGN foi discretamente mais
prevalente que CGP (51,8% vs. 48,2%, respectivamente). Dos BGN, P. aeruginosa (10,3%) e A.
baumannii (7,6%) foram os mais comuns. Esses micro-organismos foram frequentemente
associados com OPT, principalmente na osteomielite crônica de tíbia após trauma de alta energia,
tais como, fraturas associadas a acidente de moto e a episódios de guerra [23-25]. Diante desse
resultado intrigante, esse estudo também avaliou se o uso prévio e prolongado de antibióticos de
amplo espectro, tais como cefalosporinas ou quinolonas, possa ter impacto na alta freqüência de
OPT por BGN. S. aureus foi o micro-organismo mais comumente isolado (34,7%), apesar da sua
taxa de positividade ser consideravelmente inferior a outros estudos de OPT [24]. Apesar disso,
estafilococos permanece um micro-organismo importante na patogênese da infecção pós-
traumática devido à sua habilidade incrível de colonizar a pele, invadir tecidos profundos e de
sobreviver no interior de osteoblastos, produzindo biofilme [26-27]. Somente um terço das culturas
positivas de S. aureus no presente estudo foram cepas resistentes à meticilina, e foi considerado de baixa
incidência devido à alta freqüência em muitos hospitais da América Latina [3, 28]. Estafilococos
coagulase-negativo (ECN) correspondeu somente a 6,3% dos resultados. Esses achados podem
refletir o fato de que, entre os casos em que osteossíntese foi enviada para cultura, sonicação
nunca foi realizada.
O presente estudo tem limitações em potencial. Primeiramente, o estudo foi realizado em um
único hospital de ensino, localizado em uma cidade de tamanho médio de um país em
desenvolvimento (São José do Rio Preto), que oferece um centro especializado em cuidados
ortopédicos para a população regional, mas os resultados não podem ser aplicados para outros
hospitais. Entretanto, um banco de dados de um grande centro de casos de trauma, que foram
submetidos a procedimento ortopédico, foi comparado (aproximadamente 8.000). O fato do
presente estudo ser coorte prospectiva elimina assim os viés de seleção e de memória que
limitariam a realização da análise multivariada para muitas associações importantes com OPT.
Outra limitação foi a dificuldade em realizar o diagnóstico clínico da OPT, em que os sinais e
sintomas típicos de inflamação possam estar ausentes, principalmente nas infecções associadas a
osteossíntese, além do fato de que os marcadores inflamatórios séricos não são úteis e os exames
de imagem são inespecíficos [14-15]. Além disso, sonicação dos implantes recuperados
(parafusos e placas) para identificação de micro-organismos não foi realizada, influenciando
provavelmente assim o número total dos casos estudados de OPM [2].
Conclusões
Esse estudo de coorte retrospectivo de cinco anos concluiu que a OPM foi identificada em mais
de um terço dos casos. Pacientes idosos, agricultura como ocupação, fratura exposta tipo III de
Gustilo, desbridamento cirúrgico suplementar e transfusão de concentrado de hemácias no intra-
operatório foram fatores independentemente associados com OPM na análise multivariada.
Culturas identificaram principalmente bacilos Gram-negativos, mas S. aureus permanece o
principal micro-organismo isolado. Certamente, a identificação dos fatores predisponentes para
OPM pode auxiliar na escolha da terapia antimicrobiana mais apropriada e na modalidade
cirúrgica mais segura. Estudos adicionais sobre OPT devem ser realizados para confirmar os
resultados desse estudo.
Acknowledgments
Agradecemos ao Serviço de Ortopedia e Traumatologia do Hospital de Base de São José
do Rio Preto por permitir a pesquisa dos arquivos do paciente e a Patricia Fucuta por seu apoio na
análise estatística.
Tabela 1. Características demográficas e do trauma de 193 pacientes com osteomielite pós-traumática (OPTa). Dados demográficos N=193 (%)
Idade (mediana [variação]) (anos) 50 (16-88) Sexo masculino (no. [%]) 133 (68,9) Nível de escolaridade <8 anos 67 (34,7) Comorbidades (no. [%])
Alcoolismo 35 (18,1) Tabagismo 59 (30,5) Hiperglicemia intra-operatória 58 (30,0)
Ocupação (no. [%]) Agricultura 26 (13,5) Condução (carro, moto, caminhão) 24 (12,5) Construção / Operação de Máquina 44 (22,8) Negócios 40 (20,7) Atividades domésticas 59 (30,5)
Tipos de acidente (no. [%]) Acidente automobilístico 110 (57,0) Queda da própia altura (< 1m) 57 (29,5) Trauma relacionado ao futebol 3 (1,5) Queda de escada 13 (7,0) Queda do cavalo 5 (2,6) Acidente por arma de fogo 2 (1,0) Trauma penetrante com Madeira 3 (1,5)
Trauma de alta energia 133 (68,9) Classificação de Gustilo & Anderson para fratura exposta fractures
73 (37,8) Tipo-I (no. [%]) 14 (19,2) Tipo -II (no. [%]) 23 (31,5) Tipo -III (no. [%]) 36 (49,3)
Fratura fechada 120 (62,1) >1 desbridamento cirúrgico 77 (39,9) Politrauma 46 (23,8) Escore da American Society of Anesthesiologists (no. [%])
ASAb I – II (1 ou 2)
166 (90,7) ASAb III – IV (>2) 17 (9,3)
Transfusão intra-operatória de concentrado de hemácias 66 (34,2) Duração da cirurgia (média [variação]) (horas) 2,61 (1-8) Sítio de Fratura infectado (no. [%])
Membro Superior 44 (22,8) Membro Inferior 154 (79,2) Clavícula 7 (3,6) Úmero 12 (6,2) Rádio 13 (6,7) Ulna 16 (8,2) Mãos 3 (1,5) Fêmur 59 (30,5) Joelho 9 (4,6) Tíbia 56 (29) Fíbula 11 (5,7) Pés 19 (9,8)
a OPT- osteomielite pós-traumática; b ASA-Escore da American Society of Anesthesiologists.
Tabela 2. Análise univariada de fatores de risco associados com osteomielite polimicrobiana (OPMa) e osteomielite monomicrobiana (OMMb) após trauma entre 183c pacientes. Características MMOa
Pacientes OPMb Valor Pd
No. (%) No. (%) (N = 110) (N = 73) Dados demográficos
Idade (mediana [variação]) (anos) 40,5 (11 – 87) 50 (16 – 88) 0,017 Sexo masculino (no. [%]) 76 (69,0) 53 (72,6) 0,610 Nível de escolaridade >8 anos (no. [%]) 47 (42,7) 20 (27,3) 0,035 Agricultura (no. [%]) 9 (8,2) 16 (22,0) 0,008
Comorbidades (no. [%]) Tabagismo 33 (30,0) 26 (23,6) 0,426 Hiperglicemia intra-operatória Intraoperative hyperglycemia
29 (26,3) 27 (37,0) 0,127 Trauma de alta energia (no. [%]) 79 (71,8) 50 (68,5) 0,629 Queda da própria altura (no. [%]) 29 (26,4) 22 (30,1) 0.577 Fratura exposta Grau III (no. [%]) 15 (13,6) 21 (28,7) 0,012 Intervalo admissão - cirurgia >3h (no. [%]) 103 (93,6) 62 (85,0) 0,053 Duração cirurgia (mediana [variação]) (h) 2 (1-8) 2 (1-7) 0,738 Intervalo admissão - 1a dose antibiótico (h) 60 (54,5) 26 (23,6) 0,062 Seguimento clínico (variação) (dias) 728 (38 – 2539) 690 (22 – 2526) 0,980 >1 desbridamento cirúrgico (no. [%]) 34 (31,0) 41 (56,1) 0,001 Transfusão de hemácias (no. [%]) 26 (23,6) 38 (52,0) <0,0001 Fratura de fêmur (no. [%]) 26 (23,6) 31 (42,5) 0,007 >3 amostras de tecido ósseo (no. [%]) 59 (53,6) 51 (69,8) 0,028 >3 amostras de partes moles (no. [%]) 12 (11,0) 20 (27,4) 0,004 Escore ASA
ASA I - II (no. [%]) 102 (92,7) 64 (87,7) 0,249 ASA III - IV (no. [%]) 8 (7,3) 9 (12,3)
a OPM - osteomielite polimicrobiana; b OMM - osteomielite monomicrobiana; cDez pacientes (5,2%) foram excluídos dessa análise por apresentarem osteomielite com culturas negativas; d As características dos pacientes foram resumidas como frequência e porcentagem ou mediana e comparadas pelo teste qui-quadrado de Pearson ou pelo teste exato de Fisher para variáveis nominais e teste Mann- Whitney ou teste t para variáveis contínuas (SPSS version 19.0). Todos os testes foram pareados, e o valor P <0,05 foi considerado estatisticamente significante.
Tabela 3. Análise multivariada de fatores de risco para OPTa, entre 183 pacientesb.
Variáveis OMMa OPMb Odds Ratio Valor Pc
No. (%) No. (%) IC (95%) (N = 110) (N = 73)
Idade (mediana [variação]) (anos) 40,5 (11 – 87) 50 (16 – 88) 1,02 (1,01 – 1,03) 0,040
Transfusão de hemácias 26 (40,6%) 38 (59,4%) 2,15 (1,07 – 4,32) 0,031
Fratura exposta Gustilo Tipo-III 15 (41,7%) 21 (58,3%) 2,38 (1,02 – 5,56) 0,044
Agricultura 9 (8,2%) 16 (22,0%) 2,86 (1,05 – 7,79) 0,002
>1 desbridamento (no. [%]) 34 (31%) 41 (56,1%) 2,58 (1,29 – 5,16) 0,007
OMMa – osteomieltie monomicrobiana; OPMb – osteomielite polimicrobiana; cvalores P <0,05 foram considerados estatisticamente significantes.
Tabela 4. Frequency of microorganisms yielded from cultures of OPTa
Micro-organismos N (%) Staphylococcus aureus 104 (34,6)
Resistente à oxacilina 37 (12,3) Sensível à oxacilina 67 (22,3)
Pseudomonas aeruginosa 31 (10,3) Acinetobacter baumannii 23 (7,6) Enterococcus sp. 22 (7,3) Citrobacter sp. 21 (7,0) Klebsiella pneumoniae 20 (6,6) ECNa 19 (6,3) Escherichia coli 14 (4,6) Proteus sp. 14 (4,6) Candida tropicalis 2 (0,6) Outrosb 30 (10,0) aEstafilococos coagulase-negativo; bOutros - Alcaligenes sp., Enterobacter sp., Morganellamorganii, Providencia sp., Serratia sp., Stenotrophomonas maltophilia, Streptococcus agalactiae,Streptococcusviridans.
26
Article 1:
Posttraumatic Osteomyelitis: Outcome and Risk Factors for Polymicrobial Infection
Abstract
Introduction: Posttraumatic osteomyelitis (PTO) seems to be growing steadily in some developing countries, in
which mostly are monomicrobial caused by staphylococci species. However, polymicrobial posttraumatic osteomyelitis
(PMO) have been described following low extremities (ankle, calcaneus) fracture infections. In general, few studies have
attempted to show the outcome and predisposing factors associated to PMO. We hypothesized that PMO may be
associated with worse outcome, including additional orthopedic surgeries and increased use of broad-spectrum
antibiotics, more amputations and higher mortality rates compared to monomicrobial PTO.
Patients and Methods: Between August 2007 and August 2012, a single- center prospective cohort study was
carried out among 193 patients with PTO following orthopedic surgery. Bone and soft tissues were collected for cultures
and PTO was defined according to CDC/NHSN criteria. The outcome variables analyzed were extra need for surgical
and antibiotic treatments, higher rates of amputation and mortality associated to infection. Patient, injury, surgery-
associated variables and microbiological records were identified for potential confounders or risk factors associated to
PMO. Univariate and multivariable analyses using multiple logistic regression were performed, and p < 0.05 was
considered significant.
Results: Patients were mainly male (68.9%) with mean age of 50 (± 16-88) years. PTO was diagnosed in 37.8% (73/193)
patients. High-energy trauma due to road traffic accidents occurred in 57% of our population. Compared to
monomicrobial osteomyelitis, PMO was significantly associated with supplementary surgical debridement (56.1% vs.
31%; p < 0.01) and higher consumption of antibiotics; and more amputations (6.5% vs 1.3%; p < 0.01). The 2-year
cumulative survival rate for PMO and monomicrobial PTO was 84.5% and 91.8%, respectively. Factors associated to
PMO in the multivariable analysis were older age (odds ratio [OR] = 1.02, 95% confidence interval [CI] = 1.01 to 1.03, p
= 0.04), farmers (OR = 2.86, 95% confidence interval [CI] = 1.05 to 7.79, p = 0.04), open fracture Gustilo type III (OR =
2.38, 95% CI = 1.02 to 5.56, p = 0.04), need for intraoperative blood transfusion (OR = 2.15, 95% CI = 1.07 to 4.32, p =
0.03), and the need for supplementary surgical debridement (OR = 2.58, 95% CI = 1.29 to 5.16, p = 0.01). Gram-positive
cocci and Gram-negative bacilli were isolated in 48.2% and 51.8% of cases, respectively. The most common bacteria
detected (37.4%) was Staphylococcus aureus.
Conclusions: PTO is polymicrobial in more than one-third of patients, and is associated with extra surgical and
clinical treatment, and worse outcome including higher rates of amputation and mortality
KEYWORDS: Chronic osteomyelitis; polymicrobial; monomicrobial; trauma; injury; risk factors; Staphylococcus
aureus; Pseudomonas aeruginosa.
Introduction
Posttraumatic osteomyelitis (PTO) has been frequently diagnosed specially among the low- and middle-income
countries populations, in which the rates of injuries associated to fall, self-harm, interpersonal violence and road traffic
27
accident is still growing.1 Even with systemic antimicrobial therapy being applied early after the trauma, open fractures-
associated infections can be expected to occur early or late after surgical procedures, depending upon the complexity and
severity of soft tissues and bone damages.2-4 Unfortunately, there have been few publications addressing the
epidemiology and clinical outcomes of soft tissues and bone infections following non-fatal injuries, even though the
average cost of combined medical and surgical treatment for PTO is estimated at US$15,000.5 In a single center
retrospective study, development of surgical site infection (SSI) early after management of trauma was the only risk
factor on multivariate analysis associated with 30 days hospital readmission.6
Inoculation of microorganisms into the bone may happen soon after the trauma, either from an adjacent soft tissue
contamination or even during pre-operative and intra-operative bone surgeries.7-9 Interestingly, as much as 20% of
polymicrobial posttraumatic osteomyelitis (PMO) have been previously described in few case series.2-3 We described
20.8% of polymicrobial osteosynthesis-associated infections in a young Brazilian population following trauma (mainly
motorcycle accidents) and orthopedic surgery.2 Similarly, in a Chinese retrospective study of difficult-to-treat chronic
osteomyelitis, 66.5% of infections were secondary to trauma, in which PMO accounted for at least 20% of cases.3
Additionally, a population-based historical cohort study carried out in United States identified 35% of polymicrobial
contiguous osteomyelitis resulted from trauma or surgery.10
Predisposing factors for PTO have been classically sub-divided in patient-related (increased age, and comorbidities
including diabetes mellitus, obesity, poor nutrition, malignancy, and smoking), injury-related (grade of trauma energy,
severity of soft tissue damages, wound contamination, and complexity of fracture), and surgery-related (time period from
trauma to surgery, duration of surgery, need for blood transfusion, and empirical antibiotic therapy).11-13 Nevertheless,
microorganisms-related factors including the presence of multiple pathogens isolated on the affected bone and soft tissue
must also be addressed by clinical studied. To the best of our knowledge, few descriptive studies have previously shown
an incidence rate of PMO ranging from 20% to 35%, but none attempted to describe specific risk factors and outcome of
PMO.2-3,10,11 Therefore, we hypothesized that PMO may be associated with worse outcome when compared to
monomicrobial PTO, including the need for additional orthopedic surgeries and increased use of broad-spectrum
antibiotics, more amputations and higher mortality rates. We also aimed to identify risk factors predisposing patients to
develop polymicrobial deep infections following PTO. Identification of risk factors may help implementing efficient and
cost-saving control measures to reduce the frequency of PMO.
Patients and Methods Study Design
We performed a single-center observational cohort study of data collected prospectively from August 2007
through August 2012, with 193 subjects diagnosed with osteomyelitis following orthopedic surgery for closed and open
fractures, performed at the Orthopedics and Traumatology Unit of Hospital de Base, a tertiary public teaching hospital in
São José do Rio Preto, São Paulo, Brazil. The study included patients older than 12 years old and with at least 1 year of
follow-up after the surgical procedures. Standard orthopedic protocol for open and closed fractures is currently external
fixation for bone stabilization of Gustilo grade-II and grade-III and internal fixation with plates and screws or
intramedullary nails, respectively. Subjects in which the orthopedic surgical procedures were performed primarily in an
28
institution other than ours, the medical records were not available, with follow-up shorter than 12 months, who had
undergone amputation soon after trauma and with previous history PTO were excluded. The study was reviewed and
approved by the local Institutional Review Board.
Identification of post-traumatic osteomyelitis (PTO)
We defined PTO according to the criteria of the Center for Diseases Control and Prevention (CDC)/National
Healthcare Safety Network (NHSN) guidelines, in which at least one of the following criteria was present: any growth of
organism in bone and soft tissue culture; evidence of osteomyelitis on gross anatomic or histopathologic exam; and at
least two of the following signs and symptoms of inflammation: fever (>38.0°C), swelling, pain, redness, heat, drainage
and delayed wound closure with exposed bone or osteosynthesis; and at least one of the following: a) organisms
identified from blood by culture or non-culture based microbiologic testing method in a patient with imaging test
evidence suggestive of infection, which if equivocal is supported by clinical correlation; b) imaging test evidence
suggestive of infection, which if equivocal is supported by clinical correlation.14 Acute bone infection was defined when
diagnosis was performed at least 30 days after surgery for fracture.15 Diagnosis of PMO was made when either bone or
surrounded soft tissue cultures yielded at least two different microorganisms. Low-virulence microorganisms such as
coagulase-negative staphylococci were considered pathogens when the same organism was identified in at least two
different tissue samples and when at least one additional criterion for PTO was also fulfilled.
Potential risk factors
Patient, injury, and surgery-associated variables were identified by reviewing the medical, intra-operative, and
microbiological records for potential risk factors associated to PMO. We searched for demographic variables (age,
gender, occupational status, educational level), comorbidities (smoking, alcoholism, and diabetes), and American Society
of Anesthesiologists (ASA) classification. Injury-associated variables assessed were time elapsed from admission to the
first dose of antibiotic and to surgery, anatomical site of fracture, mechanism of trauma such as low-energy injury (fall
own height) or high-energy (car, motorcycle, or bicycle accident or even fall from a height above 1 m), and Gustilo open
fracture classification. Surgery-related factors analyzed were type of surgery procedure (open reduction and internal
fixation or two-stage temporary external fixator), duration of surgery, and the need for blood transfusion. Furthermore,
we also assessed the need to performing supplementary surgical debridement for infected wounds.
Specimen collection and microbiology
In the surgical ward, at least three tissue samples from infected bone and soft tissues were collected during surgical
debridement, and therefore processed for microbiology and histopathology. Tissue was homogenized in 3 ml of brain-
heart infusion (BHI) broth for 1 min and inoculated onto aerobic sheep blood agar, chocolate agar, and anaerobic blood
agar and into thioglycolate broth (BD Diagnostic Systems, Sparks, MD). Time limit for processing samples was 6 hours.
Aerobic and anaerobic plates were incubated aerobically at 35° to 37°C in 5 to 7% CO2 for 7 days, and anaerobically at
37°C for 14 days, respectively. Additionally, 0.5 ml of tissue homogenate was inoculated in thioglycolate broth,
incubated for 14 days and the turbid thioglycolate broth was sub-cultured on blood agar plates when cloudy. Colonies of
microorganisms growing on plates were identified and their susceptibility to antibiotics was tested according to standard
29
microbiologic techniques.
Statistical analysis
For statistical analysis, the overall sample and the groups assigned as monomicrobial and PMO were described as
mean and percentage for qualitative variables, and median and standard deviation (SD) for quantitative variables. The
association between qualitative variables was made using the chi-square test and Fisher's exact test. For associations
between quantitative variables we used bivariate logistic regression. The risk estimates were calculated on the variables
associated with risk factors for PMO and reported as an odds ratio with respect to 95% confidence interval (CI). We used
the multiple logistic regression model for by selecting the variables of bivariate analysis tests when there was
significance levels lower than 0.20 (p < 0.20) and remained in the final models only significant variables lower to 0.5 (p
< 0.05). We used the Epi-Info® Version 3.22 software with the data tabulation and SPSS version 20.0 (SPSS, Chicago,
IL, USA) for statistical analysis.
Results
Study population and aspects of trauma
During the study period of 2007-2012, we have followed 8.098 patients who had undergone orthopedic surgery, of
which 7510 (92.7%) and 588 (7.3%) for closed and open fractures, respectively. We included 205 patients with PTO, of
which 12 (5.9%) subjects were further excluded due to previous history of PTO (7), or to incomplete medical information
available (5). Therefore, one-hundred ninety-three PTO were analyzed, in which 110 (57%), and 73 (37.8%), presented
monomicrobial posttraumatic osteomyelitis (MMO) and PMO, respectively. Negative- culture osteomyelitis was
diagnosed in 10 (5.2%) patients and they were included in the clinical and epidemiological description. In general, PTO
rate during the study period was 2.5%. Patients mean age was 50 (± 16-88) years and 68.9% were male, and 34.7% had
poor educational status (schooling level <8 years). As much as 30% of patients referred smoking habits, 22.8% and
30.5% worked on constructions and household activities, respectively. Interestingly, high-energy trauma due to road
traffic accidents occurred in the majority (57%) of our study population, and consequently, femur (30.5%) and tibia
(29%) fractures were more frequently diagnosed. Besides, 9.3% of patients undergoing surgery for fracture stabilization
were assigned as having ASA grade higher than II, and 34.2% received blood transfusion during surgery. Gustilo type II
and III open fractures were diagnosed in 11.9% and 18.6% of patients, respectively. The clinical characteristics and
comorbidities are shown on table 1.
Outcome and potential risk factors for posttraumatic polymicrobial osteomyelitis (PMO)
Compared to monomicrobial osteomyelitis, PMO was significantly associated with supplementary surgical
debridement (31.0% vs. 56.1; p < 0.001) and higher consumption of broad-spectrum antibiotics including quinolones
(39.7% vs. 24.3; p = 0.029), cephalosporins (21.9% vs. 4.9; p < 0.001), carbapenems (31.5% vs. 3.9; p < 0.001) and
glycopeptides (49.3% vs. 27.2; p = 0.003). PMO and amputations was statistically significant (6.5% vs 1.3%; p < 0.001)
with an OR = 11.5 (95 % CI = 1.3-96.1). The 2-year cumulative survival rate of polymicrobial and monomicrobial PJIs
was 84.5% and 91.8%, respectively (p = 0.115) (Fig. 1). There were eight and one death resulting from polymicrobial
30
and monomicrobial PTO, respectively.
Patient, injury, and surgical factors that were investigated for possible association with an increased risk for PMO
in the univariate analysis are described in Table 2. Gender, comorbidities such as smoking or immunosuppression,
polytrauma, time elapsed from admission to the first dose of antibiotic and to surgery, intraoperative hyperglycemia,
appropriate type of antibiotic prescribed and time to initiate prophylaxis, time elapsed from trauma to surgery, and choice
of first surgical procedure (internal or external fixation) did not increase the risk of PMO.
Variables showing statistical significance and with clinical importance in univariate analysis have been added to
the multivariate model (table 3). Predisposing factors associated to PMO in the multivariable analysis were older age
(OR = 1.02, 95% CI = 1.01 - 1.03, p = 0.040), open fracture Gustilo type III (OR = 2.38, 95% CI = 1.02 - 5.56, p =
0.044), need for intraoperative blood transfusion (OR = 2.15, 95% CI = 1.07 - 4.32, p = 0.031), farmers (OR = 2.86, 95%
CI = 1.05 - 7.79, p = 0.040) and the need for supplementary surgical debridement (OR = 2.58, 95% CI = 1.29 - 5.16, p =
0.007).
Microbial identification
Microbiological diagnosis of PTO using intraoperative bone and soft tissue cultures identified bacteria in 94.8%.
Cultures yielded gram-negative bacilli (GNB) and gram- positive cocci (GPC) in 51.8% and 48.2%, respectively.
Notwithstanding, 34.7% (104/300) of all causative pathogens cultured in the 183 PTO were Staphylococcus aureus, of
which 12.3% (37/300) and 22.3% (67/300) were methicillin-resistant S. aureus (MRSA) and methicillin-sensitive S.
aureus (MSSA), respectively. Cultures yielded coagulase-negative staphylococci in only 6.3% (19/300). Three most
causative GNB identified were Pseudomonas aeruginosa (10.3%), Acinetobacter baumannii (7.6%), and Citrobacter sp.
(7%). In addition, tissue cultures yielded Candida tropicalis in two different patients with PTO. Table 4 shows the
frequencies of microorganisms isolated from bone and soft tissue cultures among patients presenting PMO and MMO.
Discussion
The current epidemiology of osteomyelitis in the developed countries population seems to be mainly associated to
older age and uncontrolled chronic diseases, including peripheral vascular insufficiency and diabetes mellitus.10,16 On the
other hand, in developing countries such as China and Brazil, the burden of the disease is affecting previously healthy,
economically active younger adults due to all sorts of trauma including transport injuries, falls, self-harm and
interpersonal violence.1-3 Rates of posttraumatic osteomyelitis (PTO) after internal fixation for bone stabilization of
closed fractures is expected to be low, whereas in open fractures the infection rates may be as high as 50%.7,8 In this
circumstance the polymicrobial PTO may also reach higher rates, depending upon the complexity of fracture, anatomical
site, and soft tissue contamination during pre-operative and intra-operative surgeries.2,3,9,17,18
Therefore, we performed a 5 years prospective cohort study of trauma care in a Brazilian tertiary hospital, in which
PTO was diagnosed in only 2.5%, but polymicrobial posttraumatic osteomyelitis (PMO) accounted for 37.8%. These
alarming results prompted us to understand the outcome and epidemiology of PMO, and consequently develop efficient
strategies of prevention and management. Moreover, to the best of our knowledge, no study has ever attempted to
31
evaluate the predisposing factors associated to PMO following trauma. We hypothesized there were differences
regarding surgical and clinical management, the rates of amputation, and the 2-year cumulative survival rate between
PMO and monomicrobial PTO. Indeed, PMO was statistically associated with additional orthopedic surgeries for bone
and soft tissues debridement and increased use of broad-spectrum antibiotics including combination therapy. It may
sound obvious, but data investigating the outcome and risk factor associated to PMO are scarce. Few previous case-series
associated polymicrobial osteomyelitis among patients with uncontrolled chronic diseases (diabetes mellitus) with worse
outcome and treatment failure.10,19 In addition, higher rates of amputations was statistically associated with PMO with an
OR of 11.5 (95 % CI = 1.3-96.1). We speculate the association between devitalized bone and soft tissue following high-
energy open or closed fractures with local contamination by a higher inoculum of multiple species of pathogenic bacteria
may increase local and systemic inflammatory response and influence the higher rates of amputations. On the other hand,
in our case series the outcome of PMO and monomicrobial PTO concerning 2-year cumulative survival rate were similar.
Several risk factors independently associated with PMO were identified in the present study. Older age,
agricultural workers presenting complex lower limb Gustilo III open fractures, requiring intra-operative blood transfusion
and upon which several debridement procedures were performed, were significantly associated with PMO in the
multivariable analysis. Interestingly, agricultural employment was found to be a potent risk of PMO, showing a 2.86-fold
higher risk of PMO, reaching statistical significance on multivariable-adjusted analysis. Mir et al., have previously
showed a stronger association of open, agricultural upper extremities injuries and PMO (18.7%), in which 37.5% were
polymicrobial infection.20 Gustilo III fractures of the lower limb are life-threatening injuries, in which inoculation of
microorganisms into the bone commonly happen soon after trauma from soft tissue contamination or during surgeries.7-9
Recipients of blood transfusion during surgery had 2.15-fold higher risk of PMO. The need for allogeneic blood
transfusion may reflect the severity of the injury itself, with extensive soft tissue damage and severe bleeding due to
high-energy trauma. Previous investigations have shown increased the risk for bacterial infection following blood
transfusion possibly associated to an immunomodulatory effect of blood transfusion.21
In a retrospective cohort study
performed among patients undergoing hip fracture repair, blood transfusion was associated with a 35% and 52% greater
risk of serious bacterial infection and pneumonia, respectively.22
The spectrum of microorganisms isolated from bone and soft tissues samples from patients with PTO was slight different
from that reported by other authors.23,24 Indeed, the microbiological findings of the present study added new information
to the epidemiology of PTO, because GNB was slight more prevalent than GPC (51.8% vs. 48.2%, respectively). Among
the GNB, Pseudomonas aeruginosa (10.3%) and Acinetobacter baumannii (7.6%) were the commonest in our results.
These organisms have been frequently associated with PTO, especially in chronic osteomyelitis of tibia following high-
energy injuries, such as motorcycle accidents and combat-associated fractures.23-25 Upon this intriguing result, we also
speculated if previous use of broad-spectrum systemic antibiotics such as cephalosporin or quinolones during prolonged
course of therapy might also have had some impact on the high frequency of GNB-PTO. Staphylococcus aureus was still
the most commonly isolated pathogen in our cases (34.7%) even though, we have noticed a considerably lower yield
compared to other PTO series.25 Despite of that, staphylococci will continue to play a major role on the pathogenesis of
32
posttraumatic infection due to its incredible ability not only colonize skin and invade deep tissues, but also to survive
intracellularly into osteoblasts and forming biofilm.26,27 Only one-third of our positive cultures yielding S. aureus were
MRSA strains, which was considered a low incidence due to its high frequency within many Latin America hospitals.3,28
Coagulase-negative staphylococci (CoNS) only accounted for 6.3% of our results. These findings may reflect the fact
that among our PTO cases in which osteosynthesis were retrieved for cultures, sonication was never performed.
We are aware that our study has potential limitations. First, the study was carried out at a single, large urban public
teaching center located in developing country medium-size city (São Jose do Rio Preto) which offers a specialized
orthopedic care for the local population, b/ut the results may not be applicable to other hospitals. However, we used a
large single-center database of trauma cases (roughly 8,000) who had undergone orthopedic surgeries. A notable strength
is the nature of our prospective cohort study, thus eliminating selection and recall bias that would limit the performance
of multivariable-adjusted analysis to many important associations with PTO. Another limitation was difficulties in
performing the clinical diagnosis of PTO, in which typical signs and symptoms of inflammation may be absent,
especially for osteosynthesis-associated infections, in which inflammatory blood markers are usually unhelpful, and
imaging tests are nonspecific.14,15 Furthermore, sonication on the retrieved implants (screws and plates) for the
identification of sessile microorganisms was not performed, thus probably influencing the total number of PMO cases
studied.2
Conclusions
This prospective cohort study over five years concluded that posttraumatic polymicrobial osteomyelitis (PTO)
were identified in more than one-third of the cases. Older patients, farmers, Gustilo III open fracture, supplementary
surgical debridement, and blood transfusion during surgery were independently associated with PMO in multivariable
analysis. Cultures yielded mostly Gram-negative bacilli, but S. aureus remains the leading pathogen isolated. Surely,
identifying predisposing factors for PMO may help physicians to choose the most appropriate antibiotic therapy and the
safest surgical modality. Further studies addressing PTO should be encouraged in order to confirm our results.
33
Table 1. Demographic and injury characteristics of 193 patients presenting posttraumatic osteomyelitis (PTOa).
Demographic data N=193 (%) Age (mean [range]) (years) 50 (16-88) Male sex(no. [%]) 133 (68.9) Schooling level <8 years 67 (34.7) Comorbidities (no. [%]) Alcohol abuse 35 (18.1) Smoking 59 (30.5) Intraoperative hyperglycemia 58 (30.0) Occupation (no. [%]) ü Farmer 26 (13.5) ü Driver (car, motorcycle, truck) 24 (12.5) ü Construction / Machine Operation 44 (22.8 ) ü Business 40 (20.7) Household activities 59 (30.5) Types of injury (no. [%]) Car chash accident 110 (57.0) Fall from height (< 1m) 57 (29.5) Football related injury 3 (1.5) Stairs falls 13 (7.0) Horse falls 5 (2.6) Firearm injuries 2 (1.0) Penetrating injury by a wooden foreign body 3 (1.5) High-energy injury 133 (68.9) Gustilo & Anderson Classification for open fractures 73 (37.8) ü Type-I (no. [%]) 14 (19.2) ü Type-II (no. [%]) 23 (31.5) Type-III (no. [%]) 36 (49.3) Closed fracture 120 (62.1) More of one surgical debridement 77 (39.9) Politrauma 46 (23.8) American Society of Anesthesiologists score (no. [%]) ü ASAb I – II (1 or 2) 166 (90.7) ASAb III – IV (>2) 17 (9.3) Intraoperative blood transfusion 66 (34.2) Duration of surgery (media [range]) (hours) 2.61 (1-8) Infected Fracture Location (no. [%]) ü Upper limbs 44 (22.8) ü Lower limbs 154 (79.2) ü Collarbone 7 (3.6) ü Humerus 12 (6.2) ü Radio 13 (6.7) ü Ulna 16 (8.2) ü Hands 3 (1.5) ü Femur 59 (30.5)
34
ü Knee 9 (4.6) ü Tibia 56 (29) ü Fibula 11 (5.7) ü Feet 19 (9.8) a PTO-posttraumatic polymicrobial osteomyelitis; b ASA-American Society of Anesthesiologists score.
Table 2. Univariate analysis of risk factors associated with polymicrobial osteomyelitis (PMOa) and monomicrobial osteomyelitis (MMOb) following trauma, among 183c patients.
Characteristics MMOa Patients No. (%)
(N = 110)
PMOb Patients No. (%) (N = 73)
P valued
Demographic data Age (median [range]) (yr) 40.5 (11 – 87) 50 (16 – 88) 0.017 Male sex (no. [%]) 76 (69.0) 53 (72.6) 0.610 Schooling level >8 years (no. [%]) 47 (42.7) 20 (27.3) 0.035 Farmers (no. [%]) 9 (8.2) 16 (22.0) 0.008 Comorbidities (no. [%]) Smoking 33 (30.0) 26 (23.6) 0.426 Intraoperative hyperglycemia 29 (26.3) 27 (37.0) 0.127 High-energy injury (no. [%]) 79 (71.8) 50 (68.5) 0.629 Fall from height (no. [%]) 29 (26.4) 22 (30.1) 0.577 Grade-III open fracture (no. [%]) 15 (13.6) 21 (28.7) 0.012 Admission to surgery t >3h (no. [%]) 103 (93.6) 62 (85.0) 0.053 Duration of surgery (median [range]) (hr) 2 (1-8) 2 (1-7) 0.738 Admission to first antibiotic (hr) 60 (54.5) 26 (23.6) 0.062 Follow-up (range) (days) 728 (38 – 2539) 690 (22 – 2526) 0.980 >1 surgery debridment (no. [%]) 34 (31.0) 41 (56.1) 0.001 Need for blood transfusion (no. [%]) 26 (23.6) 38 (52.0) <0.0001 Femural fractures (no. [%]) 26 (23.6) 31 (42.5) 0.007 >3 samples for bone culture (no. [%]) 59 (53.6) 51 (69.8) 0.028 >3 samples of soft tissue (no. [%]) 12 (11.0) 20 (27.4) 0.004 ASA score ASA I - II (no. [%]) 102 (92.7) 64 (87.7)
0.249 ASA III - IV (no. [%]) 8 (7.3) 9 (12.3) a PMO-polymicrobial osteomyelitis; b MMO-monomicrobial osteomyelitis; cTen patients (5.2%) were excluded from this analysis since they presented negative-culture osteomyelitis; d The patient characteristics were summarized as frequencies and percentages or median values and compared using the Pearson chi-square test or Fisher’s exact test, as appropriate, with nominal variables and the Mann-Whitney test or t test, as appropriate, with continuous variables (SPSS version 19.0). All tests were two sided, and P values of <0.05 were considered statistically significant.
35
Table 3. Multivariate logistic regression analysis of risk predictors PTOa, among 183 patientsb.
PMOa - polymicrobial osteomyelitis; bP values of <0.05 were considered statistically significant.
Table 4. Frequency of microorganisms yielded from cultures of PTOa
Microrganisms (n = 300 ) N (%) Staphylococcus aureus 104 (34.6) ü MRSAb 37 (12.3) ü MSSAc 67 (22.3) Pseudomonas aeruginosa 31 (10.3) Acinetobacter baumannii 23 (7.6) Enterococcus sp 22 (7.3) Citrobacter sp 21 (7.0) Klebsiella pneumoniae 20 (6.6) CoNSd 19 (6.3) Escherichia coli 14 (4.6) Proteus sp 14 (4.6) Candida tropicalis 2 (0.6) Otherse 30 (10.0) a PTO-posttraumatic osteomyelitis; b MRSA-Methicillin-resistant Staphylococcus aureus; c MSSA- Methicillin-sensitive Staphylococcus aureus; d CoNS-Coagulase-negative Staphylococci; e Others-Alcaligenes sp., Enterobacter sp., Morganella morganii, Providencia sp., Serratia sp., Stenotrophomonas maltophilia, Streptococcus agalactie, Streptococcus viridans.
Variables MMOa Patient No. (%)
(N = 110)
PMOb Patient No. (%) (N = 73)
Odds Ratio CI (95%)
P Valueb
Age (median [range]) (yr) 40,5 (11 – 87) 50 (16 – 88) 1.02 (1.01 – 1.03) 0.040 Need for blood transfusion 26 (40.6%) 38 (59.4%) 2.15 (1.07 – 4.32) 0.031 Gustilo Type-III open fracture 15 (41.7%) 21 (58.3%) 2.38 (1.02 – 5.56) 0.044 Farmers 9 (8.2%) 16 (22.0%) 2.86 (1.05 – 7.79) 0.002 >1 surgery debridment (no. [%]) 34 (31.%) 41 (56.1%) 2.58 (1.29 - 5.16) 0.007
36
Figure 1. Kaplan-Meier estimate of cumulative survival rate showing no difference between two-year survival rate between monomicrobial osteomyelitis (MMO) and polymicrobial osteomyelitis (PMO).
37
References
1. Zhou J, Li Y, Wang QK, Pollak AN, Slobogean GP. Status of road safety and injury burden: China. J Orthop Trauma 2014;28(Suppl 1):S41-2.
2. Yano MH, Klautau GB, da Siva CB, Nigro S, Avanzi O, Mercadante MT et al. Improved Diagnosis of Infection Associated with Osteosynthesis by Use of Sonication of Fracture Fixation Implants. J Clin Microbiol 2014;52(12):4176-82.
3. Nan Jiang N, Ma Y, Jiang Y, Zhao X, Xie G, Hu Y et al. Clinical Characteristics and Treatment of Extremity Chronic Osteomyelitis in Southern China. Medicine 2015;94(42):1-7.
4. Gosselin RA, Roberts I, Gillespie WJ. Antibiotics for preventing infection in open limb fractures. Cochrane Database Syst Rev 2004;(1):1-27.
5. Darouiche RO. Treatment of Infections Associated with Surgical Implantes. N Engl J Med 2004;350:1422-9. 6. Morris DS, Rohrbach J, Sandaram LMT, Sonnad S, Sarani B, Pascual J et al. Early hospital readmission in the
trauma population: Are the risk factors different? Injury 2014;45(1):56-60. 7. Trampuz A, Zimmerli W. Diagnosis and treatment of infections associated with fracture- fixation devices. Injury
2006;37:S59-S66. 8. Gustilo RB, Merkow RL, Templeman D. The management of open fractures. J Bone Joint Surg Am
1990;72(2):299-304. 9. Brady RA, Leid JG, Costerton JW, Shirtliff ME. Osteomyelitis: Clinical Overview and Mechanisms of Infection
Persistence. Clin Microbiol Newsl 2006;28(9):65-72. 10. Kremers HM, Nwojo ME, Ransom JE, Wood-Wentz CM, Melton III LJ, Huddleston III PM. Trends in the
Epidemiology of Osteomyelitis. J Bone Joint Surg Am 2015;97:837-45. 11. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in long bones. J Bone Joint Surg Am 2004;86(10):2305-18. 12. Uçkay I, Hoffmeyer P, Lew D, Pittet D. Prevention of surgical site infections in orthopaedic surgery and bone
trauma: state-of-the-art update. J Hosp Infect 2013;84:5-12. 13. Li G, Guo F, Ou Y, Dong G, Zhou W. Epidemiology and outcomes of surgical site infections following
orthopedic surgery. Am J Infect Control 2013;41:1268-71. 14. Centers for Disease Control and Prevention [homepage na internet]. CDC/NHSN Surveillance Definitions for
Specific Types of Infections [access on February 14, 2016]. Available in: www.cdc.gov. 15. Lipsky BA, Berendt AR. Osteomyelitis. ACP Medicine. Decker Intellectual Properties; 2010, p. 1-20. DOI
10.2310/7900.1137. 16. Lipsky BA, Berendt AR, Cornia PB, Pile JC, Peters EJG, Armstrong DG et al. 2012 Infectious Diseases Society
of America Clinical Practice. Guideline for the Diagnosis and Treatment of Diabetic Foot Infections. Clin Infect Dis 2012;54(12):132-73.
17. Malizos KN, Gougoulias NE, Dailiana ZH, Varitimidis S, Bargiotas KA, Paridis D. Ankle and foot osteomyelitis: treatment protocol and clinical results. Injury 2010;41(3):285-93.
18. Museru LM, Mcharo CN. Chronic osteomyelitis: a continuing orthopaedic challenge in developing countries. Int Orthop 2001;25(2):127-31.
19. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA et al. The microbiology of chronic osteomyelitis: Prevalence of resistance to common empirical anti-microbial regimens. Journal of Infection 2010;60:338-43.
20. Ali MH, Hoekzema NA, Bakleh M, Shin AY, Osmon DR. The Microbiology and Risk of Infection Following Open, Agricultural Upper Extremity Injuries. J Hand Surg Am 2008;33(1):87-93.
21. Tartter PI. Blood transfusion and postoperative infections. Transfusion 1989;29 (5):456–9. 22. Carson JL, Altman DG, Duff A, Noveck H, Weinstein MP, Sonnenberg FA et al. Risk of bacterial infection
associated with allogeneic blood transfusion among patients undergoing hip fracture repair. Transfusion
38
1999;39(7):694-700. 23. Patzakis MJ, Zalavras CG. Chronic posttraumatic osteomyelitis and infected nonunion of the tibia: current
management concepts. J Am Acad Orthop Surg 2005;13(6):417-27. 24. Glass GE, Barrett SP, Sanderson F, Pearse MF, Nanchahal J. The microbiological basis for a revised antibiotic
regimen in high-energy tibial fractures: preventing deep infections by nosocomial organisms. J Plast Reconstr Aesthet Surg 2011;64(3):375-80.
25. Johnson EN, Burns TC, Hayda RA, Hospenthal DR, Murray CK. Infectious complications of open type III tibial fractures among combat casualties. Clin Infect Dis 2007;45(4):409-15.
26. Lew DP, Waldvogel FA. Osteomyelitis. Lancet 2004;364 (9431): 369-79. 27. Hudson MC, Ramp WK, Nicholson NC, Williams AS, Nousiainen MT. Internalization of Staphylococcus aureus
by cultured osteoblasts. Microbial Pathogenesis 1995;19:409–19. 28. Guzmán-Blanco M, Mejía C, Isturiz R, Alvarez C, Bavestrello L, Gotuzzo E, Labarca J, Luna CM, Rodríguez-
Noriega E, Salles MJ, Zurita J, Seas C. Epidemiology of methicillin-resistant Staphylococcus aureus (MRSA) in Latin America. Int J Antimicrob Agents 2009;34(4): 304-8. doi: 10.1016/j.ijantimicag.2009.06.005
39
Artigo 2
International Orthopaedics
Predisposing Factors for Recurrence of Chronic Posttraumatic Osteomyelitis --Manuscript Draft--
Manuscript Number: INOR-D-16-02163
Full Title: Predisposing Factors for Recurrence of Chronic Posttraumatic Osteomyelitis
Article Type: Original Paper
Funding Information:
Abstract: Purpose: The incidence of posttraumatic osteomyelitis (PTO) is increasing despite new treatment strategies. Assessment of patients' outcomes following PTO is challenging due to multiple variables. The study goals are to determine the frequency of recurrence following PTO treatment and identify factors predisposing patients to treatment failure.
Methods: Between August 2007 and August 2012, a single-center prospective cohort study was performed among 193 patients diagnosed with PTO following orthopedic surgery for fracture care. Bone and soft tissues were collected for cultures and PTO was defined according to CDC/NHSN criteria. Patient, injury, surgery-associated variables, and microbiological records were reviewed for risk factors associated to recurrence of PTO. Univariate and multivariable analyses using logistic regression were performed, with p <0.05 considered significant.
Results: Thirty-eight patients (20%) of 192 diagnosed and treated for PTO failed their treatment. Factors associated with recurrence were age between 61 and 80 years [hazard ratio (HR) = 6.086, 95% confidence interval (CI) = 2.459;15.061, p = <0.001], age above 80 years [HR = 9.975 (95% CI = 3.591;27.714), p = <0.001], intraoperative blood transfusion [HR = 2.239 (95% CI = 1.138;4.406), p = 0.020], and positive culture for Pseudomonas aeruginosa [HR = 2.700 (95% CI = 1.370;5.319), p = 0.004].
Conclusions: Risk factors associated with recurrence of PTO are difficult to measure. The present study revealed that elderly patients, intraoperative blood transfusions, and infection due to P. aeruginosa were independently associated with recurrence of PTO. These factors should warn clinicians of a higher failure rate following treatment of PTO.
Corresponding Author: Mauro Jose Costa Salles, MD Division of Infectious Diseases, Department of Internal Medicine; Santa Casa de Sao Paulo School of Medical Sciences, Sao Paulo, Brazil. BRAZIL
Corresponding Author Secondary Information:
Corresponding Author's Institution:
Division of Infectious Diseases, Department of Internal Medicine; Santa Casa de Sao Paulo School of Medical Sciences, Sao Paulo, Brazil.
Corresponding Author's Secondary Institution:
First Author: Luciana S. Jorge, MD
First Author Secondary Information:
Order of Authors: Luciana S. Jorge, MD
40
Cyril Mauffrey, MD
Michael A. White, MD
David Hak, MD, MBA, FACS
Alceu G. Chueire, MD
Mauricio N. Machado, MD
Patricia S. F. Ferreira, MD Marcelo A. Nakazone, MD
Mauro Jose Costa Salles, MD
Order of Authors Secondary Information:
Author Comments: To whom it may concern:
We are submitting our paper titled "Predisposing Factors for Recurrence of Chronic Posttraumatic Osteomyelitis" for review. We look forward to our correspondence with you and hope that you will consider our paper for publication.
Thank you.
Powered by Editorial Manager® and ProduXion Manager® from Aries Systems Corporation
41
Fatores Predisponentes para Recorrência das Osteomielites Crônicas Pòs-traumáticas
Proposta: A incidência de osteomielite pós-traumática (OPT) está aumentando a despeito de novas
estratégias de tratamento. A avaliação da evolução dos pacientes após OPT é desafiadora devido a várias
variáveis. Os objetivos do estudo são determinar a frequência de recorrência das OPT após tratamento e
identificar os fatores predisponentes à falência terapêutica.
Métodos: Um estudo retrospectivo de coorte, unicêntrico, foi realizado em 193 pacientes portadores de
OPT subseqüente à cirurgia ortopédica para correção de fraturas entre agosto de 2007 e agosto de 2012.
Amostras de osso e de partes moles foram coletadas para cultura e OPT foi definida de acordo os critérios
do CDC/NHSN. Variáveis associadas ao paciente, trauma e cirurgia e resultados microbiológicos foram
revisados para fatores de risco associados à recorrência de OPT. As análises univariada e multivariada,
por regressão logística, foram realizadas, e p <0.05 foi considerado significante.
Resultados: Trinta e oito pacientes (20%) de 192 apresentaram falência após diagnóstico e tratamento de
OPT. Os fatores associados à recorrência foram a idade entre 61 e 80 anos [hazard ratio (HR) = 6,086,
intervalo de confiança de 95% (IC) = 2,459;15,061, p = <0,001], idade menor que 80 anos [HR = 9,975
(IC 95% = 3,591;27,714), p = <0,001], transfusão intra-operatória de concentrado de hemácias [HR =
2,239 (IC 95% = 1,138;4,406), p = 0,020], e cultura positiva para Pseudomonas aeruginosa [HR = 2,700
(IC 95% = 1,370;5,319), p = 0,004].
Conclusões: Os fatores de risco associados com recorrência da OPT são de difícil mensuração. O
presente estudo revelou que pacientes idosos, transfusão de concentrado de hemácias no intra-operatório e
infecção por P. aeruginosa foram independentemente associados com a recorrência da OPT. Esses fatores
devem alertar os médicos de uma maior taxa de falência terapêutica nas OPT.
Palavras-chave: osteomielite pós-traumática, fatores do paciente, tratamento, fatores microbiológicos
42
Introdução:
Informações: Apesar dos avanços nas estratégias de diagnóstico, tratamento e prevenção, existe um
aumento constante na incidência das osteomielites na população adulta [1, 2]. Nas últimas décadas, os
fatores predisponentes e os micro-organismos responsáveis pelas osteomielites mudaram drasticamente.
No passado, as infecções ósseas eram decorrentes principalmente da disseminação hematogênica aguda
de cocos Gram-positivos, tais como Staphylococcus aureus. Pelo contrário, atualmente as osteomielites
são, na maioria das vezes, pós-traumáticas, relacionadas a implantes, além de afetarem portadores de
diabetes mellitus. Os micro-organismos são tipicamente Staphylococcus aureus meticilina-resistente,
estafilococos coagulase-negativo formadores de biofilme, ou bacilos Gram-negativos multirresistentes,
incluindo Pseudomonas aeruginosa e Acinetobacter baumannii, entre outros [3, 4, 5-6]. Um estudo de
coorte histórica, baseado na população, foi realizado nos Estados Unidos e revelou que osteomielite
crônica quase triplicou com o tempo nos idosos, especialmente entre pacientes diabéticos, e que
permaneceu relativamente estável entre as crianças e adultos jovens [7]. Entretanto, um estudo chinês de
coorte avaliou a epidemiologia das osteomielites crônicas e confirmou sua frequência crescente,
principalmente entre adultos previamente saudáveis envolvidos em acidentes de tráfego e em violência
interpessoal [8]. A combinação de diagnóstico rápido, desbridamento cirúrgico agressivo e terapia
antimicrobiana específica podem reduzir a alta frequência das osteomielites pós-traumáticas (OPT),
especialmente nos países em desenvolvimento [9, 10].
Fundamentação: Em oposição aos dados a respeito da incidência crescente das OPT, as pesquisas sobre
a evolução clínica das osteomielites e os fatores predisponentes à recorrência da infecção óssea após o
tratamento das OPT são escassas [11]. Recorrências após tratamento de osteomielite de membros
inferiores correspondem a 20% a 30% [12]. Estudo retrospectivo de pacientes com osteomielite de foco
contíguo, a infecção por Pseudomonas aeruginosa e a terapia antimicrobiana inapropriada contra S.
aureus foram considerados fatores de risco independentes para recorrência [13]. Além disso, em um
43
recente estudo de coorte colombiano sobre osteomielite crônica recorrente, as taxas mais baixas de
falência terapêutica foram observadas em pacientes que receberam terapia antimicrobiana apropriada e
que foram tratados por especialistas em doença infecciosa no cenário de uma equipe multidisciplinar ao
lado dos cirurgiões ortopédicos [14].
Questionamentos do Estudo: Estudos detalhados que avaliem fatores relacionados ao paciente, ao
trauma, a achados microbiológicos e à cirurgia e que sejam predisponentes à recorrência de OPT são de
extrema importância e podem auxiliar na padronização de medidas de controle eficientes e custo-efetivas,
a fim de reduzir a frequência das OPT recorrentes em uma escala global.
Esse estudo visa:
Determinar a frequência de recorrência após tratamento das OPT;
Identificar fatores de risco associados ao paciente, trauma, micro-organismos e à cirurgia que
predisponham à recorrência das OPT .
Métodos
DelineamentodoEstudo:
Esse estudo é uma coorte prospectiva, unicêntrica, que foi realizada em um período de cinco anos (Agosto
de 2007 a Agosto de 2012) em um hospital terciário de referência regional. Os dados foram coletados de
uma coorte observacional de pacientes tratados para osteomielite pós-traumática (OPT). O foco da coleta
de dados foi comparar as características dos pacientes de acordo com a evolução clínica (sucesso ou
falência terapêutica).
Participantes/Sujeitos do Estudo: De 8.098 pacientes submetidos à cirurgia ortopédica para correção de
fraturas, 7.510 (92,7%), e 588 (7,3%) foram tratados para fraturas fechadas e expostas,
44
retrospectivamente. Duzentos e cinco pacientes evoluíram com OPT. Os critérios de inclusão foram
pacientes com idade superior a 12 anos, e com, pelo menos, um ano de seguimento após o procedimento
cirúrgico. Pacientes que apresentavam história prévia de infecção no mesmo local (7 pacientes) ou relatos
incompletos em prontuário médico (5 pacientes) foram excluídos. Um total de 193 pacientes com
diagnóstico de OPT participou do estudo. O Conselho de Ética institucional aprovou o estudo.
Descrição da experiência, tratamento ou cirurgia: Osteomielite foi definida de acordo com as diretrizes
dos Centers for Disease Control and Prevention (CDC) / National Healthcare Safety Network (NHSN). O
diagnóstico de osteomielite seguiu, pelo menos, um dos seguintes critérios: qualquer crescimento de
micro-organismo proveniente de cultura óssea e de partes moles; evidência de osteomielite em exame
anatômico ou histopatológico; e, pelo menos, dois dos seguintes sinais e sintomas de inflamação: febre
(>38.0°C), edema, dor, calor, secreção e deiscência ou cicatrização incompleta da ferida, com exposição
óssea ou da osteosssíntese; e, pelo menos, um dos seguintes: a) micro-organismos identificados de cultura
de sangue ou por outros testes microbiológicos em um paciente com exame de imagem sugestiva de
infecção; b) exame de imagem sugestiva de infecção. Osteomielite aguda e crônica foram definidas como
o surgimento do início dos sinais e sintomas de infecção até um mês após a cirurgia ou após esse
intervalo, respectivamente [15]. A remissão da infecção foi considerada na ausência de sinais clínicos,
laboratoriais e radiológicos de infecção durante a última consulta médica (mínimo de um ano de
seguimento), e nos casos em que não foi necessário novo procedimento cirúrgico nem a
repetição da terapia antimicrobiana para o mesmo local de infecção após o término do
tratamento [11, 15]. Falência terapêutica ou infecção recorrente foi definida como infecção no mesmo
local previamente controlado e que necessitou de nova cirurgia e/ou de um segundo curso completo de
terapia antimicrobiana parenteral [13, 15-18]. Para a proposta da análise do estudo, somente o primeiro
episódio de recorrência foi considerado e os episódios subsequentes foram excluídos.
45
Variáveis, evolução, fontes de dados e viés: A fim de identificar os potenciais fatores de risco associados
com falência terapêutica das OPT, várias variáveis (comorbidades, variáveis associadas ao trauma, aos
achados microbiológicos e à cirurgia ortopédica) foram revisadas no prontuário médico. Dados
demográficos (idade, gênero, ocupação e nível de escolaridade), comorbidades, tabagismo, consumo de
álcool, diabete melito e a classificação da American Society of Anesthesiologists (ASA) foram também
analisados. As variáveis associadas ao trauma incluíram o intervalo entre a admissão e a primeira dose do
antibiótico e entre a admissão e a cirurgia, o local anatômico da fratura, o mecanismo do trauma baseado
no grau de energia (baixa e alta energia), classificação de Gustilo para fratura exposta. Os fatores
relacionados à cirurgia foram o tipo de procedimento cirúrgico (redução aberta seguida de fixação interna
ou fixação em dois estágios com fixador externo temporário), duração da cirurgia, e a necessidade de
transfusão de concentrado de hemácias no intra-operatório. Além disso, a necessidade de desbridamento
cirúrgico suplementar foi avaliada para as feridas infectadas. A coleta de, pelo menos, três amostras de
partes moles e/ou de osso para microbiologia e para a patologia foi realizada na sala de cirurgia, no
momento do desbridamento do sítio cirúrgico.
Análise Estatística: Estatisticamente, o seguimento dos pacientes foi definido como o intervalo de tempo
entre as datas da primeira consulta médica e da remissão ou da falência terapêutica das OPT,
considerando, pelo menos, um ano de acompanhamento. A população global do estudo e os grupos
definidos como remissão da infecção e falência ou recorrência foram descritas como média e
porcentagem para variáveis qualitativas, e como mediana e desvio padrão para variáveis quantitativas. A
associação entre as variáveis qualitativas foi analisada pelo teste qui-quadrado e pelo teste exato de
Fisher. Já a associação entre as variáveis quantitativas foi avaliada por regressão logística. A estimativa
de risco foi calculada para as variáveis associadas com fator de risco para falência e foi relata como razão
de risco (“hazard ratio”) com intervalo de confiança (IC) de 95%. O modelo de regressão logística para
selecionar as variáveis significantes identificadas na análise univariada foi aplicado quando o nível de
46
significância foi menor que 0,20 (p < 0,20) e as variáveis com nível de significância menor que 0,5 (p <
0,05) permaneceram no modelo final. O modelo de Kaplan-Meier calculou a sobrevida livre de doença,
assim como a análise de regressão multivariada de Cox. A diferença foi considerada estatisticamente
significante se o valor de p foi menor que 0,05. Todos os dados foram analisados pela versão SPSS 23
(IBM-SPSS Inc., Chicago, IL, USA).
Resultados No período de estudo, 193 pacientes com OPT foram incluídos, embora um deles tenha sido excluído das
análises devido à perda de seguimento. Portanto, 192 pacientes foram incluídos na análise, e 154 (80,2%)
destes evoluíram com remissão da infecção óssea enquanto 38 (19,8%) apresentaram recorrência (Figura
1). As características demográficas e clínicas da população do estudo foram inseridas na Tabela 1.
Pacientes com OPT foram, na sua maioria, homens (68,9%), com uma media de idade de 50 anos
(variação, 16 a 88 anos), e mais de um terço (34,7%) referiram baixo nível educacional. Tabagismo foi
um fator positivo em 59 (30,5%) e diabete foi detectado em 58 (30%) pacientes. O trauma de alta energia
foi detectado em aproximadamente 70% dos pacientes. Sessenta e seis (34,2%) sujeitos necessitaram de
transfusão de concentrado hemácias no período intra-operatório. Aproximadamente dois terços (62%) dos
casos de OPT (120 pacientes) foram associados com fratura fechada, e fratura exposta foi visualizada em
73 pacientes (38%). Dos 193 pacientes com OPT, a infecção de membros inferiores ocorreu em 154
(79,2%), afetando principalmente o fêmur (30,5%) e a tíbia (29%).
Fatores relacionados ao paciente, trauma, cirurgia e microbiologia que foram investigados para possível
associação com falência terapêutica das OPT na análise univariada estão na Tabela 2. Pacientes com risco
maior para falência terapêutica foram mulheres (falência em 50% vs. remissão em 26,6%, p = 0,005),
idosos (idade mediana de 70 anos vs. 40,5 anos, p < 0,001), com atividades domésticas (52,6% vs. 25,3%,
p = 0,001), que sofreram queda da própria altura (60,5 vs. 22,0%, p = <0,001). Além disso, pacientes
submetidos a desbridamentos adicionais (60,5% vs. 35%, p = 0,004), e a necessidade de transfusão de
47
concentrado de hemácias no intra-operatório (60,5% vs. 28%, p <0,001) também apresentaram maior
risco para recorrência de infecção após OPT. Infecções causadas por cocos Gram-positivos, incluindo
Staphylococcus aureus e Enterococcus sp., não aumentaram o risco para recorrência. Inversamente, as
infecções por bacilos Gram-negativos, tais como Escherichia coli (15,8% vs. 5,2%, p = 0,036),
Pseudomonas aeruginosa (44,7% vs. 9,1%, p = <0,001) e Acinetobacter baumannii (26,3% vs. 8,4%, p
= 0,005) apresentaram risco mais alto de falência terapêutica na análise univariada. Por outro lado,
tabagismo (p = 0,676), fratura exposta Grau III de Gustilo (p = 0,602), intervalo entre admissão e
procedimento cirúrgico (p = 0,532), diagnóstico de osteomielite crônica (p = 0,169), cultura positiva de
partes moles para Streptococcus sp. (p = 0,051) não estiveram associados com risco significantemente
elevado para falência terapêutica das OPT.
As variáveis que apresentaram significância estatística e importância clínica na análise univariada foram
adicionadas na análise multivariada de Cox (Tabela 3). Os fatores que permaneceram como variáveis
independentemente associadas à recorrência na análise multivariada foram os pacientes idosos,
especialmente aqueles com idade entre 61 e 80 anos [hazard ratio (HR) = 6,086, intervalo de confiança
(IC) 95% = 2,459;15,061, p <0,001], e acima de 80 anos [HR = 9,975 (IC 95% = 3,591;27,714), p
<0,001]; necessidade de transfusão de concentrado de hemácias [HR = 2,239 (IC 95% = 1,138;4,406), p =
0,020]; e cultura positiva de osso e/ou de partes moles para P. aeruginosa [HR = 2,700 (IC 95% =
1,370;5,319), p = 0,004].
Forte correlação também foi identificada entre P. aeruginosa e falência terapêutica das OPT. Quando P.
aeruginosa foi o micro-organismo recuperado das culturas, a sobrevida livre de doença foi muito menor
do que quando S. aureus e Enterococcus sp. Foram isolados (28 meses vs.60 meses vs.59 meses,
respectivamente, p = 0,002), na curva de sobrevida de Kaplan-Meier para os 192 pacientes com OPT
(Figura 2). A respeito da necessidade de transfusão de concentrado de hemácias no intra-operatório, a
sobrevida de livre de doença foi de 1681 dias vs. 2136 dias na ausência de transfusão (p = 0,003) (Figura
3).
48
A frequência dos micro-organismos isolados de cultura óssea e de partes moles nos pacientes com OPT
são apresentadas na Tabela 4. Das 300 culturas positivas, S. aureus foi isolado em 104 (34,7%) casos, dos
quais 37 (12,3%) e 67 (22,3%) foram resistentes à oxacilina e sensíveis à oxacilina , respectivamente. As
culturas isolaram estafilococos coagulase-negativo em somente 6,3% (19/300). Os três bacilos Gram-
negativos mais identificados foram P. aeruginosa (10,3%), A. baumannii (7,6%) e Citrobacter sp. (7%).
Além disso, as culturas de partes moles identificaram Candida tropicalis em dois pacientes com OPT.
Discussão Análise: Osteomielite pós-traumática ocorre quando ocorre a inoculação de micro-organismos no osso
durante o processo de fratura exposta ou na cirurgia de correção de uma fratura fechada. Tíbia e fêmur
são os ossos longos mais afetados [19]. De acordo com a gravidade da fratura e do tipo de hospedeiro, a
OPT pode atingir taxas tão altas quanto 50%, e a incapacidade de controlar a infecção por desbridamento
cirúrgico agressivo e apesar da terapia antimicrobiana específica, pode ser de risco [6, 12, 18, 20-25].
Mesmo assim, os fatores de risco para recorrência da infecção após procedimento cirúrgico para OPT é de
pouco interesse na literatura científica. O presente estudo relatou a evolução de 192 pacientes que foram
submetidos aos tratamentos cirúrgico e com antibióticos para osteomielite. Desses pacientes, 38 (19,8%)
evoluíram com recorrência e o estudo visou identificar fatores predisponentes significantes para
recorrência da infecção óssea após tratamento da OPT. Os resultados mostraram que os pacientes idosos,
transfusão intra-operatória de concentrado de hemácias e infecção óssea por P. aeruginosa estiverem
associação independentemente com um risco alto de falência terapêutica.
Um número considerável de dados a respeito da incidência de osteomielite após fratura exposta e fechada
foi publicado, com taxas de 1% até mais 50% [2, 19]. Por outro lado, dados referentes ao sucesso do
tratamento das OPT são escassos. Nessa série de casos, 80,2% dos pacientes evoluíram com remissão
após, pelo menos, um ano de seguimento. Taxa de remissão de 82,1% foi observada em um estudo
retrospectivo de osteomielite pós-traumática e após procedimento ortopédico, com comprometimento da
49
tíbia distal, tornozelo e pé [23]. Além disso, resultados similares (76,7% de remissão) foram encontrados
em um estudo de coorte na Colômbia que avaliou pacientes com OPT [14]. Adicionalmente, Tice et al.
observou taxas mais baixas de remissão (69,4%) entre pacientes com osteomielite crônica de foco
contínuo associada a ferida de partes moles ou à cirurgia prévia durante um seguimento médio acima de
27,5 meses [13]. Por outro lado, taxa de remissão muito melhor (92%) foi observada um estudo suíço
caso-controle, unicêntrico, sobre infecção associada à osteossíntese [11]. A justificativa para essa
discrepância é complexa, mas o estudo presente sugere que variáveis, tais como, características dos
pacientes, proporção das fraturas de alta energia associadas a trauma e procedimentos cirúrgicos, possam
ser de risco para recorrência. De fato, as fraturas de alta energia (68.9%) foram causadas por acidentes de
tráfego, necessitando de desbridamentos cirúrgicos adicionais em 40% dos casos, o que foi raro no estudo
suíço [11].
O principal dado do presente estudo é que fatores independentes para falência terapêutica após OPT são
essencialmente fatores não modificáveis. Assim, pacientes idosos com idade entre 61 e 80 anos
apresentaram um risco seis vezes maior de recorrência após tratamento de OPT, e aqueles acima de 80
anos de idade tiveram um risco aproximado a dez vezes maior para falência. Em relação à necessidade de
transfusão intra-operatória de concentrado de hemácias, risco maior de duas vezes de recorrência foi
notado. A infecção óssea por P. aeruginosa apresentou risco de 2,7 maior de falência terapêutica. Por
outro lado, fatores independentemente associados com recorrência de infecção em publicações prévias,
tais como, tabagismo, fratura exposta grau II e III de Gustilo, classificação ASA elevada, infecção
polimicrobiana, presença de micro-organismo com multirresistência a antimicrobianos (S. aureus
resistente à oxacilina) e ausência de terapia antimicrobiana específica não foram encontrados nesse estudo
[11, 13-16, 19, 23]. Associação entre idade avançada e osteomielite foi visualizada em estudos prévios
por ser multifatorial. Esses fatores incluem características imunossupressoras do envelhecimento,
frequência mais alta de comorbidades (diabete e doença vascular periférica), e risco mais elevado de
quedas, resultando em fraturas fechadas e expostas [13, 12, 26]. Arias et al. recentemente notou risco de
50
1,3 vezes maior de osteomielite recorrente em pacientes com idade superior a 56 anos [14].
Perda maciça de sangue no momento da fratura ou durante e após a cirurgia, causando anemia grave e
sintomática, é a principal indicação clínica de transfusão de concentrado de hemácias [27]. Essa conduta
pode refletir a gravidade do trauma, com lesão extensa de partes moles e sangramento extenso
subsequente. Literatura mostrou que transfusão de concentrado de hemácias não é inofensiva. Embora
seja controverso, estudos prévios associaram transfusão de concentrado de hemácias com infecção de
prótese articular [28]. Em meta-análise publicada recentemente com objetivo de estudar fatores de risco
para infecção de prótese de quadril e de joelho, transfusão de concentrado de hemácias mostrou
associação significante com infecção [29]. Por outro lado, revisão sistemática Cochrane foi incapaz de
identificar forte associação entre transfusão de concentrado de hemácias e infecção de ferida operatória
após fratura de quadril [30]. Apesar da transfusão intra-operatória de concentrado de hemácias ser
considerada um fator de risco independente para recorrência de OPT no presente estudo, esse resultado
deve ser interpretado cuidadosamente. Paciente submetido a cirurgias complexas com tempo cirúrgico
prolongado pode ser mais propenso a receber transfusão de concentrado de hemácias. Menor taxa de
sobrevida livre de doença foi observada em pacientes que receberam transfusão de concentrado de
hemácias (taxas de sobrevida livre de infecção de 1681 dias para aqueles que receberam transfusão de
concentrado de hemácias vs. 2136 dias para os que não receberam transfusão).
Independentemente do fato do S. aureus sensível e resistente à oxacilina constituir o principal micro-
organismo isolado nas culturas decorrentes de OPT, P. aeruginosa é o bacilo Gram-negativo provável de
ser identificado nas culturas ósseas e de partes moles [3-4, 7-9, 19]. Contaminação por uma miríade de
bactérias Gram-negativas patogênicas não é um achado somente na fratura exposta, mas, em estudos
recentes envolvendo centros de referência em trauma em países em desenvolvimento, P. aeruginosa tem
sido, cada vez mais, identificada como causa de osteomielite adquirida no hospital e na infecção
relacionada a implante [4, 6, 8, 31-32]. Na visão microbiológica, a importância crescente da P.
aeruginosa, como micro-organismo responsável pela osteomielite, não é surpreendente e pode ser
51
facilmente justificada pelos seus fatores de virulência, decorrentes da sua capacidade excepcional de
formar biofilme nos tecidos e na superfície de implantes, gerando resistência completa virtualmente a
todas as classes de antimicrobianos indicados no tratamento das infecções ósseas [31, 32]. No presente
estudo, P. aeruginosa foi a segunda bactéria mais comumente isolada nos pacientes com OPT e foi
fortemente associada com infecção recorrente na análise multivariada. Além disso, o tempo de sobrevida
livre de doença foi muito menor nas OPT por P. aeruginosa do que naquelas causadas por S. aureus e
Enterococcus sp. na curva de Kaplan-Meier (28 meses vs. 60 meses vs. 59 meses, respectivamente).
Interessantemente, poucos estudos sobre infecção musculoesquelética puderam provar associação
independente entre culturas positivas por P. aeruginosa e uma evolução pior. Entretanto, a maioria dos
dados desses estudos anteriores avaliou principalmente portadores de infecção de prótese articular [15,
23, 28, 33, 34, 35, 36]. Um estudo retrospectivo identificou P. aeruginosa como fator de risco
independente para recorrência de infecção ortopédica associada a implante após cirurgia para fratura,
embora somente duas recorrências entre sete casos de infecção por P. aeruginosa tenham sido analisadas
[11]. Além disso, o mesmo grupo de estudo relatou uma tendência para menor taxa de remissão para
infecção por P. aeruginosa comparativamente àquelas causadas por S. aureus, incluindo as cepas
resistentes à oxacilina [31]. Tice et al. mostrou que, quando osteomielite é causada por P. aeruginosa, o
risco de recorrência aumentou em mais de duas vezes. Ao compreender que esse micro-organismo possa
sugerir o prognóstico do tratamento, cirurgiões ortopédicos e infectologistas deveriam intensificar as
medidas preventivas para infecção por bacilos Gram-negativos, além de uma abordagem mais agressiva
para procurar o diagnóstico microbiológico na suspeita de OPT.
Limitações: Esse estudo de centro único tem potenciais limitações, tais como, delineamento retrospectivo
com um número pequeno de pacientes com recorrências (38/192), o que pode afetar os resultados da
análise multivariada nas associações previamente descritas com OPT recorrente, que incluem fraturas
expostas de alta energia [14], presença de osteossíntese no local da infecção [11] e uso inapropriado de
52
antibióticos [13, 15]. Entretanto, a análise da sobrevida livre de doença foi também realizada nesse
estudo, usando regressão de Cox. O estudo foi realizado em um hospital public localizado em uma cidade
de tamanho médio, em um país em desenvolvimento, com serviço de ortopedia e traumatologia de
referência local, em que os resultados não possam ser aplicados para centros de outras localizações.
Entretanto, um banco de dados de um grande centro de cirurgias ortopédicas para trauma (8.000) foi
analisada. Recorrência das OPT pode ser subestimada devido à ausência de sinais e sintomas típicos de
inflamação, especialmente na infecção associada à osteossíntese, na qual os marcadores séricos de
inflamação são geralmente inúteis e os exames de imagem são inespecíficos [16, 19]. Por outro lado,
seguimento dos pacientes com OPT após alta hospitalar e após o término do tratamento é realizado pela
mesma equipe de médicos ortopedistas experientes e infectologistas no ambulatório da mesma instituição,
e, assim, esse viés de seleção é considerado bem controlado. Certamente, a recorrência de osteomielite é
descrita até muitos anos após cirurgia definitiva e terapia antimicrobiana [19, 20, 36], e assim um tempo
de seguimento mínimo aceitável para avaliar remissão da OPT na literatura é questionável [31]. Nesse
estudo, tempo de seguimento mínimo foi de um ano, embora a mediana de seguimento foi 1395 dias,
limitando a seleção de viés. Dependendo dos resultados microbiológicos, a recorrência pode ser
classificada em recaída (micro-organismo original) ou reinfecção (novo micro-organismo) [13].
Identificação de tais diferenças seria importante na configuração de medidas preventivas. Entretanto, esse
tema não foi avaliado no presente estudo.
Conclusões:
Apesar das limitações citadas, esse estudo unicêntrico revelou alta taxa de recorrência após OPT em um
grupo específico de pacientes e seu cenário clínico. Taxa mais elevada de recorrência em pacientes que
desenvolvem OPT foi visualizada nos idosos, em pacientes que necessitaram de transfusão intra-
operatória de concentrado de hemácias e nas infecções causadas por P. aeruginosa. Paciente com
qualquer um destes fatores predisponentes deveria ser reconhecido precocemente e seguido rigorosamente
53
devido ao alto risco de evolução desfavorável. Além disso, paciente com suspeita clínica de OPT ou
recorrência de infecção após OPT deve ter um diagnóstico microbiológico rápido, e uma abordagem
terapêutica multidisciplinar dirigida ao micro-organismo identificado deve ser iniciada. Estudos futuros
de coorte multicêntricos prospectivos são necessários para corroborarem esses resultados.
54
Legendas: Figura 1 representa um fluxograma, indicando a inserção dos pacientes e o acompanhamento no decorrer
do estudo. Além disso, essa figura descreve os fatores associados à falência terapêutica das osteomielites
pós-traumáticas.
Figura 2 representa estimativa de Kaplan–Meier do risco cumulativo de falência de acordo com o
tratamento avaliado no seguimento de 100 meses. O teste comparou duas curvas de sobrevida em vários
momentos. Pacientes que tiveram OPT causadas por P. aeruginosa tiveram menor sobrevida livre de
doença do que aquelas causadas por S. aureus e por Enterococcus sp. (p = 0,002).
Figura 3 representa estimativa de Kaplan–Meier do risco cumulativo de falência de acordo com o
tratamento avaliado no seguimento de 100 meses. O teste comparou duas curvas de sobrevida em vários
momentos. Pacientes que necessitaram de transfusão intra-operatória de concentrado de hemácias tiveram
menor sobrevida livre de doença do que aqueles que não receberam transfusão (p = 0,003).
Tabela 1 representa as características demográficas e do trauma de 193 pacientes associadas com
remissão e falência de tratamento da OPT.
Tabela 2 representa análise univariada dos fatores de risco associados com falência terapêutica da OPT.
Tabela 3 representa o modelo de risco da análise multivariada de Cox dos fatores de risco associados
com falência terapêutica da OPT.
Tabela 4 representa a freqüência de micro-organismos identificados de culturas.
55
Tabela 1. Características demográficas e do trauma de 193 pacientes associadas com remissão e falência de tratamento da OPTa. Dados demográficos N=193 (%)
Idade (média [variação]) (anos) 50 (16-88) Sexo masculino (no. [%]) 133 (68,9)
Nível de escolaridade <8 anos 67 (34,7) Comorbidades(no.[%])
Tabagismo 59 (30,5) Hiperglicemiaintraoperatória 58(30,0)
Ocupação(no.[%])Agricultura 26 (13,5) Condutor de veículos (carro, moto, caminhão) 24 (12,5) Construção / Operação deMáquinas 44 (22,8) Negócios 40 (20,7) Atividade Doméstica 59 (30,5)
Tipos de trauma (no. [%]) Acidente automobilístico 110 (57,0) Queda da própria altura (< 1m) 57 (29,5) Trauma relacioanado ao futebol 3 (1,5) Outras quedas 18 (9,6) Outros traumas 8 (4,0) Trauma pemetrante por corpo estranho 3 (1,5) Trauma de alta energia 133 (68,9)
Classificação de Gustilo & Anderson para fratura exposta fractures
73 (37,8) Tipo-I (no. [%]) 14 (19,2) Tipo-II (no. [%]) 23 (31,5) Tipo-III (no. [%]) 36 (49,3)
Fratura fechada 120 (62,2) Mais de um desbridamento cirúrgico 77 (39,9) Politrauma 46 (23,8) Classificação da American Society of Anesthesiologists (no. [%])
ASAb I – II (1 or 2) 166 (90,7) ASAb III – IV (>2) 17 (9,3)
Transfusão intraoperatória de concentrado de hemácias 66 (34,2) Duração da cirurgia (media [variação]) (horas) 2,61 (1-8) Local da fratura infectado (no. [%])
Membro superior 44 (22,8) Membro inferior 154 (79,2) Clavícula 7 (3,6) Úmero 12 (6,2) Rádio 13 (6,7) Ulna 16 (8,2) Mãos 3 (1,5) Fêmur 59 (30,5) Joelho 9 (4,6) Tíbia 56 (29) Fíbula 11 (5,7) Pés 19 (9,8)
PTOa:osteomielitepós-traumática;ASAb:AmericanSocietyofAnesthesiologists.
56
Tabela 2. Análise univariada dos fatores de risco associados com falência terapêutica da OPTa. Características Falência Remissão Valor Pc
No. (%) No. (%) (N = 38) (N = 154)
Dados demográficos Idade (mediana [variação]) (anos)
<40 years 70 (16 – 88) 9 (23,6)
40.5 (11 – 86) 77 (50,0)
<0,001
41 – 60 anos 6 (15,8) 55 (35,7) 61 – 80 anos 14 (37,0) 20 (13,0) > 80 anos 9 (23,6) 2 (1,3)
Sexo masculino (no. [%]) 19 (50,0) 113 (73,4) 0,005 Atividade doméstica (no. [%])
Comorbidade (no. [%]) 20 (52,6) 39 (25,3) 0,001
Tabagismo 11 (29,0) 50 (32,5) 0,676 Queda da própria altura (no. [%]) 23 (60,5) 34 (22,0) <0,001 Fratura exposta Grau-III (no. [%]) 6 (15,8) 30 (19,5) 0,602 Tempo admissão a cirurgia >3h (no. [%]) 36 (94,7) 139 (90,2) 0,532 >1 desbridamento cirúrgico (no. [%]) 23 (60,5) 54 (35,0) 0,004 Transfusão de concentrado de hemácias (no. [%]) 23 (60,5) 43 (28,0) <0,001 Fratura de membro inferior (no. [%]) 37 (97,3) 116 (75,3) 0,002 Prótese bipolar de quadril (no. [%]) Classificação ASA
8 (21,0) 5 (3,2) <0,001
ASAb I - II (no. [%]) 30 (79,0) 145 (94,1) 0,007 ASA III - IV (no. [%]) 9 (12,3) 8 (7,3)
Osteomieltie crônica (no. [%]) 16 (42,1) 84 (54,5) 0,169 Staphylococcus aureus (no. [%]) 25 (13%) 79 (41,1%) 0,010 Streptococcus sp. (no. [%]) 4 (10,5) 4 (2,6) 0,051 Enterococcus sp. (no. [%]) 8 (21,1) 14 (9,1) 0,048 Escherichia coli (no. [%]) 6 (15,8) 8 (5,2) 0,036 Pseudomonas aeruginosa (no. [%]) 17 (44,7) 14 (9,1) <0,001 Acinetobacter baumannii (no. [%]) 10 (26,3) 13 (8,4) 0,005 PTOa: osteomielite pós-traumática; ASAb: American Society of Anesthesiologists; cCaracterísticas dos pacientes foram resumidas como frequência e porcentagem ou mediana e comparadas pelo teste qui-quadrado de Pearson ou exato de Fisher por ser apropriado para variáveis qualitativas e o teste de Mann-Whitney por ser apropriado para variáveis contínuas. O valor P <0,05foi considerado estatisticamente significante.
57
Tabela 3: Análise multivariada de Cox para fatores de risco associados com falência terapêutica das OPTd
Variáveis HRa (IC 95%) Valor Pc
Idadeb
61 – 80 anos 6,086 (2,459; 15,061) <0,001 >80 anos 9,975 (3,591; 27,714) <0,001
Transfusão de concentrado de hemácias 2,239 (1,138; 4,406) 0,020 Pseudomonas aeruginosa 2,700 (1,370; 5,319) 0,004
aHazardRatio;bMenorouiguala40anoscomoreferência;cValorP<0,005foiconsideradoestatisticamentesignificante.OPTd:osteomielitepós-traumática
58
Tabela 4: Frequência de micro-organismos identificados em culturas
Micro-organismos N (%) Staphylococcus aureus 104 (34,6)
Resistente à oxacilina 37 (12,3) Sensível à oxacilina 67 (22,3)
Pseudomonas aeruginosa 31 (10,3) Acinetobacter baumannii 23 (7,6) Enterococcus sp. 22 (7,3) Citrobacter sp. 21 (7,0) Klebsiella pneumoniae 20 (6,6) ECNa 19 (6,3) Escherichia coli 14 (4,6) Proteus sp. 14 (4,6) Candida tropicalis 2 (0,6) Outrosb 30 (10,0) aEstafilococos coagulase-negativo; bOutros - Alcaligenes sp., Enterobacter sp., Morganella morganii,
Providenciasp.,Serratiasp.,Stenotrophomonasmaltophilia,Streptococcusagalactiae,Streptococcusviridans.
59
POPULAÇÃO DO ESTUDO
8.098 pacientes avaliados para seguimento
7510(92,7%)fraturasfechadas
588(7,3%)fraturasexpostas
205patientescomOPT
-12(5,9%)excluídos:
- 7OPTprévia
- 5prontuáriosincompletos
193pacienteselegívei
192pacientesincluídosnaanáliseparaevoluçãodotratamento
154pacientescomremissãodaOPT
38pacientescomrecorrênciadaOPT
Fig1.Fluxogramadoseguimentodospacientesnoestudo.
1 excluído: perda de seguimento
60
Figure 2
(Figura 2) Estimativa de risco acumulativo de falência pela curva de Kaplan–Meier de acordo com o tratamento avaliado em seguimento de 100 meses. Pacientes que evoluíram com OPT por P. aeruginosa tiveram sobrevida livre de doença menor do que por S. aureus e Enterococcus sp. (p = 0,002).
61
Figure 3
(Figura 3) Estimativa de risco acumulativo de falência pela curva de Kaplan–Meier de acordo com o tratamento avaliado em seguimento de 100 meses. Pacientes que necessitaram de transfusão de concentrado de hemácias tiveram menor sobrevida livre de doença do que aqueles que não receberam transfusão (p = 0,003).
62
Predictors of Treatment Failure in Posttraumatic Osteomyelitis
Introduction:
Despite the current knowledge in preventive measures and in the modern medical
techniques on diagnosing and the treatment of osteomyelitis, there have been a clear increasing
trend in the disease incidence, affecting either young and elderly persons (1,2). Besides, in a few
decades the predisposing factors and causative microorganisms changed dramatically from
mostly acute haematogenous spread of Gram-positive cocci such as Staphylococcus aureus to
post-trauma, implant-associated and diabetes melittus-related chronic osteomyelitis frequently
caused by methicillin-resistant Staphylococcus aureus (MRSA), biofilm-forming coagulase-
negative Staphylococcus, and a multitude of multidrug resistant (MDR) Gram-negative bacilli
including Pseudomonas aeruginosa, Acinetobacter baumannii, among others (3,4).
Recently, a population-based historical cohort study carried in United States have shown
that chronic osteomyelitis (COM) almost tripled over time in the elderly, especially among
diabetic patients while it remained relatively stable among children and young adults (5). On the
other hand, a Chinese cohort study addressing the epidemiology of COM have confirmed its
rising frequency, especially among previously healthy younger adults mainly associated to road
traffic accidents and interpersonal violence (6). Prompt diagnosis, aggressive surgical
debridement associated with targeted administration of antibiotics may in turn reduce the
growing frequency of post-traumatic osteomyelitis (PTO), especially among developing
countries population (7,8).
In contrast to a fairly amount of data showing the rising occurrence of PTO, little
attention has been paid to predictors associated to recurrent bone infection after PTO treatment
(9). Despite of that, recurrence rates following lower extremities bone infection is estimated to
occurs between 20% to 30% (20). Furthermore, more detailed studies addressing patient, injury,
microbiological findings, and surgery-related predisposing factors to recurrence of PTO are of
utmost importance, which may help implementing efficient and cost-saving control measures to
reduce its frequency. In a retrospective study of patients mostly with contiguous osteomyelitis,
bone infected by Pseudomonas aeruginosa and inappropriate antibiotic therapy for S. aureus
were independent factors for recurrence (10). Moreover, in a recent Colombian cohort study of
recurrent chronic osteomyelitis, lower rates of treatment failure were observed for whom that
received appropriate antibiotic therapy and for those who had been followed by infectious
diseases specialists organized in a multidisciplinary team along with orthopedic surgeons (11).
To the best of our knowledge, there have been very few studies examining the
predisposing factors associated to surgical and clinical treatment failure of PTO. We therefore
aimed at identifying subjects, injury, pathogen, and surgery-associated risk factors predisposing
patients to recurrent PTO.
63
Patients e Methods
Study Design
From an observational cohort of patients treated for posttraumatic osteomyelitis (PTO)
over a five-year period (2007-2012) in the Orthopedic and Traumatology Unit of Hospital de
Base (São José do Rio Preto, Brazil), we retrospectively collected data to compare
characteristics of patients according to outcome (treatment success or failure). Of 8,098 patients
undergoing orthopedic surgery due to trauma, 7,510 (92.7%), and 588 (7.3%) had closed and
open fracture, respectively. Two hundred and five patients developed PTO, although seven were
excluded due to previous history of infection in the same site, and five patients had incomplete
medical records. This left 193 subjects diagnosed with osteomyelitis following orthopedic
surgery for closed and open fractures. The study included subjects older than 12 years old and
with at least one year of follow-up after the surgical procedures. The study was reviewed and
approved by the local Institutional Review Board.
Identification of post-traumatic osteomyelitis (PTO)
Definition osteomyelitis was based upon the Center for Diseases Control and Prevention
(CDC)/National Healthcare Safety Network (NHSN) guidelines, in which at least one of the
following criteria was present: any growth of organism in bone and soft tissue culture; evidence
of osteomyelitis on anatomic or histopathologic exam; and at least two of the following signs
and symptoms of inflammation: fever (>38.0°C), swelling, pain, redness, heat, drainage and
delayed wound closure with exposed bone or osteosynthesis; and at least one of the following:
a) organisms identified from blood by culture or non-culture based microbiologic testing
method in a patient with imaging test evidence suggestive of infection; b) imaging test evidence
suggestive of infection. Acute and chronic osteomyelitis was defined as time from initiation of
signs and symptoms of infection to diagnosis lasting for less than one and more than one month,
respectively (12). We considered patients on remission of infection when there was absence of
clinical, laboratory or radiological signs of infection evaluated during the last medical visit
(minimum of one year of follow-up), and of which there was no need for reoperation or
administration of extra course of antibiotic therapy for the same site of infection following the
end of therapy (9, 12). Treatment Failure or recurrent infection was defined as infection at the
same site that had been previously controlled and which had been submitted to reoperation
and/or second complete course of parenteral antibiotic therapy (10,12-13). For the purpose of
study analysis, we included only the first episode of recurrence and subsequent episodes were
further excluded.
Potential risk factors
In order to identify potential risk factors associated to failure of treatment of PTO,
patient, injury, microbiological findings, and surgery-associated variables were assessed by
64
reviewing medical, intra-operative, and microbiological records. Demographics (age, gender,
occupational status, educational level), comorbidities (smoking, alcoholism, and diabetes), and
American Society of Anesthesiologists (ASA) classification were analyzed. Injury-associated
variables assessed were time elapsed from admission to the first dose of antibiotic and to
surgery, anatomical site of fracture, mechanism of trauma such as low-energy injury (fall own
height) or high-energy (car, motorcycle, or bicycle accident or even fall from a height above 1
m), and Gustilo open fracture classification. Surgery-related factors analyzed were type of
surgery procedure (open reduction and internal fixation or two-stage temporary external
fixator), duration of surgery, and the need for blood transfusion. Furthermore, we also assessed
the need to performing supplementary surgical debridement for infected wounds. Specimen
collection and microbiology in the surgical ward, at least three tissue samples from infected
bone and soft tissues were collected during surgical debridement, and therefore processed for
microbiology and histopathology.
Statistical analysis
For statistical analysis, the follow-up was defined as the time interval between the date of
first medical visit and date of remission or failure of treatment of PTO, considering at least one-
year of follow-up. The overall sample and the groups assigned as remission of infection and
failure or recurrence were described as mean and percentage for qualitative variables, and
median and standard deviation (SD) for quantitative variables. The association between
qualitative variables was made using the chi-square test and Fisher's exact test. For associations
between quantitative variables bivariate logistic regression was chosen. The risk estimates were
calculated on the variables associated with risk factors for failure and reported as a hazard ratio
with respect to 95% confidence interval (CI). Multiple logistic regression model by selecting the
variables of bivariate analysis tests was applied when there were significance levels lower than
0.20 (p < 0.20) and remained in the final models only significant variables lower to 0.5 (p <
0.05). The Kaplan-Meier method was used to calculate disease-free survival, and log rank test to
evaluate the equality of survival distributions across different strata. Disease-free survival was
also evaluated using univariate and multivariate Cox regression analysis. The difference was
considered statistically significant if the p-value was less than to 0.05. All data were analyzed
using SPSS version 23 (IBM-SPSS Inc., Chicado, IL, USA).
Results
Study Population
During the study period, one hundred and ninety-three patients with PTO were included,
although one patient was excluded from further analysis as he did not complete at least one-year
of follow-up. Therefore, 192 patients were included for the outcome analysis, of which 154
65
(80.2%) presented remission of bone infection at the time outcomes were analyzed, and 38
(19.8%) were diagnosed with recurrent infection (Figure 1). Demographic and clinical
characteristics of the study population are summarized on Table 1. In general, patients with
PTO were mainly male (68.9%), with mean age of fifty-years (range, sixteen to eighty-eight
years), and more than one third (34.7%) described poor educational status. Few comorbidities
were identified, including smoking in 59 (30.5%) and intraoperative hyperglycemia in 58 (30%)
patients. Interestingly, injuries were mainly associated with high-energy traumas (68.9%),
including car crash accidents and falls from height, occurring in 110 (57.0%), and 57 (29.5%)
episodes, respectively. Sixty-six (34.2%) subjects needed intraoperative blood transfusion.
Nevertheless, nearly two-thirds (62.2%) of our PTO cases were associated with closed fractures,
whereas open fractures occurred in 73 (37.8) patients. Among 193 PTO patients, lower limb
infections occurred in 154 (79.2%), affecting predominantly femur (30.5%) and tibia (29%).
Potential risk factors for recurrence of posttraumatic osteomyelitis
Patient, injury, surgical and microbiological related factors that were investigated for
possible association with treatment failure of PTO in the univariate analysis are shown in Table
2. Patients with higher risk for treatment failure were female (failure in 50% vs. remission in
26.6%, p = 0.005), older (median age of 70 years vs. 40.5 years, p < 0.001), with household
activities (52.6% vs. 25.3%, p = 0.001), in which trauma were associated to fall from height
(60.5 vs. 22.0%, p = <0.001). Additionally, patients undergoing additional debridement
procedures (60.5% vs. 35%, p = 0.004), and the need for intraoperative blood transfusions
(60.5% vs. 28%, p <0.001) also presented higher risk for recurrence of infection after PTO.
Furthermore, there were also a strong correlation between lower limb fractures (97.3% vs.
75.3%, p = 0.002), and bipolar hip prosthesis in primary orthopedic surgery (21% vs. 3.2%, p
<0.001) with treatment failure after PTO. Surprisingly, infections caused by Gram-positive
cocci, including Staphylococcus aureus and Enterococcus sp., did not increase the risk of
recurrent infection. Conversely, infections caused by when Gram-negative bacilli, such as
Escherichia coli (15.8% vs. 5.2%, p = 0.036), Pseudomonas aeruginosa (44.7% vs. 9.1%, p =
<0.001) and Acinetobacter baumannii (26.3% vs. 8.4%, p = 0.005) presented higher risk for
treatment failure, on univariate analysis. On the other hand, habits such as smoking (p = 0.676),
Gustilo Grade-III open fracture (p = 0.602), time elapsed from admission to surgery (p = 0.532),
diagnosis of chronic osteomyelitis (p = 0.169), and even the positive tissue culture for
Streptococcus sp. (p = 0.051) were not associated with a significantly increased risk of
treatment failure of PTO.
Variables showing statistical significance and presenting clinical importance in univariate
analysis have been added to the multivariate Cox proportional hazard model (Table 3). Factors
that remained independently associated to recurrent infection in the multivariable analysis were
66
elderly patients, especially those with age ranging from 61 to 80 years [hazard ratio (HR) =
6.086, 95% confidence interval (CI) = 2.459;15.061, p <0.001], and above 80 years [HR =
9.975 (95% CI = 3.591;27.714), p <0.001]; need for intraoperative blood transfusion [HR =
2.239 (95% CI = 1.138;4.406), p = 0.020]; and positive bone and/or soft tissue culture for P.
aeruginosa [HR = 2.700 (95% CI = 1.370;5.319), p = 0.004].
Indeed, we have found a strong correlation between P. aeruginosa and treatment failure
of PTO. When P. aeruginosa was the recovered pathogen, disease-free survival was much
lower than that of S. aureus and Enterococcus sp. (28 months vs. 60 months vs. 59 months,
respectively, p = 0.002), on the Kaplan-Meier survival curve of all 192 patients with PTO
(Figure 2). Regarding the need of intraoperative blood transfusion, disease-free survival was of
1681 days for those who received red blood cell transfusion vs. 2136 days for those who did not
received transfusion (p = 0.003) (Figure 3).
Microbiological Findings
The frequencies of microorganisms isolated from bone and soft tissue cultures among
patients presenting PTO are showed in Table 4. Of the 300 positive cultures, Staphylococcus
aureus was isolated in 104 (34.7%) cases, of which 37 (12.3%) and 67 (22.3%) were
methicillin-resistant S. aureus (MRSA) and methicillin-sensitive S. aureus (MSSA),
respectively. Cultures yielded coagulase-negative staphylococci in only 6.3% (19/300). Three
most causative GNB identified were Pseudomonas aeruginosa (10.3%), Acinetobacter
baumannii (7.6%), and Citrobacter sp. (7%). In addition, tissue cultures yielded Candida
tropicalis in two different patients with PTO.
Discussion
Osteomyelitis after trauma occurs when microorganisms are inoculated into bone either
after an open fracture or during surgical management of closed fracture, to which tibia and
femur are the commonest site of infection (14). Depending upon the severity of the injury, PTO
may reach rates as higher as 50%, and failure to control the infection through aggressive
surgical debridement and culture-based antibiotic therapy may be limb-threatening and also
poses a substantial financial impact (15-20). Nevertheless, risk factors for recurrent infection
following surgical-clinical treatment of PTO have received few attentions in the medical
literature. The present study reported the outcome of 192 patients submitted to surgical and
antibiotic treatment for osteomyelitis that were frequently associated with high-energy traumas
(68.9%), and from which 38 (19.8%) experienced recurrent infection. We therefore focused
specifically on identifying significant predisposing factors for recurrence of osteomyelitis
following treatment of PTO. The results identified that elderly patients, intra-operative blood
67
transfusion and infections caused by Pseudomonas aeruginosa are independently associated
with substantially increased risk of treatment failure of PTO.
Considerable amount of data has been published regarding the incidence of osteomyelitis
following open and closed fractures, with rates ranging from 1% to up to 50% (2,14). In
contrast, data describing the success of PTO management is surprisingly scarce. In this case
series, 80.2% of patients were on remission after at least one year of follow up. Remission rate
of 82.1% was observed in a retrospective study of posttraumatic and postoperative osteomyelitis
affecting the distal tibia, ankle joint and foot (18), whereas similar results (76.7% of remission)
were achieved in a Colombian cohort study of patients diagnosed with osteomyelitis
predominantly due to bone fractures (11). Additionally, Tice et al. observed fewer rates of
remission (69.4%) among patients with contiguous chronic osteomyelitis manly associated with
soft tissue wounds or following surgery (90.8%) during a mean follow up of 27.5 months (10).
On the other hand, a much better remission rate (92%) was observed in a osteosynthesis-
associated infection Swiss single-center case-control study (9). Explaining these discrepancies
may be a complex task, but we hypothesize that some differences may have played a role
including patient’s characteristics, proportions of high-energy trauma-associated fractures,
surgical techniques and antibiotic therapy choices. For example, in the present study high-
energy trauma fractures (68.9%) due to road traffic accidents and need for more than one
surgical debridement (39.9%) was frequently observed, while uncommon in the Swiss study
population (9).
Major finding of this study is that independent factors for treatment failure after
posttraumatic osteomyelitis were primarily non-modifiable risk factors. Elderly patients with
age between 61 to 80 years face a six-fold greater risk to recur after PTO management, while
among patients above 80 years of age, the risk for failure reaches almost ten-fold. Furthermore,
there is a two-fold higher risk of recurrent infection for those receiving transfusion of allogenic
blood units, and 2.7-fold higher risk of treatment failure when infections were caused by P.
aeruginosa. In contrast, factors independently associated with recurrent infection in previous
publications were not in this study including, comorbidities such as smoking, lower limb
Gustilo II and III open fractures, high ASA scores, polymicrobial infection, multi-drug resistant
microorganisms such as MRSA, and antibiotics prescribed (9-14,18). Previous authors have
shown a strong association between older age and osteomyelitis due to a several different
reasons starting from the immunocompromised features of aging, higher frequency of
comorbidities (diabetes and peripheral vascular diseases), following orthopedic surgery such as
knee and hip replacement to the higher frequency of falls resulting in closed and open bone
fractures (10,20-21). Arias et al. recently found amidst other factors, a 1.3-fold higher risk of
recurrent osteomyelitis among patients older than 56 years of age (11). Notwithstanding, in the
68
current study significant risk factors might have been interdependent and inter-related. For
example, patients with femoral neck fractures submitted to bipolar hemiarthroplasty were
significantly associated with worse outcome, in the univariate analysis (21% vs. 3.2%). This
finding may have contributed to the higher rates of recurrence in the elderly patients, since
hemiarthroplasty is an option widely accepted for proximal femur fracture correction in the
elderly, and has been previously associated with increased risk of infection (22).
Large blood loss at the time of fracture or during and after surgery causing severe and
symptomatic anemia is the main clinical indication for red blood cell transfusion (23). In
addition, transfusion of allogenic blood units may reflect the severity of the injury, producing
extensive soft tissue damage and consequently serious bleeding. Notwithstanding, intra-
operative blood transfusion is not without side effects. Although controversial, previous studies
have associated allogenic blood transfusion with periprosthetic joint infection (24). In a recent
published meta-analysis aiming at identifying risk factors for hip and knee joint infection after
total joint arthroplasty, blood transfusion was significantly associated with infection (25).
Conversely, a Cochrane systematic review was unable to identify a strong association between
blood transfusion and wound infection following hip fracture trauma (26). Even though intra-
operative blood transfusion is independently associated with recurrent PTO in the present study,
this result may be interpreted cautiously. One may speculate that patients submitted to more
complex surgeries with prolonged operative time may be more likely to have received blood
transfusion. Nevertheless, significantly lower infection-free survival rate was observed among
patients who had received blood transfusion (infection-free survival rates was of 1681 days for
those who received red blood cell transfusion vs. 2136 days for those who did not received
transfusion).
Regardless the fact that Staphylococcus aureus (MSSA and MRSA) comprises by far the
commonest infecting organism isolated on cultures from PTO, the Gram-negative rod
Pseudomonas aeruginosa is likely to be identified on soft and bone cultures (3-7,14). Not only
open fractures are contaminated by a myriad of pathogenic Gram-negative bacteria, but also
secondary hospital-acquired osteomyelitis and implant-associated infection due to P.
aeruginosa has been increasingly diagnosed specially in developing countries large trauma
centers (4,6,27, 28). Through a microbiological perspective, the growing importance of
Pseudomonas causing osteomyelitis is by no means a surprise and may be easily justified by its
virulence factors, the exceptional capacity of forming biofilms on tissues and upon implant
surfaces and to its natural ability to prompt express full resistance to virtually all classes of
antibiotic used to treat bone infections (27,28). In this study, P. aeruginosa not only accounted
for the second most isolated bacteria on patients with PTO, but was also strongly associated to
69
recurrent infection in the multivariable analysis. Likewise, on the Kaplan-Meier curve disease-
free survival was much lower among patients presenting P. aeruginosa PTO than that of S.
aureus and Enterococcus sp. (28 months vs. 60 months vs. 59 months, respectively). To our
knowledge, few studies addressing osteoarticular infection were able to prove an independent
association between positive cultures with Pseudomonas with worse outcome, even so the
majority of these previous data assessed patients with prosthetic joint infections rather than
posttraumatic osteomyelitis (12,18,24,29-32). None the less, a retrospective study identified P.
aeruginosa as an independent factor for recurrence of orthopedic implant-associated infection
following surgeries for fractures, although there were only two recurrences among seven cases
of P. aeruginosa infection analyzed (9). Furthermore, the same study group reported only a
trend towards a lower remission rate for osteoarticular infection due to P. aeruginosa than
infections due to S. aureus (including MRSA) (27). Additionally, Tice et al. showed that when
osteomyelitis was caused by P. aeruginosa the risk of recurrence increased more than two-fold,
and they also identified a positive correlation between infection due to Pseudomonas with
amputation (10). Knowing that microbiology of osteomyelitis may have prognostic
implications, orthopedic surgeons and infectious diseases specialists should emphasize
preventive measures toward Gram-negative infections and prompt microbial diagnosis upon
clinical suspicious of PTO.
This single-center study has potential limitations including its retrospective design along
with the small number of recurrent patients (38/192) included. This may affect the performance
of multivariable-adjusted analysis to previously described important associations with recurrent
PTO including high-energy open fractures (11), presence of osteosynthesis on the site of
infection (9) and inappropriate use of antibiotics (10,12). However, disease-free survival
analysis over time was also performed in this study using univariate and multivariate Cox
regression analysis. The study was carried out at a single public institution in a developing
country medium-size city offering a specialized orthopedic care for local population, from
which results may not be applicable to other centers. However, a large single-center database of
orthopedic trauma surgeries (roughly 8,000) was used for this analysis. Recurrent PTO may
have been misdiagnosed over time due to the absence of typical signs and symptoms of
inflammation especially for osteosynthesis-associated infections, in which inflammatory blood
markers are usually unhelpful, and imaging tests are nonspecific (13,14). On the other hand,
follow-up of patients with PTO after hospital discharge and treatment completion is usually
performed by the same team of experienced orthopedics and infectious diseases specialists in an
outpatient setting within the same institution and therefore, this selection bias is considered well
controlled. Of course, recurrences of osteomyelitis have been described after many years
following definitive surgical and antibiotic treatment (14,15,32), thus an accepted minimal
70
follow up to study remission of PTO in the literature is lacking and difficult to accomplish (27).
In this study, a minimal follow-up time was one year, although a median follow-up time of 1395
days was observed, also limiting the selection of bias. Depending upon the microbial results,
recurrence may be classified as either relapse (original pathogen) or reinfection (new pathogen)
(10). Identify these differences would be important to set up individual preventive measures,
though this issue was not addressed in this study.
Despite these limitations, this single-center retrospective study revealed high rate of
recurrence following PTO and elderly patients, the need for intra-operative blood transfusion
and infection due to P. aeruginosa are significant predisposing factors for unfavorable outcome.
Future prospective multicenter randomized studies may corroborate these results.
71
FACTORSASSOCIATEDWITHTREATMENTFAILUREOFPOSTTRAUMATICCHRONICOSTEOMYELITIS
.
Fig 1. Flow diagram showing patient enrollment and follow-up throughout the trial.
1Excluded:lostoffollow-up
8.098patientsassessedforfollow-up
7510(92.7%)withclosedfractures
588(7.3%)withopenfractures
205patientspresentingPTO
12(5.9%)excluded:
-7previoushistoryofPTO
-5incompletemedicalrecords
193patientseligible
192patientsincludedinanalysisfortreatmentoutcomes
154assignedforcureofboneinfection
38patientsassignedforrecurrenceofboneinfection
72
Table 1. Demographic and injury characteristics of 193 patients associated with treatment remission and failure of PTOa. Demographic data N=193 (%)
Age (mean [range]) (years) 50 (16-88) Male sex (no. [%]) 133 (68.9) Schooling level <8 years 67 (34.7)
Comorbidities (no. [%]) Smoking 59 (30.5) Intraoperative hyperglycemia 58 (30.0)
Occupation (no. [%]) Farmer 26 (13.5) Driver (car, motorcycle, truck) 24 (12.5) Construction / Machine Operation 44 (22.8) Business 40 (20.7) Household activities 59 (30.5)
Types of injury (no. [%]) Car crash accident 110 (57.0) Fall from height (< 1m) 57 (29.5) Football related injury 3 (1.5) Other falls 18 (9.6) Other injuries 8 (4.0) Penetrating injury by a wooden foreign body 3 (1.5)
High-energy injury 133 (68.9) Gustilo & Anderson Classification for open fractures 73 (37.8)
Type-I (no. [%]) 14 (19.2) Type-II (no. [%]) 23 (31.5) Type-III (no. [%]) 36 (49.3)
Closed fracture 120 (62.2) More of one surgical debridement 77 (39.9) Polytrauma 46 (23.8) American Society of Anesthesiologists score (no. [%])
ASAb I – II (1 or 2) 40 (20.7) ASAb III – IV (>2) 153 (79.3)
Intraoperative blood transfusion 66 (34.2) Duration of surgery (media [range]) (hours) 2.61 (1-8) Infected Fracture Location (no. [%])
Upper limbs 44 (22.8) Lower limbs 154 (79.2) Collarbone 7 (3.6) Humerus 12 (6.2) Radio 13 (6.7) Ulna 16 (8.2) Hands 3 (1.5) Femur 59 (30.5) Knee 9 (4.6) Tibia 56 (29) Fibula 11 (5.7) Foot 19 (9.8)
PTOa:posttraumaticosteomyelitis;ASAb:AmericanSocietyofAnesthesiologists.
73
Table 4: Frequency of micro-organisms yielded from cultures
Microrganisms N (%) Staphylococcus aureus 104 (34.6) MRSAa 37 (12.3) MSSAb 67 (22.3) Pseudomonas aeruginosa 31 (10.3) Acinetobacter baumannii 23 (7.6) Enterococcus sp. 22 (7.3) Citrobacter sp. 21 (7.0) Klebsiella pneumoniae 20 (6.6) CNSc 19 (6.3) Escherichia coli 14 (4.6) Proteus sp 14 (4.6) Candida tropicalis 2 (0.6) Othersd 30 (10.0) a MRSA-Methicillin-resistant Staphylococcus aureus; b MSSA- Methicillin-sensitive Staphylococcus aureus; c CNS-Coagulase-negative Staphylococci; d Others - Alcaligenes sp., Enterobacter sp., Morganella morganii, Providencia sp., Serratia sp., Stenotrophomonas maltophilia, Streptococcus agalactie, Streptococcus viridans
74
Table 2. Univariate analysis of risk factors associated with treatment failure of PTOa. Characteristics Failure
No. (%) (N = 38)
Remission No. (%) (N = 154)
P valuec
Demographic data Age (median [range]) (yr) 70 (16 – 88) 40.5 (11 – 86) <0.001 <40 years 9 (23.6) 77 (50) 41 – 60 years 6 (15.8) 55 (35.7) 61 – 80 years 14 (37) 20 (13) > 80 years 9 (23.6) 2 (1.3) Male sex (no. [%]) 19 (50) 113 (73.4) 0.005 Household activities (no. [%]) 20 (52.6) 39 (25.3) 0.001 Comorbidities (no. [%]) Smoking 11 (29.0) 50 (32.5) 0.676 Fall from height (no. [%]) 23 (60.5) 34 (22.0) <0.001 Grade-III open fracture (no. [%]) 6 (15.8) 30 (19.5) 0.602 Admission to surgery t >3h (no. [%]) 36 (94.7) 139 (90.2) 0.532 >1 surgery debridement (no. [%]) 23 (60.5) 54 (35.0) 0.004 Need for blood transfusion (no. [%]) 23 (60.5) 43 (28.0) <0.001 Lower limb fractures (no. [%]) 37 (97.3) 116 (75.3) 0.002 Bipolar hip prosthesis (no. [%]) 8 (21.0) 5 (3.2) <0.001 ASA score ASAb I - II (no. [%]) 30 (79.0) 145 (94.1)
0.007 ASA III - IV (no. [%]) 9 (12.3) 8 (7.3) Chronic osteomyelitis (no. [%]) 16 (42.1) 84 (54.5) 0.169 Staphylococcus aureus culture (no. [%]) 25 (13%) 79 (41.1%) 0.010 Streptococcus sp. culture (no. [%]) 4 (10.5) 4 (2.6) 0.051 Enterococcus sp. culture (no. [%]) 8 (21.1) 14 (9.1) 0.048 Escherichia coli culture (no. [%]) 6 (15.8) 8 (5.2) 0.036 Pseudomonas aeruginosa culture (no. [%]) 17 (44.7) 14 (9.1) <0.001 Acinetobacter baumannii culture (no. [%]) 10 (26.3) 13 (8.4) 0.005 PTOa: posttraumatic osteomyelitis; ASAb: American Society of Anesthesiologists; cPatient characteristics were summarized as frequencies and percentages or median and compared using the Pearson Chi-Square test or Fisher's exact test as appropriate to nominal variables and Mann-Whitney Test or T-Test as appropriate to continuous variables. All tests were two sided, and P values of <0.05 were considered statistically significant.
75
Table 3: Multivariate Cox proportional hazard model of risk factors associated with treatment failure of PTOd. Variables HRa (CI 95%) P Valuec
Ageb 61 – 80 years 6.086 (2.459; 15.061) <0.001 >80 years 9.975 (3.591; 27.714) <0.001 Need for blood transfusion 2.239 (1.138; 4.406) 0.020 Pseudomonas aeruginosa culture 2.700 (1.370; 5.319) 0.004 aHazard Ratio; bLess than or equal 40 years as reference; cAll tests were two sided, and P values of <0.05 were considered statistically significant. PTOd: posttraumatic osteomyelitis;
Figure 2. Kaplan–Meier estimates of the cumulative risk of failure according to the treatment assessed at 100 months’ follow-up. The log rank test compared two survivalcurvesacrossmultiple timepoints.Patients who had PTO caused by P. aeruginosa had lower disease-freesurvivalthanbyS.aureusandEnterococcussp(p=0.002).
76
Figure3.Kaplan–Meier estimates of the cumulative risk of failure according to the treatment assessed at 100 months’ follow-up. The log rank test compared two survivalcurvesacrossmultiple time points.Patients who need of blood transfusion had lower disease-free survival than those who did not need transfusion (p=0.003).
77
References
1. Uçkay I, Hoffmeyer P, Lew D, Pittet D. Prevention of surgical site infections in
orthopaedic surgery and bone trauma: state-of-the-art update. J Hosp Infect 2013;84(1):
5-12.
2. Li GQ, Guo FF, Ou Y, Dong GW, Zhou W. Epidemiology and outcomes of surgical
site infections following orthopedic surgery. Am J Infect Control 2013 Dec;41:1268-71.
3. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA et al. The
microbiology of chronic osteomyelitis: Prevalence of resistance to common empirical
anti-microbial regimens. J Infect 2010 May;60:338-43.
4. Yano MH, Klautau GB, da Siva CB, Nigro S, Avanzi O, Mercadante MT et al.
Improved Diagnosis of Infection Associated with Osteosynthesis by Use of Sonication
of Fracture Fixation Implants. J Clin Microbiol 2014 Dec;52 (12): 4176-82.
5. Kremers HM, Nwojo ME, Ransom JE, Wood-Wentz CM, Melton LJ 3rd, Huddleston
PM 3rd. Trends in the Epidemiology of Osteomyelitis: a population-based study, 1969
to 2009. J Bone Joint Surg Am 2015 May;97 (10):837-45.
6. Jiang N, Ma YF, Jiang Y, Zhao XQ, Xie GP, Hu YJ et al.
Clinical Characteristics and Treatment of Extremity Chronic Osteomyelitis in Southern
China: A Retrospective Analysis of 394 Consecutive Patients. Medicine 2015 Oct;94
(42): 1-7.
7. Museru LM, Mcharo CN. Chronic osteomyelitis: a continuing orthopaedic challenge in
developing countries. Int Orthop. 2001;25(2): 127-31.
8. Jorge LS, Chueire AG, Rossit AR. Osteomyelitis: a current challenge. Braz J Infect Dis
2010;14(3):310-5.
9. Al-Mayahi M, Betz M, Müller DA, Stern R, Tahintzi P, Bernard L, et al. Remission rate
of implant-related infections following revision surgery after fractures. Int Orthop 2013
Nov;37:2253–8.
10. Tice AD, Hoaglund PA, Shoultz DA. Risk factors and treatment outcomes in
osteomyelitis. J Antimicrob Chemother 2003 May;51(5):1261–8.
11. Arias CA, Betancur MCT, Pinzón MA, Arango DC, Taffur CAC, Prada EC.
Differences in the Clinical Outcome of Osteomyelitis by Treating Specialty:
Orthopedics or Infectology. PLoS ONE 2015;10(12):1-13.
12. Senneville E, Joulie D, Legout L, Valette M, Dezèque H, Beltrand E, et al. Outcome
and Predictors of Treatment Failure in Total Hip/Knee Prosthetic Joint Infections due to
Staphylococcus aureus. Clin Infect Dis 2011 Aug;53(4):334–40.
78
13. Arnold R, Rock C, Croft L, Gilliam BL, Morgan DJ. Factors Associated with Treatment
Failure in Vertebral Osteomyelitis Requiring Spinal Instrumentation. Antimicrob
Agents Chemother 2014;58(2):880-4.
14. Patzakis MJ, Zalavras CG. Chronic Posttraumatic Osteomyelitis and Infected Nonunion
of the Tibia: Current Management Concepts. J Am Acad Orthop Surg 2005 Oct;13:417-
27.
15. Trampuz A, Zimmerli W. Diagnosis and treatment of infections associated with
fracture-fixation devices. Injury 2006 May;37: Suppl 2:S59-S66.
16. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in long bones. J Bone Joint Surg Am
2004 Oct;86-A(10): 2305-18.
17. Ovaska MT, Mäkinen TJ, Madanat R, Huotari K, Vahlberg T, Hirvensalo E et al. Risk
Factors for Deep Surgical Site Infection Following Operative Treatment of Ankle
Fractures. J Bone Joint Surg Am 2013 Fev;95(4):348 -53.
18. Malizos KN, Gougoulias NE, Dailiana ZH, Varitimidis S, Bargiotas KA, Paridis D.
Ankle and foot osteomyelitis: treatment protocol and clinical results. Injury 2010
Mar;41(3): 285-93.
19. Sanders J, Mauffrey C. Long bone osteomyelitis in adults: fundamental concepts and
current techniques. Orthopedics 2013 May;36(5):368-75.
20. Huang CC, Tsai KT, Weng SF, Lin HJ, Huang HS, Wang JJ et al. Chronic
osteomyelitis increases long-term mortality risk in the elderly: a nationwide population-
based cohort study Huang et al. BMC Geriatr 2016 Mar;16:72 doi 10.1186/s12877-016-
0248-8.
21. Cunha BA. Osteomyelitis in elderly patients. Clin Infect Dis 2002 Aug;35(3):287-93.
22. Gallardo-Calero I, Larrainzar-Coghen T, Rodriguez-Pardo D, Pigrau C, Sánchez-Raya
J, Amat C et al. Increased infection risk after hip hemiarthroplasty in institutionalized
patients with proximal femur fracture. Injury 2016 Apr;47(4):872-6.
23. Tartter PI. Blood transfusion and postoperative infections. Transfusion 1989 Mar;29
(5): 456–9.
24. Pulido L, Ghanem E, Joshi A, Purtill J, Parvizi J. Periprosthetic joint infection: the
incidence, timing, and predisposing factors. Clin Orthop Relat Res 2008
Jul;466(7):1710-5.
25. Zhu Y, Zhang F, Chen W, Liu S, Zhang Q, Zhang Y. Risk
factors for periprosthetic joint infection after total joint arthroplasty: a systematic
review and meta-analysis. J Hosp Infect 2015 Feb;89(2):82-9.
79
26. Brunskill SJ, Millette SL, Shokoohi A, Pulford EC, Doree C, Murphy MF et al.
Red blood cell transfusion for people undergoing hip fracture surgery. Cochrane
Database Syst Rev 2015 Apr;(4):CD009699. doi:10.1002/14651858.CD009699.pub2.
27. Seghrouchni K, van Delden C, Dominguez D, Benkabouche M, Bernard L, Assal M et
al. Remission after treatment of osteoarticular infections due to Pseudomonas
aeruginosa versus Staphylococcus aureus: a case-controlled study. Int Orthop 2012
May;36(5):1065–71.
28. Zuluaga AF, Galvis W, Saldarriaga JG, Agudelo M, Salazar BE, Vesga O. Etiologic
diagnosis of chronic osteomyelitis: a prospective study. Arch Intern Med 2006
Jan;166(1):95–100.
29. Hsieh PH, Lee MS, Hsu KY, Chang YH, Shih HN, Ueng SW. Gram-negative prosthetic
joint infections: risk factors and outcome of treatment. Clin Infect Dis 2009
Oct;49(7):1036–43.
30. Martínez-Pastor JC, Muñoz-Mahamud E, Vilchez F, García-Ramiro S, Bori G, Sierra J
et al. Outcome of acute prosthetic joint infections due to gram-negative bacilli treated
with open debridement and retention of the prosthesis. Antimicrob Agents Chemother
2009 Nov; 53(11):4772–7.
31. Rodríguez-Pardo D, Pigrau C, Lora-Tamayo J, Soriano A, del Toro MD, Cobo J et al.
Gram-negative prosthetic joint infection: outcome of a debridement, antibiotics and
implant retention approach. A large multicentre study. Clin Microbiol Infect 2014
Nov;20(11):O911-9.
32. Uçkay I, Assal M, Legout L, Rohner P, Stern R, Lew D et al. Recurrent osteomyelitis
caused by infection with different bacterial strains without obvious source of
reinfection. J Clin Microbiol 2006 Mar;44(3):1194–6.
80
5. Considerações Finais
Esse estudo de coorte retrospectivo de cinco anos em um hospital terciário concluiu que a
infecção polimicrobiana pós-traumática foi identificada em mais de um terço dos casos.
Pacientes idosos, as atividades de trabalho que envolvem a agricultura, o número de
desbridamentos cirúrgicos e a transfusão de glóbulos vermelhos foram fatores de risco
independentes para osteomielite polimicrobiana pós-traumática na análise multivariada. As
culturas microbiológicas identificaram, na maioria das vezes, bacilos Gram-negativos, mas
Staphylococcus aureus permanece o principal micro-organismo isolado. Certamente, a
identificação dos fatores predisponentes para osteomielite pós-traumática polimicrobiana pode
auxiliar o médico na escolha da terapia antimicrobiana mais apropriada e da modalidade
cirúrgica mais segura.
Em relação ao segundo artigo, os resultados mostraram alta taxa de recorrência das
osteomielites pós-traumáticas em pacientes idosos, que necessitaram de transfusão de sangue no
período intra-operatório e nas infecções causadas por P. aeruginosa.
Os estudos ressaltaram a importância de um atendimento multidisciplinar no Serviço de
Ortopedia e Traumatologia, que envolva especialidades médicas, não só cirurgião ortopédico e
vascular, mas também geriatra, infectologista, microbiologista e radiologista, além de outros
serviços, tais como enfermagem, serviço social e psicologia.
O diagnóstico e tratamento precoces e rápidos permanecem essenciais, a fim de se evitar
as complicações da cronificação da osteomielite.
O conhecimento do comportamento das diferentes bactérias é essencial para prevermos a
evolução de cada caso e a transfusão de concentrado de hemácias e suas potenciais complicação
devem ser avaliadas previamente à sua indicação.
A formação de médicos clínicos e principalmente cirurgiões deve conter a importância do
envelhecimento populacional devido ao aumento da sobrevida em geral. Condutas terapêuticas
rápidas nessa população são fundamentais para a manutenção da vida com qualidade.
Ambos os estudos mostraram resultados locais até então nunca divulgados, definindo
uma população de traumas ortopédicos, com poucos estudos publicados.
Estudos prospectivos multicêntricos devem ser encorajados a fim de se confirmar nossos
resultados.
81
6. Referências Bibliográficas
1. Berbari EF, Steckelberg JM, Osmon DR. Osteomyelitis. In: Mandell GL, Bennett JE, Dolin R. Principles and Practice of Infectious Diseases. 6th Ed. Phyladelphia: Churchill Livingstone; 2005:1322-32.
2. Ciampolini J, Harding KG. Pathophysiology of chronic bacterial osteomyelitis. Why do antibiotics fail so often? Postgrad Med J 2000;76:479-83.
3. Lew DP, Waldvogel FA. Osteomyelitis. N Engl J Med 1997; 336:999-1007. 4. Waldvogel FA, Medoff G, Swartz MN. Osteomyelitis: a review of clinical features,
therapeutic considerations and unusual aspects. N Engl J Med 1970;282(4):198-206. 5. Lipsky BA, Berendt AR, Deery HG, Embil JM, Joseph WS, Karchmer AW et al.
Diagnosis and Treatment of Diabetic Foot Infections. CID 2004; 39:885–910. 6. Frykberg RG, Zgonis T, Armstrong DG, Driver VR, Giurini JM, Kravitz SR et al.
Diabetic Foot Disorders: A Clinical Practice Guideline (2006 revision). J Foot Ankle Surg 2006:45(5):S1-66.
7. Gustilo R, Anderson J. Prevention of infection in the treatment of one thousand and twenty-five open fractures of long bones. J Bone Joint Surg Am 1976;58: 453-8.
8. Lima ALLM, Zumiotti AV, Uip DE, Silva JS. Fatores preditivos de infecção em 9. pacientes com fraturas expostas nos membros inferiores. Acta Ortop Bras
2004;12(1):32-9. 10. Brause BD. Infections with Prostheses in Bonés and Joints. In: Mandell GL, Bennett JE,
Dolin R. Principles and Practice of Infectious Diseases. 6th Ed. Phyladelphia: Churchill Livingstone; 2005:1332-7.
11. Ehrlich GD, Stoodley P, Kathju S, Zhao Y, McLeod BR, Balaban N et al. Engineering Approaches for the Detection and Control of Orthopaedic Biofilm Infections. Clin Orthop Relat Res 2005;437:59–66.
12. Scales J F, Herschell W. Perspex (methylmethacrylate) in orthopaedics. Brit Med J 1945;2:245-9.
13. Judet J, Judet R. Use of artificial femoral head for arthroplasty of hip joint. J Bone Joint Surg (Br) 1950;32:166-71.
14. Petty W. The effect of methylmethacrylate on bacterial inhibiting properties of normal human serum. Clin Orthop 1978;132:266-77.
15. Petty W. The effect of methylmethacrylate on bacterial phagocytosis and killing by human polymorphonuclear leukocytes. J Bone Joint Surg Am 1978;60:752-7.
16. 15. Gristina A G. Biomaterial-centered infection; microbial adhesion versus tissue integration. Science 1987;237:1588-95.
17. Van de Belt H, Neut D, Schenk W, van Horn JR, van der Mei HC, Busscher HJ. Infection of orthopedic implants and the use of antibiotic-loaded bone cements. Acta Orthop Scand 2001;72(6):557–71.
18. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA ET el. The Microbiology of chronic osteomyelitis: Prevalence of resistance to common empirical anti-microbial regimes. J Infect 2010;60:338-43.
19. Tice AD, Pamela A, Hoaglund PA, Shoultz DA. Outcomes of osteomyelitis among patients treated with outpatient parenteral antimicrobial therapy. Am J Med 2003;114:723-8.
20. Donlan RM, Costerton JW. Biofilms: Survival Mechanisms of Clinically Relevant Microorganisms. Clin Microbiol Rev 2002;15(2):167–93.
21. 20. Dunne Jr WM. Bacterial Adhesion: Seen Any Good Biofilms Lately? Clin Microbiol Rev 2002;15(2):155–66.
22. Zimmerli W, Trampuz A, Ochsner PE. Prosthetic-Joint Infections. N Engl J Med 2004;351:1645-54.
23. Darley ESR, MacGowan AP. Antibiotic treatment of Gram-positive bone and joint infections. JAC 2004;53:928–35.
82
24. Zuluaga AF, Galvis W, Jaimes F, Vesga O. Lack of microbiological concordance between bone and non-bone specimens in chronic osteomyelitis: an observational study. BMC Infectious Diseases 2002:1-7. [citado ano mês dia]. Disponível em: URL: http://www.biomedcentral.com/1471-2334/2/8.
25. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in Long Bones. J Bone Joint Surg 2004;86(10):2305-18.
26. Zhou J, Li Y, Wang QK, Pollak AN, Slobogean GP. Status of road safety and injury burden: China. J Orthop Trauma 2014;28(Suppl 1):S41-2.
27. Yano MH, Klautau GB, da Siva CB, Nigro S, Avanzi O, Mercadante MT et al. Improved Diagnosis of Infection Associated with Osteosynthesis by Use of Sonication of Fracture Fixation Implants. J Clin Microbiol 2014;52(12):4176-82.
28. Nan Jiang N, Ma Y, Jiang Y, Zhao X, Xie G, Hu Y et al. Clinical Characteristics and Treatment of Extremity Chronic Osteomyelitis in Southern China. Medicine 2015;94(42):1-7.
29. Gosselin RA, Roberts I, Gillespie WJ. Antibiotics for preventing infection in open limb fractures. Cochrane Database Syst Rev 2004;(1):1-27.
30. Darouiche RO. Treatment of Infections Associated with Surgical Implantes. N Engl J Med 2004;350:1422-9.
31. Morris DS, Rohrbach J, Sandaram LMT, Sonnad S, Sarani B, Pascual J et al. Early hospital readmission in the trauma population: Are the risk factors different? Injury 2014;45(1):56-60.
32. Trampuz A, Zimmerli W. Diagnosis and treatment of infections associated with fracture- fixation devices. Injury 2006;37:S59-S66.
33. Gustilo RB, Merkow RL, Templeman D. The management of open fractures. J Bone Joint Surg Am 1990;72(2):299-304.
34. Brady RA, Leid JG, Costerton JW, Shirtliff ME. Osteomyelitis: Clinical Overview and Mechanisms of Infection Persistence. Clin Microbiol Newsl 2006;28(9):65-72.
35. Kremers HM, Nwojo ME, Ransom JE, Wood-Wentz CM, Melton III LJ, Huddleston III PM. Trends in the Epidemiology of Osteomyelitis. J Bone Joint Surg Am 2015;97:837-45.
36. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in long bones. J Bone Joint Surg Am 2004;86(10):2305-18.
37. Uçkay I, Hoffmeyer P, Lew D, Pittet D. Prevention of surgical site infections in orthopaedic surgery and bone trauma: state-of-the-art update. J Hosp Infect 2013;84:5-12.
38. Li G, Guo F, Ou Y, Dong G, Zhou W. Epidemiology and outcomes of surgical site infections following orthopedic surgery. Am J Infect Control 2013;41:1268-71.
39. Centers for Disease Control and Prevention [homepage na internet]. CDC/NHSN Surveillance Definitions for Specific Types of Infections [access on February 14, 2016]. Available in: www.cdc.gov.
40. Lipsky BA, Berendt AR. Osteomyelitis. ACP Medicine. Decker Intellectual Properties; 2010, p. 1-20. DOI 10.2310/7900.1137.
41. Lipsky BA, Berendt AR, Cornia PB, Pile JC, Peters EJG, Armstrong DG et al. 2012 Infectious Diseases Society of America Clinical Practice. Guideline for the Diagnosis and Treatment of Diabetic Foot Infections. Clin Infect Dis 2012;54(12):132-73.
42. Malizos KN, Gougoulias NE, Dailiana ZH, Varitimidis S, Bargiotas KA, Paridis D. Ankle and foot osteomyelitis: treatment protocol and clinical results. Injury
83
2010;41(3):285-93. 43. Museru LM, Mcharo CN. Chronic osteomyelitis: a continuing orthopaedic challenge in
developing countries. Int Orthop 2001;25(2):127-31. 44. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA et al. The
microbiology of chronic osteomyelitis: Prevalence of resistance to common empirical anti-microbial regimens. Journal of Infection 2010;60:338-43.
45. Ali MH, Hoekzema NA, Bakleh M, Shin AY, Osmon DR. The Microbiology and Risk of Infection Following Open, Agricultural Upper Extremity Injuries. J Hand Surg Am 2008;33(1):87-93.
46. Tartter PI. Blood transfusion and postoperative infections. Transfusion 1989;29 (5):456–9.
47. Carson JL, Altman DG, Duff A, Noveck H, Weinstein MP, Sonnenberg FA et al. Risk of bacterial infection associated with allogeneic blood transfusion among patients undergoing hip fracture repair. Transfusion 1999;39(7):694-700.
48. Patzakis MJ, Zalavras CG. Chronic posttraumatic osteomyelitis and infected nonunion of the tibia: current management concepts. J Am Acad Orthop Surg 2005;13(6):417-27.
49. Glass GE, Barrett SP, Sanderson F, Pearse MF, Nanchahal J. The microbiological basis for a revised antibiotic regimen in high-energy tibial fractures: preventing deep infections by nosocomial organisms. J Plast Reconstr Aesthet Surg 2011;64(3):375-80.
50. Johnson EN, Burns TC, Hayda RA, Hospenthal DR, Murray CK. Infectious complications of open type III tibial fractures among combat casualties. Clin Infect Dis 2007;45(4):409-15.
51. Lew DP, Waldvogel FA. Osteomyelitis. Lancet 2004;364 (9431): 369-79. 52. Hudson MC, Ramp WK, Nicholson NC, Williams AS, Nousiainen MT. Internalization
of Staphylococcus aureus by cultured osteoblasts. Microbial Pathogenesis 1995;19:409–19.
53. Guzmán-Blanco M, Mejía C, Isturiz R, Alvarez C, Bavestrello L, Gotuzzo E, Labarca J, Luna CM, Rodríguez-Noriega E, Salles MJ, Zurita J, Seas C. Epidemiology of methicillin-resistant Staphylococcus aureus (MRSA) in Latin America. Int J Antimicrob Agents 2009;34(4): 304-8. doi: 10.1016/j.ijantimicag.2009.06.005
33. Uçkay I, Hoffmeyer P, Lew D, Pittet D. Prevention of surgical site infections in
orthopaedic surgery and bone trauma: state-of-the-art update. J Hosp Infect 2013;84(1):
5-12.
34. Li GQ, Guo FF, Ou Y, Dong GW, Zhou W. Epidemiology and outcomes of surgical
site infections following orthopedic surgery. Am J Infect Control 2013 Dec;41:1268-71.
35. Sheehy SH, Atkins BA, Bejon P, Byren I, Wyllie D, Athanasou NA et al. The
microbiology of chronic osteomyelitis: Prevalence of resistance to common empirical
anti-microbial regimens. J Infect 2010 May;60:338-43.
36. Yano MH, Klautau GB, da Siva CB, Nigro S, Avanzi O, Mercadante MT et al.
Improved Diagnosis of Infection Associated with Osteosynthesis by Use of Sonication
of Fracture Fixation Implants. J Clin Microbiol 2014 Dec;52 (12): 4176-82.
84
37. Kremers HM, Nwojo ME, Ransom JE, Wood-Wentz CM, Melton LJ 3rd, Huddleston
PM 3rd. Trends in the Epidemiology of Osteomyelitis: a population-based study, 1969
to 2009. J Bone Joint Surg Am 2015 May;97 (10):837-45.
38. Jiang N, Ma YF, Jiang Y, Zhao XQ, Xie GP, Hu YJ et al.
Clinical Characteristics and Treatment of Extremity Chronic Osteomyelitis in Southern
China: A Retrospective Analysis of 394 Consecutive Patients. Medicine 2015 Oct;94
(42): 1-7.
39. Museru LM, Mcharo CN. Chronic osteomyelitis: a continuing orthopaedic challenge in
developing countries. Int Orthop. 2001;25(2): 127-31.
40. Jorge LS, Chueire AG, Rossit AR. Osteomyelitis: a current challenge. Braz J Infect Dis
2010;14(3):310-5.
41. Al-Mayahi M, Betz M, Müller DA, Stern R, Tahintzi P, Bernard L, et al. Remission rate
of implant-related infections following revision surgery after fractures. Int Orthop 2013
Nov;37:2253–8.
42. Tice AD, Hoaglund PA, Shoultz DA. Risk factors and treatment outcomes in
osteomyelitis. J Antimicrob Chemother 2003 May;51(5):1261–8.
43. Arias CA, Betancur MCT, Pinzón MA, Arango DC, Taffur CAC, Prada EC.
Differences in the Clinical Outcome of Osteomyelitis by Treating Specialty:
Orthopedics or Infectology. PLoS ONE 2015;10(12):1-13.
44. Senneville E, Joulie D, Legout L, Valette M, Dezèque H, Beltrand E, et al. Outcome
and Predictors of Treatment Failure in Total Hip/Knee Prosthetic Joint Infections due to
Staphylococcus aureus. Clin Infect Dis 2011 Aug;53(4):334–40.
45. Arnold R, Rock C, Croft L, Gilliam BL, Morgan DJ. Factors Associated with Treatment
Failure in Vertebral Osteomyelitis Requiring Spinal Instrumentation. Antimicrob
Agents Chemother 2014;58(2):880-4.
46. Patzakis MJ, Zalavras CG. Chronic Posttraumatic Osteomyelitis and Infected Nonunion
of the Tibia: Current Management Concepts. J Am Acad Orthop Surg 2005 Oct;13:417-
27.
47. Trampuz A, Zimmerli W. Diagnosis and treatment of infections associated with
fracture-fixation devices. Injury 2006 May;37: Suppl 2:S59-S66.
48. Lazzarini L, Mader JT, Calhoun JH. Osteomyelitis in long bones. J Bone Joint Surg Am
2004 Oct;86-A(10): 2305-18.
49. Ovaska MT, Mäkinen TJ, Madanat R, Huotari K, Vahlberg T, Hirvensalo E et al. Risk
Factors for Deep Surgical Site Infection Following Operative Treatment of Ankle
Fractures. J Bone Joint Surg Am 2013 Fev;95(4):348 -53.
85
50. Malizos KN, Gougoulias NE, Dailiana ZH, Varitimidis S, Bargiotas KA, Paridis D.
Ankle and foot osteomyelitis: treatment protocol and clinical results. Injury 2010
Mar;41(3): 285-93.
51. Sanders J, Mauffrey C. Long bone osteomyelitis in adults: fundamental concepts and
current techniques. Orthopedics 2013 May;36(5):368-75.
52. Huang CC, Tsai KT, Weng SF, Lin HJ, Huang HS, Wang JJ et al. Chronic
osteomyelitis increases long-term mortality risk in the elderly: a nationwide population-
based cohort study Huang et al. BMC Geriatr 2016 Mar;16:72 doi 10.1186/s12877-016-
0248-8.
53. Cunha BA. Osteomyelitis in elderly patients. Clin Infect Dis 2002 Aug;35(3):287-93.
54. Gallardo-Calero I, Larrainzar-Coghen T, Rodriguez-Pardo D, Pigrau C, Sánchez-Raya
J, Amat C et al. Increased infection risk after hip hemiarthroplasty in institutionalized
patients with proximal femur fracture. Injury 2016 Apr;47(4):872-6.
55. Tartter PI. Blood transfusion and postoperative infections. Transfusion 1989 Mar;29
(5): 456–9.
56. Pulido L, Ghanem E, Joshi A, Purtill J, Parvizi J. Periprosthetic joint infection: the
incidence, timing, and predisposing factors. Clin Orthop Relat Res 2008
Jul;466(7):1710-5.
57. Zhu Y, Zhang F, Chen W, Liu S, Zhang Q, Zhang Y. Risk
factors for periprosthetic joint infection after total joint arthroplasty: a systematic
review and meta-analysis. J Hosp Infect 2015 Feb;89(2):82-9.
58. Brunskill SJ, Millette SL, Shokoohi A, Pulford EC, Doree C, Murphy MF et al.
Red blood cell transfusion for people undergoing hip fracture surgery. Cochrane
Database Syst Rev 2015 Apr;(4):CD009699. doi:10.1002/14651858.CD009699.pub2.
59. Seghrouchni K, van Delden C, Dominguez D, Benkabouche M, Bernard L, Assal M et
al. Remission after treatment of osteoarticular infections due to Pseudomonas
aeruginosa versus Staphylococcus aureus: a case-controlled study. Int Orthop 2012
May;36(5):1065–71.
60. Zuluaga AF, Galvis W, Saldarriaga JG, Agudelo M, Salazar BE, Vesga O. Etiologic
diagnosis of chronic osteomyelitis: a prospective study. Arch Intern Med 2006
Jan;166(1):95–100.
61. Hsieh PH, Lee MS, Hsu KY, Chang YH, Shih HN, Ueng SW. Gram-negative prosthetic
joint infections: risk factors and outcome of treatment. Clin Infect Dis 2009
Oct;49(7):1036–43.
62. Martínez-Pastor JC, Muñoz-Mahamud E, Vilchez F, García-Ramiro S, Bori G, Sierra J
et al. Outcome of acute prosthetic joint infections due to gram-negative bacilli treated
86
with open debridement and retention of the prosthesis. Antimicrob Agents Chemother
2009 Nov; 53(11):4772–7.
63. Rodríguez-Pardo D, Pigrau C, Lora-Tamayo J, Soriano A, del Toro MD, Cobo J et al.
Gram-negative prosthetic joint infection: outcome of a debridement, antibiotics and
implant retention approach. A large multicentre study. Clin Microbiol Infect 2014
Nov;20(11):O911-9.
64. Uçkay I, Assal M, Legout L, Rohner P, Stern R, Lew D et al. Recurrent osteomyelitis
caused by infection with different bacterial strains without obvious source of
reinfection. J Clin Microbiol 2006 Mar;44(3):1194–6.