Monografia de Parasitas
-
Upload
larry-oscar-chani-paucar -
Category
Documents
-
view
91 -
download
0
description
Transcript of Monografia de Parasitas

1
I. INTRODUÇÃO:
O presente é uma revisão bibliográfica, procurando-se sintetizar os
conhecimentos prévios com as novas investigações sobre os parasitas,
incluindo-se variadas imagens em diversos estágios do ciclo biológico em que
o homem é-o hospedeiro intermediário o definitivo, podendo variar
dependendo da parasita. Em realidade as parasitas que afetam aos homens
compreendem inumeráveis espécies, nesta revisão só apenas se abordaram
as que são transmitidas pelos alimentos, que pelo geral é de origem animal,
isto porque os animais domésticos são frequentemente hospedeiros
intermediários e finais. Mais também os alimentos de origem vegetal podem
transmitir parasitas, neste caso a transmissão é por má manipulação, isto
também implica aos alimentos processados, onde o manipulador de alimentos
é o responsável pela contaminação dos alimentos.
Então as parasitas que afetam ao homem, e que são transmitidas pelos
alimentos estão compreendidas em três grandes grupos. O primeiro grupo são
os Protozoários, na qual compreende seis gêneros importantes desde o ponto
de vista alimentar, O segundo são os Platelmintos, que tem um numero igual
de gêneros do que o anterior e o terceiro grupo são Nematelmintos, que
compreendem só três gêneros de duas Classes. Por tanto a presente revisão
bibliográfica esta dividida em três capítulos segundo os grupos, subcapítulos
que compreende os gêneros e as espécies de interesse.

2
II. PROTOZOÁRIOS
Pertencesse ao Reino Protista, que compreende também as algas e aos
fungos flagelados. Eles são os menores e mais primitivas formas de animais.
Desde o ponto de vista alimentar, seis gêneros são os mais importantes:
2.1. O Gênero Giárdia
Gállego, 2007 indica que a descrições das características de Giardia
intestinalis em nível genérico não são necessárias porque todas as espécies
deste gênero mostram a morfologia similar. Podem-se encontrar citadas em
ocasiões como G. duodenalis, G. lamblia ou como a primeira antes
mencionada que é a denominação correta.
Segundo a descrição de James 2005 sobre a morfologia das células deste
protozoário que é chamado de Trofozoítas, ele menciona que produzem
cistos, que é a primeira forma na agua e em alimentos, têm forma de pêra com
um tamanho de 8 a 20 μm de comprimento e 5 a 12 μm de largura. Os
Trofozoítas têm oito flagelos que permitem a sua motilidade em forma de
«folha caindo».
Figura 1. Giárdia intestinalis em estagio de Trofozoíta, a. visto frontal, b. visto
de perfil, c. mostrando o disco Antero - Ventral. d. cisto, e. Trofozoíta fixado
sobre um entorócitos. (Gállego, 2007)

3
A agua é a fonte mais comum de giárdia, após a ingestão, os cistos de giárdia
desencistam no trato gastrointestinal com o auxilio do acido estomacal e das
enzimas proteases. Os Trofozoítas (ver figura 2) não são ativamente
fagocíticos e obtém seus nutrientes por absorção. Ocasionalmente, invadem
os ductos viliares, induzindo à colecistite, que é a inflamação da vesícula biliar,
e não penetram intensamente nos tecidos parentais.
Em vários incidentes registrados de surtos de giardíase os sintomas das
vitimas foram; Cólica abdominal, distinção abdominal, febre, fadiga, náusea, e
perda de peso. A giardíase é uma doença altamente contagiosa. A dose
infectivas mínima é de 10 cistos ou menos. É diagnosticada pela
demonstração microscópica de Trofozoítas em amostras fecais, por meio de
esfregaços corados. O teste de ensaio imunoenzimático (ELISA) é efetivo,
quando uma vez anticorpos circulantes como linfócitos são ativados durante a
infecção.
Figura 2. Giardia intestinalis em estagio de Trofozoíta
(http://www.pathobio.sdu.edu.cn/sdjsc/webteaching/Course/webteach/Protozo
an/Giardia-20lamblia/GiardiaTroph(1).jpg)
O ciclo biológico das giádias é muito simples, porém os processos de divisão
celular são complexos, que se desenvolvem para a multiplicação de seus

4
Trofozoítas. Este processo é conhecido como divisão binaria, neste processo
cada núcleo se divide dorsoventralmente, depois daquilo os produtos da
divisão se separam para um ou outro lado do flagelado, que inicia a separação
do plasma. Durante este processo ocorre também a duplicação das organelas
da célula do protozoário, no entanto o disco ventral e o corpo central
desaparecem. As ultimas mencionadas são formadas mais tarde. O ciclo
biológico que involucra ao homem como hospedeiro definitivo se mostra na
figura 3. Na qual se descreve graficamente como é o processo de infecção do
homem, que via oral- fecal, seja, indiretamente pela ingestão de agua e
alimentos contaminados ou diretamente de pessoa a pessoa por meio de
mãos contaminadas com cistos de Giárdia. E o processo de incubação e de 2
a 3 semanas.
Figura 3. Ciclo biológico da Giárdia intestinalis que involucra ao homem como
hospedeiro. (http://www.scoop.it/t/giardia-lamblia)

5
Os trofozoítos colonizam o intestino, onde permanecem aderidos à mucosa
intestinal por meio do disco ventral. Muitos desses trofozoítos passam por um
processo de encistamento, ao final do qual são produzidos os cistos. Esse
processo pode se iniciar no baixo íleo, mas o ceco é considerado o principal
sítio de encistamento. Durante o encistamento, ao redor do trofozoíto é
secretada pelo parasito uma membrana cística resistente composta
parcialmente por quitina. Dentro do cisto ocorre nucleotomia, podendo ele
apresentar-se então com quatro núcleos. Os cistos produzidos são excretados
juntamente com as fezes do hospedeiro podendo permanecer viáveis por
vários meses no meio ambiente, desde que em condições favoráveis de
temperatura e umidade. (Amato-Neto, 2008)
Por outra parte não foi demostrado a produção de nenhuma enterotoxina por
G. lambia, a diarréia é causada por outros fatores. A droga utilizada para o
tratamento da giardíase é a quinacrina, derivado da acridina. Também são
utilizados metronidazol e tinidazol.
A infecção por Giardia é cosmopolita, ocorrendo em áreas desenvolvidas e em
desenvolvimento. Os índices de prevalência variam de 2 % nos países
desenvolvidos até 30% nos países em desenvolvimento. Segundo a
Organização Mundial de Saúde (OMS), estima-se que haja 200 milhões de
pessoas com giardíase sintomática no mundo e 500 mil novos casos
registrados anualmente em populações residentes na Ásia, África e América
Latina.
A continuação se mostram alguns casos históricos de surtos ocasionados por
G. intestinalis, (James 2005):
Em 1960, membros de uma família ingeriram pudim que provavelmente foi
contaminado por fezes de roedores.

6
1968 a 1969 se registraram 19 casos em um surto de giardíase em EUA,
não foram fornecidos maiores detalhes.
1976 aprox. 1400 americanos da ilha de madeira contraíram giardíase,
após consumir agua da torneira, sorvete e vegetais crus.
Em 1979, 29 funcionários de uma escola rural em Minnesota contraíram a
doença por consumir salmão caseiro.
Em 1985, 13 pessoas desenvolveram a doença, depois de estarem
presentes em um piquenique em Connecticut, após de ingerir salada de
macarrão.
Em 1988, 21 membros de uma igreja em México foram vitimas de
giardíase, após o consumo de tacos.
2.2. O Gênero Entamoeba
A Entamoeba histolytica, pertencesse a este gênero, esta parasita produze a
disenteria amebítica o amebíase. Esta parasita é rara em meio anaeróbico e
os trofozoítas carecem de mitocôndria, é aerotolerante e necessita de glicose
e galactose como principal substrato respiratório. As dimensões dos
trofozoitos são de 10-60 μm, enquanto os cistos têm 10-20 μm. Os trofozoítas
são moveis e os cistos não, muitas vezes são encontrados associados a E.
coli no intestino e fezes. (Koneman, 2006)
Em fezes de casos de desinteira a E. histolytica contem células vermelhas do
sangue que ingeriram por pseudopodia, mais a E. coli sempre é encontrada
em maior numero contudo, este organismo não ingere células vermelhas
sanguíneas. Os trofozoitos não conseguem sobreviver no meio ambiente, pero
na forma de cistos ela consegue sobreviver por três meses. Uma pessoa
infectada pode transmitir 4,5 x 107 cistos por dia. (James, 2005)
O habitat da E. histolytica esta no intestino grosso e no cólon, na primeira
ocorre a reprodução das células pela fissão binaria, já no íleo ocorre a

7
formação de cistos os quais podem permanecer livre no lúmen. A transmissão
de cistos por os alimentos é possível por hábitos de higiene inadequados.
Uma estimativa indica que o 10% da população do mundo esteja infectada por
E. histolytica que produzem casos de colite ameboide.
Figura 4. Ciclo biológico de E. histolytica (Ruiz, 2008)
O Período de incubação é 2 a 4 semanas, os sintomas permanecem por
alguns meses, e começam com defecações liquidas e sem febre, a presença
de muco e sangue são características nas fezes. Depois aparece a dor
abdominal, febre diarreia grave, vômito e dor um tanto semelhante a
shigelose. Elevadas concentrações de células de amebas e muco podem
desenvolver-se no cólon, induzindo a obstrução intestinal. As amebas podem
permanecer até por muitos anos.

8
O diagnostico é pela demonstração de trofozoitos e cistos nas fezes ou
fragmentos de mucosa. Alguns métodos imunológicos foram desenvolvidos
como; hemaglutinação indireta, imunoflorescência indireta, aglutinação em
látex e ELISA. Os medicamente usados para o tratamento são; metronidazol e
cloroquina.
2.3. Gênero Toxoplasma
A Toxoplasmose é doença produzida por Toxoplasma gondii, os oocistos
medem 10-12 μm de diâmetro (Fig. 5A e Fig. 6) e possuem uma parede
grossa. Os esporozoítas têm forma crescente e medem 3-7 μm (Fig. 5B e C)(
Juneau 2009). É um parasita intracelular obrigatório. Foi isolado pela primeira
vez em 1908 de um roedor africano “gondi”. Na maioria dos casos de ingestão
de oocistos em humanos não causa sintomas, porque ela fica em estado
latente (encistado). (James 2005; Weiss and Kim 2014)
Figura 5. (A) Oocistos e a (B e C) Formação de esporozoítas (Dubey et al,
1998)
Os gatos são os únicos hospedeiros definitivos deste organismo, nele se
desenvolve a fase intestinal e sexual, os gatos podem transmitir os oocistos a
traves das fezes para outros animais vertebrados incluídos ao homem. O
oocisto liberado pode sobreviver mais do que um ano em ambiente aquecido e
úmido.

9
Figura 6. Estrutura do Toxoplasma gondii
(http://fullmal.hgc.jp/tg/docs/toxoplasma.html)
A maioria dos indivíduos infectados com T. gondii, são assintomáticos, isto
porque após os esporófitos passar a parede intestinal, ele vai ficar em forma
de cisto (latente) devido ao sistema imunológico do individuo hospedeiro.
Figura 7. Ciclo biológico do Toxoplasma gondii
(http://www.caribvet.net/es/diseases/toxoplasmosis)
Quando o cisto e fragmentado por razoes de imunossupressão os braquiozitas
são liberas e passam à forma ativa produzindo sintomas como: febre, dor de

10
cabeça, dores musculares inchação dos linfonodos. Os dores musculares
podem durar, mas de um mês (Weiss and Kim 2014). A terapia
antimicrobiana consiste na administração de sulfonamidas, pirimetamina +
clindamicina ou fluconazol. James 2005 indica que a prevenção pode ser
feita, evitando-se contaminação do meio com fezes de gato e consumo de
alimentos que contêm cistos viáveis, os quais podem ser destruídos pelos
seguintes métodos:
Aquecimento acima de 60ºC,
Irradiação a um nível mínimo de 30 krad (0,3 kGy) e
Congelamento mais não e recomendado
Alguns casos históricos representativos de surtos se apresentam a
continuação:
Em 1985, foi estimado 2,3 milhões de casos nos EUA, o numero excede o
registro de casos de outras doenças. Desde 1954 se suspeita de carnes
malcozidas como meio de transmissão. Na França, no início da década 1960
31% das 641 crianças internadas no hospital tornaram-se soropositivas após o
ingresso. O numero aumento quando foram servidas duas refeições contendo
carne de carneiro malcozida. Em 1968, 35 estudantes de medicina em New
York, foram infectados, após comer hamburguer malpassado e cinco deles
desenvolveram toxoplasmose clínica. Em 1974, uma criança de 7 meses
desenvolveu toxoplasmose clínica, após consumir leite de cabra não
pasteurizada. Em São Paulo 110 estudantes universitários sofreram de
toxoplasmose aguda após consumiram carne malpassada.
2.4. Gênero Sarcosystis
Os investigadores Gutierrez, 2000; Lindsay and Weiss 2004; Riemann and
Cliver 2006, descrevem que este gênero tem duas espécies que ocasionam

11
infecções transmitidas por alimentos e causam doenças extra intestinais em
humanos, são os seguintes: Sarcocystis hominis (portador é o gado) e o
Sarcocystis suihominis (portador é o suíno). E em ambas o hospedeiro
definitivo é o homem. Após a ingestão de Sarcocystis, bradizoítas são
liberadas e penetram na lâmina própria do intestino delgado, onde a
reprodução sexuada ocorre, conduzindo a formação de esporocistos, os quais
são eliminados nas fezes.
E quando os esporocistos são ingeridos por animais (gado e suínos), os
esporozoítas são liberados e espalham-se por todo o corpo do animal,
multiplicando-se assexuadamente, formando Sarcocystis em todos os
músculos esqueléticos e cardíaco. Os bradizoítas de sarcocystis ao olho nu e
alcançam um centímetro de diâmetro. Os sintomas em humanos ocorrem
dentro de 3 a 6 horas e consiste em náuseas, dor de estomago e diarreia.
Figura 8. Ciclo biológico de S. hominis e S. suihominis (http://www.e-
cleansing.com/wp-content/uploads/2009/12/Sarcocystis_LifeCycle_v3.gif)

12
Devido ao fato de bovino e suíno servirem como hospedeiros intermediários
para esses parasitas, seu potencial patogênico em alimentos para humanos é
obvio. Vários estudos demostraram que a aplicação de temperatura de 60 a
71,1 ºC em cozimento de carnes contaminadas com sarcocystis e que foram
subsequentemente administradas a humanos e animais, não produziu a
infecção.
2.5. Gênero Cryptosporidium
Segundo os pesquisadores Miodrag Belosevic and AWWA Research
Foundation, 2000; Bartley and Becker 1999; Fayer and Xiao 2008, a
criptosporidiose é uma infecção produzida por o Cryptosporidium parvum, que
foi descrito pela primeira vez em 1907. O primeiro caso humano só ter sido
registrado em 1976, essa doença existe em todo o mundo, com prevalência de
1 a 4 % em pacientes com diarréia. Na Inglaterra e em Gales no período de
1985 a 1989 a C. parvum foi à quarta doença mais frequente. Em humanos a
doença é autolimitante em indivíduos imunocompetentes, e grave em
imunocomprometidos (SIDA). E o Protozoário pode estar presente na água. E
a rota de transmissão fecal-oral é a mais importante, mais se sabe que pode
ocorrer a transmissão indireta por alimentos como a leite. O C. parvum é uma
parasita coccídio intracelular obrigatório, que tem seu ciclo de vida em um
hospedeiro.
Após a ingestão do oocisto, ocorre a liberação de esporozoítas, os quais
penetram nas microvilosidades dos entorócitos do hospedeiro, onde se
produze a reprodução sexual para o desenvolvimento dos zigotos. Os zigotos
formam oocistos de parede espessa, os quais esporulam dentro das células
hospedeiras, que depois serão liberadas nas fezes. Os oocistos são esféricos
e têm em media 4,5 a 5,0 de tamanho. Cada oocisto contem quatro
esporozoítas, e são muito resistentes ao meio natural.

13
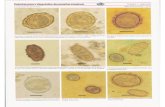
Figura 9. Comparação de Oocistos de C. parvum e G. lamblia
(www.facmed.unam.mx/deptos/microbiologia/parasitologia/criptosporidiasis.html)
Pesquisas demostraram que temperaturas em torno a 60 ºC e -20 ºC podem
matar o oocisto. A Criptosporidiose humana pode ser adquirida, por uma das
cinco rotas; zoonótica, pessoa a pessoa, agua, nosocomial ou alimento.
Figura 10. Ciclo biológico do Cryptosporidium parvum
(http://bagginis.blogspot.com.br/2014_11_01_archive.html)

14
James 2005 indica que o curso clinica da criptosporidiose em humanos
depende do estado imune, por tanto os casos mais graves ocorrem em
imunocomprometidos. Em indivíduos imunocompetentes os organismos
parasitam o epitélio intestinal e causa diarréia. A doença é autolimitante e tem
um período de incubação de 6 a 14 dias, os sintomas aparecem em torno de 9
a 23 dias. Além da diarréia, outros sintomas podem ocorrer, como dor
abdominal, náusia, vômito e febre. Os sintomas podem permanecer por mais
de 30 dias.
E que o diagnostico da doença pode ser feita pela identificação de oocistos
nas fezes das vitimas. Métodos de coloração são utilizados; coloração ácido-
rápida modificada, coloração negativa, flutuação com açúcar e teste de
imunofluorescência direta. No tratamento com os antibióticos
aminoglicosídeos paromomicina e geneticina demostraram inibir o crescimento
intracelular.
Diversos surtos foram registrados desde 1984 e se relatam a continuação
fazendo ênfases no meio de transporte dessa doença:
O primeiro surto ocorreu no Texas, em 1984, após o consumo de água
de poço artesiano.
Três surtos independentes ocorreram no Reino Unido, em 1988-1989, os
casos foram relacionados ao consumo de água tratada e agua da piscina
contaminada.
No Maine, em 1993, uma sidra de maça causou o surto com 150 vítimas.
No Minnesota, em 1995, uma salada de frango causou o surto com 20
vítimas.
No New York, em 1996, uma sidra não pasteurizada causou o surto com
20 vítimas.
No Washintong, em 1997, cebolas verdes cruas causaram o surto com
54 vítimas.

15
2.6. Gênero Cyclospora
Segundo Chacín-Bonilla e Barrios 2011, A Ciclosporose é uma
doença transmitida por alimentos e é ocasionada por Cyclospora
cayetanensis, os oocistos de desta parasita medem aproximadamente 8-10
μm de diâmetros e contêm dois esporocistos (de dimensões 4 e 6 μm) e cada
esporocisto contêm dois esporozoítas. Os oocistos são ácido-resistentes,
sensíveis quanto á secagem, mas resistentes ao cloro.
Figura 11. Esquema do ciclo biológico do Cyclospora cayetanensis
(http://aprendeenlinea.udea.edu.co/lms/moodle/mod/resource/view.php?inpop
up=true&id=101084)
A transmissão de pessoa a pessoa é incomum, os oocistos quando são
excretados devem esporular para tornar-se infectivas. Os oocistos nas fezes
podem ser identificados por esfregaço simples, microscopia epifluorescente. O
C. Cayetanensis é um patógeno intestinal que parasita células epiteliais do
jejuno. E os sintomas que ocasionam são semelhantes à cryptosporidiose, a
diarreia é prolongada, mas autolimitante, com media de 24 a 43 dias. O
período de incubação varia entre 2 e 11 dias.

16
Por outra parte James 2005, relata que o primeiro surto de ciclosporose
ocorreu no E.U.A em 1990, em um hospital, onde foram registrados 21 casos,
a fonte foi água de torneira. Mais o maior surto bem-definido aconteceu em
1996, em 20 estados dos EUA, com 1465 casos, o veículo alimentar foi
framboesa importada.

17
III. PLATELMINTOS
3.1. Gênero Fasciola
Gallego 2006; Romero 2007; James 2005 descrevem as características mais
ressaltantes da parasita assim como os meios pelo qual atravessa até tornar-
se numa doença em humanos, que se detalham a continuação:
A Fasciola hepatica, é encontrado onde são criadas ovelhas e gados. Estes,
Juntamente com humanos, são os principais hospedeiros definitivos. Esse
parasita amadurece nos ductos biliares, e seus grandes ovos operculados
(150 x 90 μm) entram no trato alimentar pelos dutos biliares, para logo ser
liberadas nas fezes. Após 4 a 15 dias na agua o miracídio se desenvolve e
penetra no caramujo, transformando-se em esporocisto. Este produz a rédia-
mãe, que mais tarde torna-se rédia-filha e cercaria. Quando as cercarias saem
do caramujo elas nadam livremente até fixarem-se na vegetação rastreira e no
agrião, encistando-se para formar a metacercaria.
Quando é ingerida a metacercaria, ela descencista no duodeno, passa a
traves da parede do intestino e entra na cavidade cêlomica. Logo entram no
fígado, onde se alimentam sobre as células e se estabelecem nos ductos
biliares, onde amadurecem.
Figura 12. Fasciola hepática em estagio adulta.
(http://www.biologia.seed.pr.gov.br/modules/galeria/uploads/3/10fhepatica.jpg)

18
Esta parasita é contraída pela ingestão de fígados de bovino crus o mal
cozidos. Os sintomas consistem em febre, mal-estar geral, fadiga, perda de
apetite, peso e dor na região do fígado. Esta doença é acompanhada
tipicamente por eosinofilia. Os sintomas em humanos desenvolvem-se 30 dias
após a infecção. A fasciolíase pode ser diagnosticada pela demonstração de
ovos nas fezes, em fluidos biliares ou duodenal. O tratamento é pela
administração de praziquantel.
Figura 13. Ciclo biológico da fascíola hepática
(http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/images/fasciol
a_ciclo-b.jpg)
3.2. GÊNERO FASCIOLOPSIS
Gallego 2007; Koneman et al 2006; Liu 2013 descrevem as características
da parasita e o ciclo biológico onde o homem forma parte, que continuação se
detalham:

19
A Fasciolopsis buski, Produz a doença chamada de fasciolopsíase, o hábitat
desse organismo é similar ao da F. hepatica. Onde humanos são hospedeiros
definitivos e diversos caramujos são os primeiros hospedeiros intermediários e
os segundos são as plantas como o agrião. A diferença da F. hepatica é que
ela surge no duodeno e jejuno de humanos e suínos.
Os sintomas humanos de fasciolopsíase são relacionados ao número de
parasitas, e não há sintomas quando poucos parasitas estão no corpo.
Quando os sintomas ocorrem, eles se desenvolvem dentro de 1 a 2 meses
após a infecção e consistem em diarreia grave, dor abdominal, perda de peso
e fraqueza generalizada, e alguns casos extremos levam até a morte do
individuo hospedeiro. Provavelmente os metabolitos gerados durante a
infecção são provavelmente os causadores dos sintomas.
Figura 14. Vista da parte ventral da Fasciolopsis buski
(http://www.microbiologybook.org/parasitology/fasbus-1pd.jpg)
O diagnostico é realizado pela demonstração dos ovos nas fezes, as quais
têm dimensões de 130 a 140 μm por 80 a 85 μm. E o tratamento efetivo é pela
administração de niclosamida ou praziquantel.

20
Figura 15. Ciclo biológico do Fasciolopsis buski
(http://www.parasitesinhumans.org/pictures/fasciolopsis-buski-life-cycle.gif)
Alguns vegetais que não são cozidas e que consumem em fresco podem ser
veículos para a transmissão desta doença a humanos. Na figura 15 se
descreve graficamente os estágios pelo qual atravessa a F. buski até chegar
ao homem na qual começa no estagio de ovos não embrinados na agua.
3.3. GÊNERO PARAGONIMUS (Koneman 2006 e Liu 2013)
Duas espécies deste gênero são responsáveis pela doença Paragonimíase,
principalmente por Paragonimus westermani, que é encontrado na Ásia,
África, América do Sul e central. Assim como também por P. Kellicotti que é
encontrado na América de Norte e Central. Ao contrario dos trematódeos P.
westermani é um parasita do pulmão.

21
Figura 16. Ciclo biológico de Paragonimus ssp.
(http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/images/parag
onimus_ciclo-b.jpg)
O ciclo biológico começa com a liberação dos ovos são no escarro de
hospedeiros definitivos, após 3 semanas o miracídio é liberado em meio
úmido, para logo penetrar num caramujo que é o primeiro hospedeiro
intermédio, onde vai dar origem a rédia-filha e cercária aproximadamente ao
78 dias da infecção. A cercária passa ao segundo hospedeiro intermediário
que são os caranguejos ou camarão de agua doce, nos quais encistam-se.
Figura 17. Ovo de Paragonimus westermani
(http://www.microbiologybook.org/parasitology/papa1-pd.jpg)

22
Quando o hospedeiro definitivo ingere o crustáceo infetado, as metacercarias
saem dos seus envoltórios e vão para as paredes do duodeno e finalmente até
o pulmão em forma de cistos nos tecidos conectivos. E os ovos são expulsos
novamente no escarro de 2 a 3 meses depois para começar novamente com o
ciclo. Após o período de incubação se produz os sintomas que consistem em
tosse crônica grave e dor toráxica, e o escarro e de cor marrom-avermelhado
com presença de sangue.
Figura 18. Adulto de Paragonimus westerman
(http://www.microbiologybook.org/parasitology/papa2-pd.jpg)
O diagnostico é realizado pela demonstração dos ovos de P. westermani, os
quais possuem dimensões de 80-120 de comprimento e 50-60 de diâmetro.
Também se podem utilizar teste de fixação de complemento, testes de ELISA.
Por outra parte o tratamento se realiza com praziquantel.
i
3.4. Gênero Clonorchis (James 2005 e Koneman 2006)
A Clonorquíase é uma doença ocasionada por Clonorchis sinensis, que é uma
cirrose biliar que tem ocorrências frequentes na china oriental. Esta parasita
tem tipicamente três hospedeiros: dois intermediários onde a parasita se
desenvolve até o estágio juvenil o de larva, e outro hospedeiros definitivo onde
se desenvolve até o estagio adulto e começa a sua reprodução.
O ciclo biológico desta espécie começa quando os ovos são depositados em
agua, liberam larvas cilíadas (miracídios) que invadem aos caramujos, já

23
dentro deles se enrolam formando esporocistos e se reproduzem
assexuadamente para formar embriões.
Figura 19. Ciclo biológico Clonorchis sinensis
(http://www.infectionlandscapes.org/2012/06/liver-flukes-part-1-clonorchis-
sinensis.html)
Os embriões desenvolvem uma rédia que escapa do esporocisto e começa
alimentar-se dos tecidos do hospedeiro. Dentro das rédias se desenvolvem
embriões e formam cercárias que é liberada a traves de um poro.
A cercária é uma parasita em miniatura com uma cauda, que abandona o
caramujo e nada até sue próximo hospedeiro, um peixe, molusco ou
assemelhados. A cercária cresce dentro do novo hospedeiro liberando a
cauda, tornando-se um cisto posteriormente. No interior no cisto desenvolve-
se a metacercária que completa seu desenvolvimento dentro no hospedeiro
final.

24
Figura 20. Vista de Clonorchis sinensis em estagio adulto (Sociedade de
parasitologia de Korean, 2003)
Após ingestão da metacercária presente no peixe, as paredes do cisto
dissolvem-se no intestino liberando vermes jovens, migrando ao fígado do
hospedeiro instalando-se nos ductos biliares.
Estas parasitas são comuns na China, na Coreia, no Japão e em partes do
Sudoeste da Ásia. Geralmente a doença produzida por esta parasita é
associada à ingestão de um prato feito com peixe cru na China.
3.5. Género Diphyllobothrium (Erichsen 2006)
A Difilobotríase é uma infecção contraída pela ingestão de peixe cru o
malcozido, e é causado por Diphyllobothrium latum, que as vesses se
conhece como tênia de peixe. Os hospedeiros definitivos são humanos e
outros mamíferos. E os hospedeiros intermediários são peixes de agua doce e
salmão, nos quais as larvas Plerocercóide (ou metacestoda) são formadas.
Quando o homem consume o peixe que contém a larva Plerocercóide, esta se
liga à mucosa ilíca por duas estruturas adesivas (bótria), onde cada escólex
desenvolve-se em 3 a 4 semanas até formas adultas. O verme em estagio
maduro (Fig. 21), o seu estróbilo desenvolve-se as proglótides aumentando de
comprimento de 10 a 20 m, e cada verme pode produzir 3 a 4 mil proglótides.

25
Figura 21. Pela esquerda imagem Diphyllobothrium latum em estagio adulto e
pela direita os proglótides.
(http://41.media.tumblr.com/1d698b547d785331394183c3d0cb738b/tumblr_mm02glRcyQ1rsd
qvqo1_1280.jpg)
Esta parasita pode liberar mais de um milhão de ovos nas fezes das vitimas,
as quais são mais frequentemente encontradas nas fezes do que as
proglótides.
Figura 22. Ovos de Diphyllobothrium latum
(http://www.scielo.br/img/revistas/rsbmt/v39n1/a17fig02.jpg)
Quando os ovos são depositados na agua, estas liberam larvas natatórias,
que logo invadem pequenos crustáceos em os quais sofrem metamorfose até
o estagio juvenil (metacestoda) ou larva procercóide. Quando o crustáceo é
ingerido por algum peixe a larva migra aos músculos do novo hospedeiro onde
se desenvolve a larva plerocercóide.

26
Figura 23. Ciclo biológico de Diphyllobothrium latum
(http://www.cdc.gov/parasites/images/diphyllobothrium/d_latum_lifecycle.gif)
Por outra o primeiro caso foi registrado em 1906 que foi relacionado a
consumo de sushi, que um prato popular em oriente. Os sintomas são dor
epigástrica, cólica abdominal, vômito, perda de apetite, vertigem, obstrução
intestinal e perda de peso. Mas muitos casos são assintomáticos. E o
diagnostico é pela demonstração de ovos nas fezes. E o tratamento é o
mesmo para teníases.
O risco de contrair essa infecção é alto quando se consumir peixe cruz o
malpassadas, mais prevenção pode ser feita, cozinhando o peixe à
temperatura igual o acima de 60ºC, ou congelar o peixe a -20 ºC pelo mínimo
60 horas.

27
3.6. Gênero Taenia (Romero 2007)
A síndrome teníases é causada em humanos por duas espécies deste gênero;
Taenia saginata e Taenia solíum, sendo os humanos hospedeiros definitivos,
nos quais se desenvolve os estágios; adulto e de maturação sexual, e o
estágio larval ou juvenil são desenvolvidas em hospedeiros intermediários que
pelo geral animais herbívoros.
Esses helmintos não têm sistemas vascular, respiratório ou digestivo. E
depende completamente do hospedeiro para sua nutrição. Seu metabolismo é
principalmente anaeróbico. O verme adulto tem escólex de aproximadamente
um mm de tamanho. Abaixo da cabeça tem segmentos formando o estróbilo,
composto por proglótides, cada um desses tem órgãos de reprodução
completos.
Figura 24: (A) Estróbilo e cabeça de T. saginata e (B) Estróbilo e cabeça de T.
solíum (http://cdn.plp.cl/chacalon/2013/12/618543/original/taenia-saginata-vs-
solium.jpg?1387539186)
Um verme adulto tem dois mil proglótides, e libera diariamente de 8 a 9
proglótides, e cada um contem 80 mil ovos, de 30 a 40 μm de diâmetro cada
um. O tamanho dessa parasita vá de 4 a 6 metros, com período de vida de até

28
25 anos. Quando os proglótides são liberados no solo, estas liberam os ovos
contendo embriões desenvolvidos que podem sobrevir meses.
Quando os ovos são ingeridos pelos herbívoros, os embriões são liberados e
penetram nas paredes do intestino para ser carregados nos músculos
estriados na língua, no coração, do diafragma, da mandíbula e dos membros
traseiros, onde são formadas as larvas chamadas de cisticercos. A
cisticercose é o termo utilizado para indicar a existência destas parasitas em
hospedeiros intermediários, o cisticerco aparece geralmente entre 2 a 3 meses
após a ingestão dos ovos.
Figura 25. Ciclo biológico de T. saginata e T. solíum
(http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/images/taenia
_ciclo-b.jpg)
A infecção causada pelo verme T. solium, tem algumas diferenças ao T.
saginatus, como; humanos e suínos podem ser hospedeiros finais e
intermediários, o escólex tem ganchos em discos de sucção e o estróbilo pode

29
medir de 2 a 4 m, contendo em torno de mil proglótides. Os embriões de T.
solium são levados para os tecidos do corpo incluindo olhos e cérebro. Por
outra parte os sintomas no caso da cisticercose em humanos conduzem a
eosinofilia. A teníase em humanos é diagnosticada por demonstração de ovos
ou proglótides nas fezes. Fixação do complemento, hemaglutinação indireta e
teste de imunofluorescência, são métodos auxiliares no diagnostico.
Para o tratamento contra os vermes adultos é utilizada a niclosamina ou
praziquantel. No caso da cisticercose são utilizados procedimentos quirurjicos.
Mais a prevenção desta doença pode ser efetuada por meio da aplicação de
temperaturas acima de 60 ºC, esta operação no processo de elaboração de
alimentos pode destruir o cisticerco presentes em carnes de suínos e gados.
Por outro lado o congelamento destas mesmas carnes a -10 ºC por um
período de 10 a 15 dias ou imersão em solução de sal inativará esses
parasitas

30
IV. NEMATELMINTOS
Os nematelmintos causadores de doenças veiculadas por alimentos
pertencem a duas ordens do filo Nematódeo:
4.1. Gênero Trichinella (Gutierrez 2000 e James 2005)
A Trichinella spiralis produz a triquinose (triquinelose). Descoberto em 1835 (J.
Paget) e o primeiro caso foi relatado na Alemanha 1859. O T. spiralis não tem
estagio de vida livre. Ele é contraído pela ingestão de produtos malcozidos
geralmente de suínos. As fêmeas deste parasita tem um comprimento de 3 a 4
mm e os machos em torno da metade. Ovos são incubados pelas fêmeas e
tem um comprimento de 0.1 mm, cada fêmea pode produzir até 1500 ovos.
As larvas liberadas penetram a parede do intestino e invadem os músculos
esqueléticos e também incluem os dos olhos, da língua, e do diafragma. E
crescem em torno de 1 mm no musculo e posteriormente se encistam,
encurvando-se, possibilitando a calcificação das paredes do cisto após 6 a 18
meses.
Figura 26. Cisto de T. spiralis calcificadas em tecidos musculares
(http://www.telmeds.org/wp-content/uploads/2009/10/Tspiralis_larva21.jpg)

31
Quando a carne contendo os cistos é ingerida pelo homem se produze a sua
liberação pela atividade enzimática do estomago, e a maturação desta
parasita ocorre no lúmem do intestino. Quando há ingestão de alimentos
fortemente contaminados por cistos, a Trichinella penetra na mucosa intestinal
produzindo náusea, dor abdominal, diarreia e algumas vezes vômito, se
produz em um a dois dias. Quando a ingestão de poucas larvas, o período de
incubação pode durar até 30 dias, se 10 ou menos larvas são depositadas por
grama de tecido muscular, pelo geral no existe sintomas, e quando há 100 ou
mais larvas por grama aparecem os sintomas descritos anteriormente. Caso
houvesse acima de 1000 larvas por grama podem ocorrer consequências
graves.
Figura 27. Ciclo biológico de T. spiralis
(http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/images/tspirali
s_ciclo-b.jpg)
O diagnostico pode ser feita por biópsias nos músculos suspeitosos de
infecção. Os métodos imunológicos utilizados são; floculação com bentonite,
floculação colesterol-lecitine e aglutinação em látex, esses métodos
mencionados podem dar positivos após 3 semanas da infecção.

32
E a prevenção, usando temperaturas acima de 60ºC para o cozimento de
carnes é efetiva na destruição das larvas caso estivessem presentes. Por
outra parte também as baixas temperaturas de congelação podem fazer
perder sua efetividade, que vai depender do tempo de congelação e
temperatura. Childers et al, (1982), Avaliaram o efeito da aplicação de NaCL,
aw, e o método de fermentação na viabilidade de T. spiralis, em salame
Genova, o resultado foi que as larvas foram destruídas após 30 dias.
4.2. Gênero Anisakis e Pseudoterranova (Koneman 2006 e James 2005)
Produzem a infecção chamada de Anisaquiase e os responsáveis são duas
espécies destes dois gêneros; Anasakis simplex e Pseudoterranova
decipiens. Eles têm diversos hospedeiros intermediários, e os humanos não
são seus hospedeiros finais e a doença ocorre acidentalmente, devido a
intercursos nos ciclos de vida desses vermes.
Figura 28. Ciclo biológico da A. simplex e P. decipiens
(http://www.elrinconin.es/aula/lego1/p_anisakis/ciclo.jpg)

33
Os hospedeiros definitivos são mamíferos marinos como Baleia para o A.
simplex e focas para o P. decipiens, estes mamíferos podem liberar milhares
de ovos nas fezes nas aguas de seu habitat, já na agua os ovos liberam larvas
que logo serão ingeridas por pequenos crustáceos, sendo estes seus
primeiros hospedeiros, após os crustáceos parasitados são ingeridas por
outros crustáceos maiores se desenvolve o estagio larval que é o estagio
infeccioso para peixes, humanos e baleias que são seus hospedeiros naturais.
Figura 29. Carne de peixe infectado com A. simplex e P. decipiens
(http://www.labocal.com/modulos/usuariosFtp/conexion/imagenes586a.jpg)
Os sintomas se desenvolvem após 4 a 6 horas do consumo do peixe infectado
e consistem em dores epigástricas e vômitos. Os casos mais graves podem
ocorrer defecações com sangue e febre. Caso eles penetrar a mucosa do
intestino, pode formar um granulo eosinofílico ou causar peritonite.
Figura 30. Parasita penetrando a mucosa do intestino
(http://gsdl.bvs.sld.cu/greenstone/collect/preclini/index/assoc/HASH421a.dir/fig
01a110.png)

34
O diagnostico, pode ser efetuada por endoscopia, após a detecção pode ser
feita a intervenção cirúrgica para retirar os parasitas presentes. Outras formas
de identificação destas parasitas incluem a fixação do complemento e
imunoflorescência indireta. E o tratamento se efetua por administração de
tiabendazol que é efetivo na eliminação da parasita.
A prevenção de Anisaquiase pode ser feita evitando o consumo de peixe cru o
malcozido. E as formas infectivas podem ser destruídas pela aplicação de
temperaturas acima de 60 ºC nas carnes de peixes que são potencialmente
veículos de transmissão desta doença. Além disso, o congelamento das
carnes a temperaturas de -20ºC ou mais baixas por um período no menos de
60 horas inativara a larva. Por outra parte a imersão em salmoura das carnes
de peixes potencialmente contaminadas por quatro semanas podem inativar
também as larvas.

35
V. PESQUISAS ATUAIS
5.1. A Perspective on Cryptosporidium and Giardia, with an Emphasis on
Bovines and Recent Epidemiological Findings
Journal Advances in Parasitology
Harshanie Abeywardena H. et al., 2015
Objetivo Fornecer uma revisão de alguns aspectos-chave da epidemiologia
molecular da criptosporidiose e giardíase em animais, com ênfase em bovinos,
resumir as pesquisas de Cryptosporidium e Giardia de bovinos e búfalos de
água em partes da Austrália e Sri Lanka, considerando aspectos de saúde
pública, e Fornecer uma perspectiva sobre as futuras avenidas de estudo.
Concluiu-se que os estudos recentes reforçam o fato que bovinos
abrigar Cryptosporidium e Giardia que provavelmente representam um risco
para a saúde humana e para destacar a necessidade de futuras investigações
da biologia, genética de populações e dinâmica de transmissão
de Cryptosporidium e Giardia em bovinos, búfalos e outros ruminantes em
regiões geográficas diferentes, o destino e transporte de estágios infectantes
após a sua liberação no meio ambiente, bem como para as melhores
estratégias para o controle e prevenção da criptosporidiose e giardíase,
guiado por estudos de epidemiologia molecular.
5.2. Chapter Two – Tradition and Transition : Parasitic Zoonoses of People
and Animals in Alaska, Northern Canada, and Greenland
Journal Advances in Parasitology
Jenkins E. et al, 2013
Objetivo: Avaliação abrangente da diversidade, distribuição, ecologia,
epidemiologia e significado de nove parasitos zoonóticos nas populações
animais e humanos no Norte de Norte América e da Groenlândia (Norte).

36
Conclui-se que com base em uma avaliação de risco qualitativa com critérios
fortemente ponderada para a saúde humana, estes parasitas zoonóticos são
classificados, em ordem decrescente de importância, como se segue:
Echinococcus multilocularis, Toxoplasma gondii, Trichinella e Giardia,
Echinococcus granulosus/canadenses e Cryptosporidium, Toxocara,
Anisaquídeos nematóides e cestodes diphyllobothrium. Recentes e futuras
tendências na importância destes parasitas para a saúde humana no Norte
são exploradas. Parasitas que submetem ao desenvolvimento dependente da
temperatura no ambiente (como Toxoplasma, Ascaris e Anisaquídeos
nematóides, e Cestodes diphyllobothrium) provavelmente serão submetidos a
acelerado desenvolvimento em áreas endêmicas e espécies irão mover para o
norte, resultando em mudanças de fauna.
5.3. Cryptosporidiosis in Southeast Asia: What's out There?
Journal Advances in Parasitology. Volume 71
Lim Y et al, 2010
O objetivo do presente capítulo é rever os dados e informações disponíveis
sobre criptosporidiose no Sudeste Asiático e para fornecer recomendações na
busca de uma melhor compreensão do Cryptosporidium nesta região, a fim de
facilitar o desenvolvimento de intervenções multidisciplinares eficazes para
controlar criptosporidiose
Conclusão:
A criptosporidiose é uma doença socioeconomicamente importante, entérica
causada por um grupo de parasitas protozoários do
género Cryptosporidium. Embora muito se saiba sobre Cryptosporidium e do
impacto da criptosporidiose e outras doenças diarreicas em países
desenvolvidos, este não é o caso de muitos países da África, América do Sul e
na Ásia em desenvolvimento. No sudeste da Ásia, o que representa um

37
epicentro para doenças infecciosas emergentes, criptosporidiose foi relatada
em países, como o Camboja, Indonésia, Laos, Malásia, Myanmar, Filipinas,
Cingapura, Tailândia e Vietnã. Na maioria desses países, os prováveis fatores
predisponentes para criptosporidiose incluem o rápido crescimento
populacional e urbanização em expansão (que estão frequentemente ligadas a
suprimentos inadequados de água municipal e mal gerido eliminação de
resíduos), bem como o clima tropical e o aumento da prevalência de HIV /
AIDS e outras doenças infecciosas.

38
VI. BIBLIOGRAFIA
Amato-Neto, V. et al., 2008, Parasitologia - Uma abordagem clínica.
Primeira edição. Rio de Janeiro: Elsevier, 2008. 400 p.
Gallego J. 2006. Manual de Parasitología: Morfología y biología de los
parásitos de interés sanitario. Primera edición. Barcelona. Pag. 139-140
James M. 2005. Microbiologia de Alimentos. Sexta edição. Brazil. Editora
Armed. Pag. 606-607
Koneman E., 2006. Diagnostico microbiológico. Sexta edición. España.
Editora Panamericana. Pag. 1206-1207.
Dubey, J.P., Lindsay, D.S, Speer, C.A. (1998). Structures of Toxoplasma
gondii tachyzoites, bradyzoites, and sporozoites and biology and development
of tissue cysts. Clin Microbiol Rev. Apr;11(2):267-99.
Chacín-Bonilla e Barrios, 2011, Cyclospora cayetanensis: biología,
distribución ambiental y transferencia, Scielo: Biomédica vol.31 no.1 Bogotá,
Universidad del Zulia.
Erichsen V. et al., 2006, Diphyllobothrium latum: relato de caso no Brasil,
Rev. Soc. Bras. Med. Trop. vol.39 no.1, Universidade Federal do Rio Grande
do Sul, Porto Alegre, RS
Weiss and Kim 2014, Toxoplasma Gondii: The Model Apicomplexan;
Perspectives and Methods, 2nd Edition.

39
Juneau M., 2009, Isolation and Characterization of Toxoplasma Gondii
Bradyzoite Development Mutants, University of Wisconsin-Madison, Print
ProQuest LLC. Pag. 21
Gutierrez Y., 2000, Diagnostic Pathology of Parasitic Infections with Clinical
Correlations. Second Edition, Oxford University. Pag. 186
Lindsay D., and Weiss L., 2004, Opportunistic Infections: Toxoplasma,
Sarcocystis, and Microsporidia. Kluwer Academic Publishers, World Class
Parasites: Volumen 9, Boston. Pag. 114.
Riemann H. and Cliver D., 2006, Foodborne Infections and Intoxications,
Elservir: Food Science and Technology, International Series, Third Edition.
USA. Pag. 457
Miodrag Belosevic and AWWA Research Foundation, 2000,
Cryptosporidium Parvum Viability Assay. USA.
Bartley C. and Becker C., 1999, Inactivation of Cryptosporidium parvum
oocysts in Drinking Water, Calgon Carbon Corporations Sentinel Ultraviolet
Reactor Michigan.
Fayer R. and Xiao L., 2008, Cryptosporidium and Cryptosporidiosis, Print
for Taylor and Francis Group, Second Edition. USA.
Romero R., 2007, Microbiologia y parasitologia humana: Bases etiológicas
de las enfermedades infeccionsas y parasitarias, Editorial Panamericana, 3ra
Edición, Mexico.

40
Koneman E. et al., 2006. Color Atlas and Textbook of Diagnostic
Microbiology. Sixth Edition. Print Lippincott Williams and Wilkins. Pag. 1288.
Philadelphia.
Liu D., 2013, Molecular Detection of Human Parasitic Pathogens, Print
Taylor and Francis Group. Pag 353.
Abeywardena et al., 2015. A Perspective on Cryptosporidium and Giardia,
with an Emphasis on Bovines and Recent Epidemiological Findings. Journal
Advances in Parasitology.
Jenkins E. et al, 2013, Chapter Two – Tradition and Transition : Parasitic
Zoonoses of People and Animals in Alaska, Northern Canada, and Greenland.
Journal Advances in Parasitology.
Lim Y et al, 2010, Cryptosporidiosis in Southeast Asia: What's out There?
Journal Advances in Parasitology. Volume 71
Ruiz M. 2008. Parasitología clínica. Encontrado na web site:
http://commons.wikimedia.org/wiki/File:Entamoeba_histolytica_life_cycle-
en.svg
The Korean Society Parasitology, 2003, Encontrado na web site:
http://atlas.or.kr/atlas/alphabet_view.php?my_codeName=Clonorchis%20sinen
sis , Revisado en 14 de abril 2015