PROTEÍNAS
-
Upload
guilherme-sousa -
Category
Documents
-
view
10 -
download
3
description
Transcript of PROTEÍNAS

DISCIPLINA DE QUÍMICA ORGÂNICACURSO DE AGRONOMIA
PROFESSORA DRA. NILÉIA CRISTINA
Fernanda Lemos Gabriel Portela Guilherme Brandt Guilherme Sousa
PROTEÍNAS

INTRODUÇÃO Móleculas de natureza heteropolimérica;
Células vivas: cerca de 50% do seu peso seco;
Produtos vegetais mais ricos em proteínas: leguminosas; sementes oleaginosas; GRÃOS EM GERAL nozes;

INTRODUÇÃO Componentes da membrana plasmática e
citoesqueleto celular;
Funções fisiológicas;
Regeneração de tecidos, catalisadores de reações químicas, sistema imunológico;
Ácidos nucléicos: crescimento e reprodução;

INTRODUÇÃO Unidade básica: aminoácido ligado entre si
por ligações peptídicas;
Seres humanos: cerca de 20 aminoácidos diferentes para compor suas proteínas.
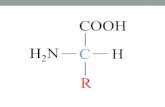
Aminoácido:
Fonte: http://wikiciencias.casadasciencias.org/wiki/index.php/Amino%C3%A1cido

INTRODUÇÃO
Propriedades da proteína:
determinadas pelo número e espécie dos resíduos de aminoácidos;
determinadas pela sequência de aminoácidos na molécula.
Fonte: Google Images

NUTRIÇÃO Moléculas utilizadas no crescimento e manutenção
do corpo;
Componente estrutural de todas as células: músculos;
Quebradas na digestão para a obtenção de aminoácidos;
Fundamentais para a formação de células sanguíneas;
Fonte: http://recuerdosdepandora.com/wp-content/uploads/2011/01/musculo.jpg

NUTRIÇÃO Alimentação animal:
Volumosos: TF > 18% (alto VE);
Concentrados: TF < 18% (baixo VE);
Concentrados energéticos: < 20% PB; Concentrados protéicos: > 20% PB;
Fonte: Google Images

NUTRIÇÃO Alimentos que podem ser utilizados como
concentrados: milho: referencial para os concentrados energéticos soja: referência a concentrados protéicos.
Concentrados protéicos: principal objetivo: fornecer proteína de elevada
digestibilidade; alto valor biológico sendo ricos em aminoácidos
essenciais;

NUTRIÇÃO Percentagem de proteína bruta dos alimentos:
Milho, 9% PB; Soja, 45% PB; Algodão, 30% PB; Amendoim, 50% PB; Girassol, 20% PB; Linhaça, 35% PB; Capim Brachiaria s.p, 12% PB;
Fonte: Google Images

NUTRIÇÃO Consumo diferente da necessidade do corpo: reserva
de curta duração; impossível armazenamento de proteínas em longo prazo;
As proteínas são convertidas em aminoácidos pelo fígado;
Excesso: aumento do teor de cálcio na urina;
Falta: resultam em condições físicas variadas, diarréia, dermatose;

BIOQUÍMICA Macromoléculas originadas por reações
químicas entre aminoácidos;
Hidrólise: aminoácidos de origem;
Reações: amina, ácido carboxílico ou radical R;
Aminoácidos Peptídeos Proteínas;
Fon
te:
htt
p:/
/wik
icie
ncia
s.c
asad
ascie
ncia
s.o
rg/w
iki/
ind
ex.p
hp
/Am
ino
%C
3%
A1
cid
o

BIOQUÍMICA
Importância das proteínas: encontram-se em todos os organismos;
Contém sempre C, H, O, N;
Podem conter S e mais raramente I, Fe, P;
Fonte: Google Images

BIOQUÍMICA Glicina + Alanina (aminoácidos originais): dipeptídeo;
Grupo CARBOX (glicina) + grupo AMÍNICO (alanina) - H2O (produto)
Resultado: AMIDA (Base do peptídeo formado + H2O);
Fon
te:
htt
p:/
/ww
w.i
nfo
escola
.com
/bio
qu
imic
a/q
uim
ica-d
as-p
rote
inas/

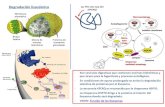
BIOSSÍNTESE PROTÉICA
Síntese de proteínas;
Diretamente relacionado aos ácidos nucléicos:
DNA (Ácido Desoxirribonucléico); RNA (Ácido Ribonucléico);

BIOSSÍNTESE PROTÉICA
Controle do processo: DNA (moléculas mestre da vida);
Instrução para a síntese de uma proteína: RNA;

BIOSSÍNTESE PROTÉICA
Ácidos Nucléicos:
macromoléculas denominados nucleotídeos; açúcar (pentose) – desoxirribose DNA;
ribose RNA;

BIOSSÍNTESE PROTÉICA
Esqueleto da molécula:
bases nitrogenadas açúcares fosfato

BIOSSÍNTESE PROTÉICA Código genético do DNA:
trincas de bases: códons (três letras - aminoácido)
código genético degenerado:
aminoácido pode ser codificado por mais de uma trinca de bases nitrogenadas

BIOSSÍNTESE PROTÉICA Bases nitrogenadas: ligam-se por
complementaridade: DNA: entre as duas fitas do DNA
Adenina (A) + Timina (T) Citosina (C) +Guanina (G)
RNA: fita simples Bases se complementam em associação com a molécula de
DNA: TRANSCRIÇÃO Outras moléculas de RNA: TRADUÇÃO Não possui Timina: Adenina (A) + Uracila (U)

BIOSSÍNTESE PROTÉICA TRANSCRIÇÃO:
molécula de RNA sintetizada: molde de DNA: sintetizados todos os tipos de RNAs da célula:
RNAm RNAR RNAt RNAs menores
RNAm: informação genética às proteínas Demais RNAs: funções estruturais e catalíticas
Todos envolvidos na síntese proteíca

BIOSSÍNTESE PROTÉICA
TRADUÇÃO:
RNAm - sequência de aminoácido; códon: corresponde a um aminoácido;

BIOSSÍNTESE PROTÉICA Citoplasma:
RNAt aminoácidos dissolvidos transporte RNAm;
RNAt reconhece o códon (AUG) codifica metionina;
RNAt: anticódon específico Reconhecimento RNAt-RNAm: ribossomo desloca-se sobre o
RNAm Une os aminoácidos transportados Repetido até que o RNAr encontre o códon de parada cadeia de aminoácidos (molécula de proteína)

ESTRUTURA
Formas tridimensionais variadas;
Obtenção da forma:
fatores externos (influência de chaperonas); através das próprias propriedades químicas de seus
aminoácidos;
Fon
te:
Goog
le I
mag
es

ESTRUTURA Quatro tipos de estruturas:
variação nas composições aminoácidas; cadeia; forma tridimensional;
primária;secundária; terciária;quaternária;
Fonte: Google Images

ESTRUTURA Estrutura primária:
determinada pela sequência de aminoácidos ao longo da cadeia;
Estrutura primária da proteína 1EFN
Fonte: wikimedia.org

ESTRUTURA Estrutura secundária:
organização dos aminoácidos na sequência primária da proteína; devido a rotação das ligações entre os carbonos α e os grupos
amina e o ácido carboxílico;Estrutura secundária da molécula protéica mioglobina
Fonte: wikimedia.org

ESTRUTURA Estrutura terciária:
é definida pela forma como a molécula se organiza no espaço;
Estrutura terciária da molécula protéica 1EFN
Fonte: wikimedia.org

ESTRUTURA Estrutura quaternária:
formada a partir da união de várias moléculas protéicas envolvidas num complexo multi-protéico;
Estrutura quaternária da
molécula protéica 1EFN
Fonte: wikimedia.org

ESTRUTURA Proteína 1B6Q
CNOS
Fonte: Swiss Institute of Bioinformatics

FUNÇÃO CELULAR Enzimas: proteínas catalisadoras
reações químicas complexas em altas velocidades;
Propriedades de atuação das enzimas: Especificidade de substratos: sustâncias que
reagem sob o estímulo enzimático; Dependência do pH: pH específico de ação; Dependência de temperatura: desnaturação;

FUNÇÃO CELULAR Estrutura enzimática e função catalítica;
Ligação do substrato específico à enzima;
Sítio ativo: resíduos de aminoácidos capazes de interagir com
o substrato;
Integridade da molécula enzimática;

FUNÇÃO CELULAR
Proteínas Ligantes;
A estrutura dinâmica das proteínas:
Ligação reversível a outras moléculas: ligantes

FUNÇÃO CELULAR Sinalização celular: percepção e resposta;
Erros: doenças;
Estudo das sinalizações: prevenção de possíveis doenças;
Sinalização entre células de organismos de diferentes;

FUNÇÃO CELULAR Principais intervenientes no interior das
células;
Principal componente celular;
Conjunto de proteínas que podem ser expressas numa determinada célula: proteoma

MÉTODO DE ESTUDO
Proteínas: moléculas biológicas mais intensivamente estudadas;
Estudos divididos em meios:
in vitro in vivo in silico

MÉTODO DE ESTUDO Estudo in vitro: compreensão do desempenho
das suas funções protéicas: o estudo da cinética enzimática;
Estudo in vivo: dados sobre o papel fisiológico da proteína no contexto de uma célula ou de um organismo;
Estudo in silico: métodos computacionais para estudar proteínas;

CONCLUSÃO Proteínas estão presentes em todos os seres vivos; Participam em diversos processos celulares, sendo Partes vitais para o metabolismo; Divergências em seu consumo recomendado
podem acarretar complicações físicas e mentais; Formatos tridimensionais: fatores determinantes de
suas funções no organismo, tópico de pesquisa da biologia estrutural;
Macromoléculas são as reguladoras da atividade celular;

DISCIPLINA DE QUÍMICA ORGÂNICACURSO DE AGRONOMIA
PROFESSORA DRA. NILÉIA CRISTINA
Fernanda Lemos Gabriel Portela Guilherme Brandt Guilherme Sousa
PROTEÍNAS