FARMACOTECNICA - Isotonicidade – Preparacoes Oftalmicas, Nasais E Otologicas
UNIVERSIDADE FEDERAL DE GOIÁS DISCIPLINA: … · semana de vida até o momento em que surgiu a...
Transcript of UNIVERSIDADE FEDERAL DE GOIÁS DISCIPLINA: … · semana de vida até o momento em que surgiu a...
UNIVERSIDADE FEDERAL DE GOIÁS
ESCOLA DE VETERINÁRIA E ZOOTECNIA
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA ANIMAL
DISCIPLINA: SEMINÁRIOS APLICADOS
CIRCOVIROSE SUÍNA E SEU CONTROLE
UMA REVISÃO
Thales Coelho de Alvarenga
Orientador (a): Wilia Marta Elsner Diederichsen de Brito
GOIÂNIA
2011
iii
THALES COELHO DE ALVARENGA
CIRCOVIROSE SUÍNA E SEU CONTROLE
UMA REVISÃO
Seminário apresentado junto à
Disciplina Seminários Aplicados do
Programa de Pós-Graduação em
Ciência Animal da Escola de
Veterinária e Zootecnia da
Universidade Federal de Goiás. Nível:
Doutorado.
Área de Concentração:
Sanidade Animal, Higiene e
Tecnologia de Alimentos (SANHTA)
Linha de Pesquisa:
Etiopatogenia, epidemiologia,
diagnóstico e controle das doenças
infecciosas dos animais
Orientador (a):
Wilia Marta Elsner Diederichsen de Brito – IPTSP/UFG
Comitê de Orientação:
Jurij Sobestiansky – EVZ/UFG
GOIÂNIA 2011
iv
SUMÁRIO
1 INTRODUÇÃO .................................................................................................... 1
2 REVISÃO DE LITERATURA ............................................................................... 3
2.1Histórico ......................................................................................................... 3
2.2 Agente etiológico .......................................................................................... 4
2.3 Epidemiologia e Formas de transmissão ...................................................... 5
2.4 Patogenia ...................................................................................................... 7
2.5 Manifestações clínicas .................................... Erro! Indicador não definido.
2.5.1 SMDS ..................................................................................................... 7
2.5.2 PNDS ..................................................................................................... 9
2.5.3 PNP ........................................................ Erro! Indicador não definido.0
2.5.4 Falhas reprodutivas .............................................................................. 10
2.5.5 Tremores congênitos ............................................................................ 10
2.5.6 Enterite associads ao PCV2 ................................................................. 10
3 IMUNOLOGIA ................................................................................................... 12
4 FATORES QUE MODULAM DOENÇAS CAUSADAS POR PCV2 ................... 13
4.1Fatores virais ............................................................................................... 13
4.2Fatores do hospedeiro ................................................................................. 14
4.3Co-infecções ................................................................................................ 14
4.4Imunomodulação ......................................................................................... 14
5 DIAGNÓSTICO ................................................................................................. 15
5.1Técnicas de diagnóstico laboratorial ............................................................ 16
5.1.1 PCR ........................................................ Erro! Indicador não definido.6
5.1.2 ISH e IHQ ............................................................................................ 1.6
6 CONTROLE ...................................................................................................... 17
6.1Medidas higiênicas ...................................................................................... 17
6.2Medidas sanitárias ....................................................................................... 18
7 CONSIDERAÇÕES FINAIS .............................................................................. 22
REFERÊNCIAS .................................................................................................... 23
v
LISTA DE FIGURAS
Figura 1 - Representação esquemática da partícula do vírus da
circovirose suína
2
Figura 2 - Figura de leitões na fase de creche, com um animal
acometido por SMDS
8
Figura 3 - Figura de um leitão com sinais clínicos de PNDS 9
Figura 4 - Esquema de sinais clínicos e achados histopatológicos
de um animal acometido de enterite por PCV2
1
vi
LISTA DE QUADROS
Quadro 1 - Esquematização dos 20 princípios de Madec 1
Quadro 2 - Vacinas comerciais para PCV2 2
1 INTRODUÇÃO
A suinocultura brasileira, a exemplo das outras cadeias produtivas
do agronegócio, cresceu significativamente nos últimos anos. Atualmente o
Brasil é o 4º maior produtor de suínos no mundo e o 4º maior exportador de
carne suína no mercado internacional. Os dados da suinocultura brasileira
indicam a existência de 1,65 milhões de matrizes suínas, produziu 3,24 milhões
de toneladas de carne em 2010 e apresentou uma receita de US$ 1,34 bilhões
em exportações em 2010. Temos mais de 50 mil produtores, gerando um
milhão de empregos diretos
Segundo a associação brasileira da indústria importadora e
exportadora de carne suína (Abipecs), uma vantagem comparativa significativa
para o Brasil na ampliação da sua participação no mercado internacional está
na disponibilidade de terras agriculturáveis a serem exploradas e na
capacidade de produção de grãos que o país apresenta, aliadas a grande
extensão geográfica do país. Porém o Brasil encontra barreiras sanitárias em
praticamente todos os maiores importadores de carne suína do mundo, com
exceção da Rússia, que ainda não integra a Organização Mundial do Comércio
(OMC) (ABIPECS, 2011).
Dentre as principais doenças que causam impacto negativo na
suinocultura brasileira encontra-se a circovirose suína (CV). Atualmente a
maior parte das granjas brasileiras é positiva para o circovírus suíno tipo 2
(PCV2), que é responsável por importantes impactos na saúde dos animais. A
doença cursa com alto índice de abortos e natimortos nas matrizes e afeta
principalmente animais nas fases de crescimento e engorda. Causa grande
prejuízo na indústria suinícola em decorrência do aumento da mortalidade,
diminuição do desempenho dos animais e elevados índices de refugagem
(LÓPEZ-SORIA et al., 2005).
Estudos ―in vitro‖ demonstraram que o vírus sozinho é incapaz de
causar doença clínica. Mas se associado a outros fatores pode desencadear
enfermidades, sendo considerada então uma doença multifatorial. Nos animais
de crescimento e terminação é chamada de síndrome multissistêmica do
definhamento suíno (SMDS), principal manifestação clínica da CV. As taxas de
morbidade e letalidade em decorrência da manifestação da SMDS variam entre
2
quatro e 30%, dependendo das práticas de manejo, co-infecções, fatores
genéticos do hospedeiro e genótipo viral (GRAU-ROMA et al., 2009).
O PCV2 é considerado ubíquo nos suínos e é excretado por via
nasal, bronquial, fecal e urinária de animais com ou sem a SMDS, sendo as
secreções nasais ou aerossóis apontados como a principal forma de
transmissão horizontal (CAPRIOLI et al., 2006).
Nas propriedades nas quais a SMDS é relatada, geralmente,
observa-se a associação entre o PCV2 e outros vírus (vírus da síndrome
reprodutiva e respiratória suína, parvovírus suíno, influenza suína e
coronavírus) e/ou bactérias como Haemophilus parasuis, Actinobacilus
pleuropneumoniae, Streptococcus suis e Mycoplasma hyopneumoniae) (KIM et
al., 2001).
Um diagnóstico de circovirose suína deve apresentar os sinais
clínicos associados com lesões macro e microscópicas e detecção do material
genético viral. Apesar do sucesso das vacinas no controle de circovirose,
devemos lembrar que esta síndrome tem uma etiologia multifatorial, portanto
uma avaliação dos fatores de risco na exploração é necessária (OPRIESSNIG
et al., 2007).
Diante da importância dessa enfermidade no rebanho mundial e do
fato de não se ter um modelo eficaz de controle das manifestações clínicas da
infecção, este estudo tem como objetivo revisar aspectos da infecção pelo
PCV2 com um enfoque maior na prevenção e controle dos fatores secundários.
3
2 REVISÃO DE LITERATURA
2.1 Histórico
O circovírus suíno foi relatado primeiramente por Tischer et al.
(1974), mediante microscopia eletrônica, ao observarem um vírus
morfologicamente semelhante a um picornavírus, que causava infecção
persistente em cultivo celular de rim suíno (PK-15) sem induzir efeito citopático.
Posteriormente, foi demonstrado que esse vírus possuía um genoma composto
por um filamento único de DNA, circular e fechado, razão pela qual
denominaram-o de circovírus suíno (TISCHER et al., 1982).
Infecções experimentais com PCV em suínos permitiram verificar a
eliminação do agente nas fezes e na secreção nasal dos animais, mas os
animais não apresentaram sinal clínico de doença ou alterações morfológicas
(TISCHER et al., 1986).
Diante desses resultados, estudos com o agente tornaram-se
irrelevantes até que, em 1991, no Canadá, um veterinário observou um grupo
de animais que apresentavam um quadro grave de emagrecimento progressivo
com dificuldades respiratórias, palidez e icterícia, com mortalidade de
aproximadamente 10% (SEGALES, 2007).
Estes animais foram necropsiados e foi coletado material para
exame histopatológico que revelou a presença de lesões no sistema linfóide
(depleção linfocitária e infiltração granulomatosa dos tecidos linfóides) de
origem até então desconhecida (SEGALES, 2007).
Em 1994, um surto de uma doença inflamatória com caquexia
progressiva, elevadas taxas de mortalidade e afetando principalmente leitões
da creche, com evolução subaguda a crônica foi descrito no Canadá em
sistemas de produção de variados status sanitários (SEGALES, 2007).
Em 1998, Hamel et al. descreveram toda a sequência genômica do
agente causal dos surtos e associaram ao vírus descrito anteriormente por
Tischer, 1974 e concluíram que esta variante do vírus apresentava diferenças
em relação ao circovírus não patogênico anteriormente isolado nas células de
rim de suínos PK-15 (68% de homologia).
4
Desta forma o circovírus patogênico, associado aos sinais clínicos
relatados, foi denominado de circovírus suíno tipo 2 (PCV2), enquanto que o
circovírus não patogênico passou a ser conhecido como circovírus suíno tipo 1
(PCV1) (MEEHAN et al., 1998).
A circovirose suína foi diagnosticada pela primeira vez no Brasil em
2000. Desde então vários casos novos de suspeita clínica com confirmação
laboratorial foram identificados e atualmente encontra-se disseminada por todo
o território nacional causando grandes perdas econômicas para a suinocultura
brasileira (ZANELA et al., 2001).
2.2 Agente etiológico
O PCV pertence à família Circoviridae, que se subdivide em dois
gêneros: Circovirus e Gyrovirus. O gênero Circovirus compreende os circovírus
suíno tipos 1 e 2 (PCV1 e PCV2), vírus da doença do bico e das penas,
circovírus do canário (CaCV), circovírus do pato (DuCV), circovírus do tentilhão
(FiCV), circovírus do ganso (GoCV), circovírus da gaivota (GuCV), circovírus do
pombo (PiCV) e o circovírus do estorninho (StCV). No gênero Gyrovirus,
apenas uma espécie é conhecida, o vírus da anemia da galinha (CAV) (KATO
et al.,1995; TODD et al., 2001).
Vírus pertencentes à família Circoviridae tem em comum a simetria
icosaédrica e ausência de envelope (Figura 1). O genoma é covalentemente
fechado, medindo de 15 à 17nm, composto por uma fita circular simples de
DNA (característica que permite distingui-los dos demais vírus) (TODD et al.,
2001).
A família Circoviridae é estreitamente relacionada à família
Nanoviridae que acomete as plantas, tem sido proposto que um antepassado
do PCV1 pode ter sido um nanovírus de planta que infectou um hospedeiro
vertebrado e recombinou com um RNA vírus, provavelmente um calicivírus
(GIBBS et al., 1999).
Existem várias pequenas inserções e deleções localizadas em toda
a extensão do genoma do DNA viral que parecem ser responsáveis pelas
diferenças de patogenicidade entre PCV1 e PCV2. Foram sugeridos 11
fragmentos de leitura aberta (ORFs) no genoma, porém apenas ORF1 e ORF2
5
são expressas em ambos os vírus, PCV1 e PCV2. A ORF1 codifica para duas
proteínas de replicação (rep e rep’) e a ORF2 codifica uma proteína do
capsídeo (cap) (Liu, et al., 2006).
Uma sequência de 501 nucleotídeos da ORF2 foi analisada e
permitiu dividir o PCV2 em dois grandes grupos. Nomeados PCV2a e PCV2b.
PCV2a tem 1.767 nucleotídeos e PCV2b tem 1768 nucleotídeos. Estudos
demonstram que o PCV2b é um pouco mais virulento que o PCV2a. No Brasil
existem os dois subtipos (CASTRO, 2005).
Figura 1: Representação esquemática do vírus da circovirose suína. Fonte: Viralzone (2008).
O circovírus resiste à inativação quando exposto a ambiente ácido
(pH 3), a clorofórmio, a temperaturas entre 56ºC e 70ºC, ao congelamento, à
luz ultra-violeta e a desinfetantes. O agente permanece estável em fezes e
secreções respiratórias (SHIBATA et al., 2003).
Estudos revelam que os PCVs podem ser inativados por
desinfetantes alcalinos (hidróxido de sódio), por agentes oxidantes (hipoclorito
de sódio) e por amônio quaternário ou fenol. O PCV2 resiste a ação de
desinfetantes comerciais com base em alcoól, clorexidina ou iodo (ROYER et
al., 2001).
2.3 Epidemiologia e formas de transmissão
O PCV2 acomete exclusivamente suínos. Outras espécies de
interesse pecuário (bovinos, caprinos e ovinos) não revelaram nenhum sinal de
infecção por PCV2. Todas as raças de sus domesticus são susceptíveis a
6
infecção pelo vírus. No caso do javali (sus scrofa), diversos estudos foram
publicados que comprovam a presença de PCV2 nesta espécie (RODRIGUEZ-
ARRIOGA et al., 2003; ELLIS et al., 2003).
O PCV2 é eliminado nas secreções respiratórias, secreções orais,
secreções urinárias e fezes em animais com SMDS, bem como em suínos
infectados, mas aparentemente saudáveis. Suínos clinicamente afetados
eliminam vírus em maior quantidade em comparação com porcos infectados,
mas clinicamente saudáveis. O PCV2 foi igualmente detectado no leite de
porcas, incluindo colostro, e em sêmen de cachaço, sem que existam
alterações na morfologia ou viabilidade dos espermatozóides (HA et al., 2009).
O sêmen de animais infectados com PCV2 pode ser infeccioso.
Lopez-Soria et al., (2011) observaram que matrizes inseminadas com sêmen
infectado pelo vírus da CV, não manifestaram viremia e nem foram detectados
anticorpos para PCV2, o mesmo se passando com os seus fetos. Num outro
estudo porém, marrãs provenientes de granjas livres de patógenos (SPF) foram
inseminadas com sêmen contendo elevada concentração de PCV2. Elas
apresentaram falhas reprodutivas e foi isolado PCV2 nos leitões abortados. No
entanto, não se sabe se a quantidade natural de PCV2 contida no sêmen é
suficiente para infectar as porcas e os leitões (MADSON et al., 2009).
Estudos em que os leitões foram monitorizados a partir da primeira
semana de vida até o momento em que surgiu a doença mostraram uma maior
prevalência de PCV2 em secreções nasais que em retais, apoiando a idéia de
que a via oro-nasal é, provavelmente, a principal via de transmissão horizontal
(GRAU-ROMA et al., 2008).
Existem evidências de que é possível ocorrer a transmissão vertical,
infecção do embrião ou feto no útero, como identificado pelo isolamento de
PCV2 em fetos abortados, com lesões características no miocárdio (LOPEZ-
SORIA et al., 2008).
Estudos epidemiológicos descrevem a presença de um maior
numero de outras infecções ou doenças em explorações afetadas pelo PCV2,
como parvovirose suína, pneumonia por Mycoplasma hyorhinis, doença de
Aujeszky, doença de Glasser, meningite por Streptococcus, salmonelose,
colibacilose pós-desmame e pneumonia bacteriana. Permanece a dúvida, se
as co-infecções facilitam a expressão da SMDS, ou se e a imunossupressão
7
causada pelo PCV2 que facilita o desenvolvimento dessas infecções (LOPEZ-
SORIA et al., 2008).
Num estudo publicado, Pallares et al. (2002), identificaram as co-
infecções mais comuns nos EUA em 484 casos de suínos com SMDS.
Verificou-se que em 52% (251/484) dos casos existia co-infecção com vírus da
síndrome respiratória e reprodutiva suína (PRRS), 36% (172/484) com
Mycoplasma hyopneumoniae, infecções bacterianas em 22% (105/484), vírus
da influenza suína (SI) em 5,4% (26/484) e em apenas 2% dos casos se
observou exclusivamente PCV2.
2.4 Patogenia
O PCV2 possui a capacidade de infectar células de origem epitelial,
endotelial e mielóide. O PCV pode replicar em algumas linhagens celulares
suínas e é dependente de proteínas celulares expressas durante a fase S do
ciclo celular. Dessa forma, a replicação vírica seria mais eficiente em tecidos
com marcada atividade mitótica. Após atingir o sistema linfático ocorre viremia
no sangue e os vírus atingem os órgãos alvos (CASTRO et al., 2007).
2.5 Manifestações clínicas
Alem da SMDS, várias doenças foram associadas ao PCV2 e, atualmente,
são conhecidas como doenças associadas ao circovírus suíno (PCVAD). Neste
grupo estão incluídas a SMDS, síndrome de nefropatia e dermatite suína
(PDNS), falhas reprodutivas, enterite associada ao PCV2, pneumonia
necrosante proliferativa (PNP) e doenças do complexo respiratório suíno
(PRDC) (OPRIESSNIG et al., 2007).
2.5.1 SMDS
A síndrome multissistêmica do definhamento é a doença mais
frequentemente associada ao PCV2. A maioria dos sinais clínicos desta
doença são inespecíficos, mas seis sinais clínicos fundamentais formam a base
do diagnóstico clínico preliminar, presentes na seguinte ordem de freqüência e
8
restritos a animais com idade de oito e 13 semanas: caquexia, dispnéia,
linfoadenopatia, diarréia, palidez e icterícia (Figura 2). Tosse, pirexia, úlcera
gástrica, meningite e morte súbita, também, têm sido relatados, porém são
menos frequentes (MADEC et al., 2000).
De acordo com Ségales et al. (2004), na necropsia, os pulmões não
conseguem entrar em colapso, em alguns casos crônicos os rins têm listras
brancas ou manchas. Porcos acometidos também apresentam hipertrofia dos
linfonodos inguinais, submandibulares, mesentéricos e mediastínicos. Lesões
granulomatosas também podem ser encontradas nos pulmões, fígado, rim,
coração e intestinos.
Depleção linfocitária de diferentes níveis e perda da arquitetura
folicular dos linfonodos são achados comuns em quase todos os animais
afetados. Outro achado importante em animais que manifestam a SMDS é a
presença de inclusões citoplasmáticas basofílicas de PCV2 no interior das
células histiocíticas. Lesões microscópicas observadas nos rins consistem em
nefrite intersticial não purulenta (SEGALES et al., 2004).
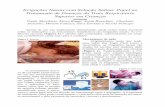
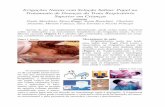
Figura 2: Animais na fase de creche, visualização de um animal com SMDS. Fonte: Opriessnig, 2007.
9
2.5.2 PNDS
O PDNS pode afetar suínos da recria, engorda e, esporadicamente,
animais adultos. A prevalência da síndrome nas explorações afetadas é
relativamente baixa, inferior a 1%.
Os suínos com PDNS apresentam anorexia, depressão, prostração,
relutância em se movimentar e temperatura normal ou alterada. No entanto, o
sinal mais evidente, particularmente na fase aguda da doença, e a presença de
lesões de pele que se caracterizam por máculas e pápulas irregulares,
vermelho a púrpura, que ocasionalmente coalescem para formar grandes
manchas e placas irregulares (Figura 3). Com o tempo, as lesões ficam
cobertas por crostas escuras e desaparecem gradualmente, por vezes
deixando cicatrizes. (CASTRO, 2007)
Segundo Castro (2007), os rins, macroscopicamente, apresentam-se
aumentados, anêmicos e cobertos por petéquias. Os principais achados
microscópicos incluem glomerulonefrite necrosante fibrinosa e vasculite
necrosante sistêmica.
Figura 3: Leitão com sinais clínicos de PNDS. Fonte: Suinocultura em foco (2005).
10
2.5.3 PNP
Forma severa de pneumonia intersticial caracterizada por hipertrofia
e proliferação de pneumócitos tipo 2 e da presença de células necróticas no
interior do alvéolo. O diagnóstico baseia-se em critérios histopatológicos
incluindo a presença de células necróticas, macrófagos e bronqueolite
necrosante (GRAU-ROMA et al., 2008).
2.5.4 Falhas reprodutivas
As granjas acometidas apresentam elevadas taxas de abortamento,
fetos mumificados e leitões natimortos. A principal lesão microscópica está
presente no coração, onde se observa uma miocardite fibrosante e/ou
necrosante (característico de falências reprodutivas associadas ao PCV2)
(SEGALES et al., 2004).
2.5.5 Tremores congênitos
Tremor congênito (CT), também denominado mioclonia congênita,
caracteriza-se pelo tremor da cabeça e pernas de leitões recém-nascidos. O
tremor congênito divide-se em dois tipos (A e B) baseados na presença (A) ou
ausência (B) de mielina no sistema nervoso central ou periférico. O ácido
nucléico do PCV-2 foi detectado em tecido neural e fígado de animais com CT,
permitindo a associação do agente com a enfermidade (SEGALÉS et al.,
2004).
2.5.6 Enterite associada ao PCV2
Os casos de enterite associada ao PCV2 são cada vez mais
frequentes. A maior parte dos suínos atingidos tem entre oito a 16 semanas de
idade. A ocorrência de enterite associada ao PCV2 é semelhante na forma
clínica e de lesões a ileíte subaguda ou crônica associada à Lawsonia
intracellularis. A mucosa intestinal apresenta-se muito espessada e os
linfonodos mesentéricos hipertrofiados (Figura 4). O exame microscópico
11
confirma a presença de enterite granulomatosa, que é geralmente associada a
abundantes cargas de antígeno de PCV2 (KIM et al. 2001).
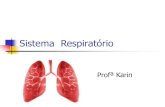
Figura 4- A- Antígenos de PCV2 com coloração marrom dentro de linfócitos e macrófagos nas células da lâmina própria do íleo. B- Espessamento da mucosa intestinal e aumento dos linfonodos mesentéricos. C- Animal com diarréia leve Fonte: Opriessnig, 2007.
12
3 IMUNOLOGIA
A sintomatologia clínica das doenças associadas ao PCV2 sugere
uma disfunção imunológica. Em geral observa-se hipertrofia dos linfonodos,
extensas lesões linfóides e alteração nos padrões de citocinas liberadas no
sangue e tecidos linfóides.
As alterações observadas nos animais afetados sugerem que há
uma incapacidade dos animais em montar uma resposta imunológica
adequada. As lesões relacionam-se à diminuição dos linfócitos B e T e
aumento de monócitos e macrófagos no sangue e tecidos (SEGALES et al.,
2004).
Estudos indicam que apesar de estarem presente em células
endoteliais, epiteliais e linfócitos, o PCV2 tem como principal alvo as células
apresentadoras de antígenos – macrófagos e células dendríticas (CDs). E
embora elas mantenham a capacidade de apresentar antígenos para os
linfócitos, é a sua capacidade de reconhecimento antigênico que se encontra
alterada (FRANÇA et al., 2005).
Ainda é desconhecida se a redução de linfócitos em suínos afetados
pelo PCVAD é devido a uma menor produção desses na medula óssea,
redução da proliferação de tecidos linfóides secundários, ou aumento da perda
de linfócitos na medula óssea, sangue periférico e tecidos linfóides secundários
através de necrose ou apoptose induzida pelo vírus (OPRIESSNIG et al.,
2007).
O PCV2 interfere com a produção dos fatores de maturação por
parte das CDs plasmocíticas, impedindo, desta forma, a ativação dos linfócitos
T por parte das CDs mielóides maduras, que tem como consequência a
ausência de respostas imunitárias específicas contra outros agentes
patogênicos (MCCULLOUGH et al., 2009)
O PCV2 induz as células mononucleares a produzir grande
quantidade de interleucina 10 (IL-10) interferindo com as respostas antigênicas
de memória através da inibição de IFN-γ, IFN-α e IL-12. O PCV2 também inibe
a produção de IL-2, através de um mecanismo independente da IL-10. Estas
observações indicam que a infecção por PCV2, leva a ausência de respostas
13
antígeno – específicas, tornando desta forma os animais suscetíveis a infecção
por outros agentes patogênicos (FORT, 2009).
O PCV2 possui também a capacidade de induzir a expressão de
MCP1 (proteína 1 quimiotáxica para macrófagos), em macrófagos e outras
células inflamatórias dos linfonodos afetados, atraindo assim mais células
mononucleares que serão responsáveis pela formação das macrófagos
epitelióides e células gigantes que, por sua vez, são iniciadores do processo
inflamatório granulomatoso encontrados nos animais acometidos pelas PCVAD
(FRANÇA, et al., 2005).
4 FATORES QUE MODULAM DOENÇAS CAUSADAS POR PCV2
4.1 Fatores virais
A resistência aos desinfetantes deve-se a ausência de um envelope
externo. Além disso, a resistência a elevadas temperaturas levou a concluir que
os produtos derivados de plasma suíno possam conter vírus residual viável
(GRAU-ROMA et al., 2011).
Apesar do PCV2 estar associado a diversas síndromes clínicas, não
existe diferenças significativas no genoma dos vírus analisados de síndromes
diferentes. Análise da seqüência de PCV2 de suínos afetados por PCVAD e
suínos com infecção, porém clinicamente saudáveis, mostrou homologia de
seqüência de 95,6 a 100%. Isto indica que há outros fatores que afetam a
expressão da doença. Tem sido demonstrado que PCV2 isolados de suínos
clinicamente saudáveis podem causar PCVAD em condições experimentais
(HASSLUNG et al., 2005).
Foi demonstrado que duas mutações de aminoácidos no genoma do
PCV2 alteraram significativamente as lesões macroscópicas e histopatológicas
em suínos, indicando que apenas pequenas alterações no genoma viral são
necessárias para alterar a função do vírus. A detecção de grandes quantidades
de PCV2 no soro indica um aumento da probabilidade do animal desenvolver
quadro clínico, mas não o suficiente para estabelecer o diagnóstico individual
(FENAUX et al., 2004).
14
4.2 Fatores do hospedeiro
Todas as raças de suínos parecem ser suscetíveis à infecção e
doença clínica, porém existe uma maior prevalência em animais de raça pura
do que em mestiços. Os animais machos são mais suscetíveis quando
comparado as fêmeas, leitões com baixo peso ao nascer tem maior
suscetibilidade de desenvolver alguma síndrome do que os demais leitões, o
índice de mortalidade de leitões que nascem de porcas infectadas por PCV2 é
significativamente maior (GRAU-ROMA et al., 2011).
Em um estudo feito por Opriessnig et al. (2009), 39 animais da raça
pietran e 39 da raça landrace, provenientes da mesma propriedade e
submetidos as mesmas condições de manejo, foram inoculados com PCV2 e
necropsiados 21 dias após inoculação. A severidade das lesões da raça
landrace foi significamente maior quando comparadas as da raça pietran,
indicando que existe um fator genético influenciando a severidade da doença.
4.3 Co-infecções
O diagnóstico e o controle de outros agentes infecciosos
encontrados em suínos afetados por PCVAD, diminui a severidade da afecção
e melhora os índices zootécnicos da granja (OPRIESSNIG et at., 2007).
Experimentalmente, a vacinação de fêmeas infectadas por PCV2
contra Erysipelothrix rhusiopathiae e PPV, reduziu o número de leitões
mumificados. Além disso, os leitões nascidos de porcas infectadas por PCV2 e
vacinadas foram menos suscetíveis de manifestar SMDS do que os
provenientes de porcas infectadas por PCV2 e não vacinadas (ROSE et al.,
2007).
Até o momento, as medidas implementadas para tratar as PCVAD
através do uso de drogas não foram eficazes (MADEC et al., 2008).
4.4 Imunomodulação
A imunossupressão do hospedeiro é fundamental para que ocorram
os casos de PCVAD no suíno (OPRIESSNIG et al., 2007).
15
Num estudo onde 12 leitões com um dia de vida foram inoculados
com PCV2, um grupo foi tratado com dexametasona e outro com ciclosporina.
No grupo com ciclosporina houve a constatação de maior replicação do PCV2
e disseminação para os hepatócitos além de ausência de reações inflamatórias
típicas de PCVAD, indicando que as lesões inflamatórias granulomatosas são
imunomediadas (KRAKOWKA et al., 2002).
Em outro estudo, leitões retirados via cesariana, sem ingestão de
colostro, foram inoculados com PCV2 e um grupo recebeu tratamento com
dexametasona, neste grupo observou-se lesões inflamatórias típicas de
PCVAD enquanto que no outro não foram observadas lesões, concluindo que a
supressão da imunidade mediada por células desempenha um papel
importante na PCVAD (KAWASHIMA et al., 2003).
5 DIAGNÓSTICO
A vasta disseminação do PCV2 na população de suínos, representa
uma dificuldade na avaliação do estado sanitário de uma exploração. Por esta
razão, um PCR ou sorologia positivos apenas indicam a presença de infecção,
não sendo em nenhum caso indicativo de doença (CASTRO, 2007).
Devido a este fato, Sorden (2000) propôs uma definição de
diagnóstico baseado em três pressupostos:
presença de sinais clínicos como atraso no crescimento, diarréia,
transtornos respiratórios, hipertrofia dos linfonodos (principalmente os
inguinais), e em alguns casos icterícia.
lesões histológicas presentes como depleção linfocitária nos
órgãos e no sangue, inflamação granulomatosa em qualquer órgão e
corpúsculos de inclusão de PCV2.
Detecção de PCV2 nas referidas lesões.
No caso de PDNS é imprescindível a presença de lesões cutâneas
hemorrágicas e necrosantes, além de vasculite necrosante sistêmica e
glomerulonefrite necrosante fibrinosa. Nos problemas reprodutivos deve-se
constatar abortos ou presença de natimortos com hipertrofia cardíaca do
coração fetal. Em casos de enterite associas ao PCV2 constata-se diarréia
16
persistente, lesões nas placas de Peyer com grande quantidade de antígeno de
PCV2 (SEGALES et al., 2005).
A grande gama de manifestações clínicas do circovírus suíno exige
um extenso e variável diagnóstico diferencial, sendo as principais enfermidades
a considerar: peste suína clássica, peste suína africana, eperitrozoonose,
erisipelose, doença de Aujesky, doença de Glasser, salmoneloses, parvovírus
suíno e enterites, entre outras (OPRIESSNIG, 2007).
5.1 Técnicas de diagnóstico laboratorial
5.1.1PCR
A demonstração de ácido nucléico de PCV2 por PCR não substitui a
avaliação clínica dos suínos e avaliação histopatológica dos tecidos, uma vez
que muitos suínos saudáveis são positivos para PCV2 sem estarem afetados
por PCVAD.
Um PCR quantitativo determina a quantidade de ácido nucléico viral
em soro e tecidos, portanto tem um valor preditivo da evolução clínica,
podendo ser bastante útil no diagnóstico (SEGALES et al., 2005).
5.1.2 ―In situ hibridization‖ e imunohistoquímica
A ―in situ hibridization‖ (ISH) para PCV2 utiliza uma sonda de DNA
marcada que corresponde a uma parte do genoma do PCV2. Na
imunohistoquímica (IHQ) utiliza-se um anticorpo monoclonal ou policlonal para
detectar antígeno de PCV2 em secções de tecido fixadas com formol e
embebidas em parafina. A ISH demonstra ser mais específica (OPRIESSNIG et
al., 2007)
17
6 CONTROLE
6.1 Medidas higiênicas
A correta adoção de medidas de manejo permite um adequado
controle sobre as causas que levam ao aparecimento das PCVAD. Em geral
propriedades acometidas por PCV2 apresentam muitos erros de manejo e de
forma a superar essas deficiências, Madec criou um conjunto de medidas de
manejo que ficaram conhecidas como o plano dos 20 princípios de Madec
(quadro 1) (SEGALES et al., 2005).
Qabela 1- 20 princípios de Madec
Setor da Granja
Medidas a serem adotadas
Maternidade 1.Esvaziamento, limpeza e desinfecção de fossas e canaletas
2.Lavar as matrizes e fazer uso de antiparasitários
3.Evitar adoções de leitões por outra matriz
4.Usar programas de vacinação adequados
Creche 5.Uso de pequenas pocilgas com paredes divisórias sólidas
6.Esvaziamento, limpeza e desinfecção de fossas e canaletas
7.Densidade animal: 3 suínos por m2
8.Bebedouro com 7 cm por leitão
9.Boa ventilação
10. Manter temperaturas de conforto
11.Não misturar lotes de animais
Engorda 12.Uso de pequenas pocilgas com paredes divisórias sólidas
13.Esvaziamento, limpeza e desinfecção de fossas e canaletas
14.Densidade animal: 0.75m2 por animal
15. Assegurar boa ventilação e temperatura adequada
16.Não misturar animais de diferentes lotes
17.Não misturar animais de diferentes idades
Todos os setores
18.Respeitar o fluxo de animais e de ar
19.Respeitar regras de higiene quando da intervenção como castrações, injeções, etc...
20.Remover casos confirmados de PCVAD para a enfermaria
Além dos princípios indicados por Madec, Gadd (2006), preconizou
diversas outras formas de controlar as PCVAD, como: Adquirir animais de
reposição apenas de granjas clinicamente livres de PCVAD; Assegurar que o
veículo de transporte passe por procedimentos de desinfecção e que seu
condutor deva sempre circular com roupas e calçados adequados e limpos, e
18
sempre que possível, evitar que ele entre na exploração ou se aproxime dos
animais; Descarregar os novos animais para a quarentena e observá-los
regularmente; Utilizar apenas desinfetantes comprovadamente eficazes
incluindo os rodilúvios e pedilúvios; Assegurar que não existe acesso não
autorizado à granja; Controle de pragas eficaz contra roedores e especialmente
aves; Implementar o sistema tudo dentro/tudo fora, em todas as fases da
produção; Certificar que as superfícies estão corretamente limpas antes de
aplicar o desinfetante; Ter especial atenção ao fato de que o PCV2 pode
sobreviver nos tubos e nos tanques de água.
No caso de uma epidemia de PCVAD, Gadd (2006) indica algumas
medidas para minimizar o impacto, como: Na fase inicial da epidemia, apenas
uma porcentagem de leitões estão afetados (10-15%). De modo a evitar o
contagio de outras ninhadas e a disseminação viral, deve-se evitar adoções e
utilizar apenas uma seringa por ninhada; Verificar a estratégia de vacinação
para as doenças que favorecem a disseminação do PCV2 na exploração ou
que podem atuar como co-fatores, como o parvovírus suíno e doenças
respiratórias; Evitar densidades excessivas de população, pocilgas mal
ventiladas, variações de temperatura e correntes frias; não permitir a
acumulação de sujidades nas salas de parto e creche para evitar a persistência
viral.
6.2 Medidas sanitárias
Anteriormente ao uso das vacinas, que ocorreu a partir de 2006, o
controle da circovirose suína estava centrado nas boas práticas de produção,
evitando o estresse animal, controlando as co-infecções e eliminando fatores
de risco que induziam a imune-estimulação (OPRIESSNIG et al., 2007).
Opriessnig et al., (2007) observaram uma maior mortalidade de
leitões nascidos de porcas que apresentavam viremia e também de porcas com
baixo título de anticorpos para PCV2, significando que estes baixos títulos de
anticorpos estavam diretamente relacionados com a mortalidade dos leitões.
19
Os leitões que ingeriram o colostro e possuíam anticorpos de origem
maternal tiveram menor predisposição a desenvolver SMDS e menor
mortalidade (LOPÉZ-SÓRIA et al., 2008).
Porém os anticorpos maternos apenas limitam a circulação e
excreção viral, não sendo totalmente eficazes na prevenção da infecção pelo
PCV2. O animal torna-se mais susceptível a partir do declínio dos anticorpos
adquiridos via colostro até o completo desenvolvimento da imunidade ativa,
que ocorre no período de creche, por volta da quinta à oitava semana de vida
(MADEC et al., 2008).
Como as PCVAD estão associadas à forte estimulação do sistema
imune, Radostitis et al., (2007) levantaram a hipótese de que as vacinas e seus
adjuvantes teriam a capacidade de agravar as manifestações clínicas do PCV2,
baseando-se no fato de as vacinas conterem antígenos que estariam atuando
como agentes virais, bacterianos, ou ainda como imuno-estimulantes.
Os mesmos autores observaram que todos os adjuvantes utilizados,
num período precoce da infecção, aumentaram a depleção linfocitária, em
fases mais tardias da infecção (35 dias pós infecção), a duração da viremia e
os níveis de PCV2 no soro (RADOSTITIS et al., 2007).
A seroterapia foi também uma medida bastante utilizada. Consistia
na colheita do sangue dos animais que sobreviviam à infecção e, portanto
tinham elevados títulos de anticorpos que eram injetados, via peritoneal, nos
animais com o objetivo de conferir proteção antes do período crítico de
emagrecimento. Embora a ocorrência de alguns resultados inconsistentes, a
seroterapia obteve certo sucesso, pois diminuiu a mortalidade dos animais.
Porém deve-se considerar o seu grande risco para a biossegurança (MADEC
et al., 2008).
As primeiras vacinas foram preparadas a partir de pulmão ou de
tecido linfóide obtidos a partir de suínos acometidos por PCVAD e inativados
por formaldeído (vacinas autógenas). Foram usadas por alguns profissionais
para combater os prejuízos associados ao PCV2. Tendo sido relatado uma
diminuição considerável da mortalidade (de 20% para 3%). Esta prática
todavia, também apresenta risco de biossegurança (GRAU-ROMA et al., 2011).
O aparecimento das vacinas para PCV2 revolucionou os aspectos
referentes ao controle das PCVDA, demonstrando resultados extremamente
20
positivos com relação a diminuição das lesões e à mortalidade (LOPÉZ-SÓRIA
et al., 2008).
Até o presente momento, quatro vacinas já foram produzidas
(Quadro 2) e são baseadas em cepas do genótipo PCV2a. A primeira vacina no
mercado foi a CIRCOVAC®, do laboratório Merial, com PCV2 inativado,
adjuvante oleoso para uso em matrizes e marrãs de duas a quatro semanas
antes da parição (GRAU-ROMA et al., 2011).
As outras três vacinas comerciais são vacinas recombinantes,
utilizadas em suínos em crescimento, ao redor da terceira semana de idade.
Suvaxyn PCV2 OneDose® é produzida com base em um vírus quimérico da
infecção, que contém o gene imunogênico ORF2 Cap do PCV2, inserido na
estrutura genômica central não patogênica do PCV1. Ingelvac CircoFLEX® e
Porcilis PCV® Circumvent® são vacinas de subunidades baseadas em um
produto do ORF2 expresso no baculovírus (KEKARAINEN et al., 2010).
Quadro 2 – vacinas comerciais.
Vacina Laboratório Antígeno Posologia Licenciado para
CIRCOVAC® Merial PCV2 inativado
2ml duas doses para primíparas e depois 1 dose por ciclo
Reprodutoras
Porcilis PCV® Circumvent®
Intervet Proteína ORF2 de PCV2
2ml uma dose Leitões > 3 semanas
Ingelvac CircoFLEX®
Boehringer Ingelheim
Proteína ORF2 de PCV2
1ml uma dose Leitões > 2 semanas
Suvaxyn PCV2 One Dose®
Fort Dodge Quimera inativada PCV1-PCV2
2ml duas doses
Leitões > 4 semanas
Embora a vacinação das matrizes garanta que os leitões recebam
grande quantidade de anticorpos maternos, estudos feitos por Madson et al.,
2008 indicaram que transmissão vertical de PCV2 de fêmeas vacinadas aos
seus leitões pode ocorrer.
Antes do uso das vacinas, deve-se confirmar o diagnóstico de
circovirose suína, e lembrar que a síndrome por ela causada é multifatorial, e
21
por isso deve-se levar em consideração a influência dos fatores de risco e
adotar medidas de manejo para prevenção e controle (MADEC et al., 2008).
Lyoo et al. (2010) realizaram um estudo comparativo com três
vacinas comerciais e observaram que em cada um dos três lotes de suínos
vacinados houve redução do número de animais com viremia quando
comparados ao grupo controle que foi infectado e não recebeu nenhum tipo de
vacina.
Em um estudo similar Opriessnig et al. (2009) observaram uma
diminuição da viremia em animais vacinados para PCV2 e também uma menor
severidade das lesões linfóides quando comparados ao grupo controle não
vacinado e infectado.
O uso de vacinas deve ser aplicado após uma análise da relação
custo-benefício.
22
7 CONSIDERAÇÕES FINAIS
O circovírus suíno (PCV2) está amplamente disseminado no
rebanho suíno mundial, acarretando graves prejuízos econômicos. A
variabilidade dos sinais clínicos das PCVADs torna a doença de difícil
diagnóstico, sendo por vezes confundida com uma gama de doenças. Isto
acarreta um retardo na adoção de medidas de controle trazendo grandes
prejuízos econômicos.
Programas de controle incluem aspectos de manejo, nutrição e
imunização, o advento das vacinas possibilitou uma redução na mortalidade e
diminuição dos sintomas clínicas. Ainda não há um programa de controle 100%
eficaz e as medidas atualmente preconizadas devem ser adaptadas de granja
para granja.
Mais estudos devem ser feitos para se conseguir uma vacina
totalmente eficaz em prevenir a infecção e seu exato momento de aplicação
para que não haja interferência dos anticorpos maternos.
23
REFERÊNCIAS
1. ABIPECS. Associação brasileira da indústria produtora e exportadora de carne suína. Disponível em http://www.abipecs.org.br. Acessado em 10 de setembro de 2011.
2. CAPRIOLI A.; MCNEILLY F.; MCNAIR I.; LAGAN-TREGASKIS P.;
ELLIS J.; KRAKOWKA S.; MCKILLEN J.; OSTANELLO F.; ALLAN G. PCR detection of porcine circovirus type 2 (PCV2) DNA in blood, tonsillar and faecal suabes from experimentally infected pigs. Res.Vet. Sci. 81:287-292. 2006.
3. CASTRO, A.M.M.G. Caracterização genética de amostras brasileiras de
Circovírus suíno tipo 2 (PCV-2). 120f. Tese (Doutorado em Medicina Veterinária – Área de Epidemiologia Experimental e Aplicada às Zoonoses) Faculdade de Medicina Veterinária e Zootecnia,Universidade de São Paulo, São Paulo, 2005.
4. CASTRO A.M.M.G.; CORTEZ, M.B.; HEINEMANN, P.; BRANDÃO, L.J.;
RICHTZENHAIN T. Arq. Inst. Biol., São Paulo, v.74, n.3, p.281-291, jul./set., 2007.
5. ELLIS, J.; SPINATO, M.; YONG, C.; WEST, K.; MCNEILLY, F.;
MEEHAN, B.; KENNEDY, S.; CLARK, E.; KRAKOWKA, S.; ALLAN, G. Porcine Circovirus 2–associated disease in Eurasianwild boar. Journal of Veterinary Diagnostic Investigation, 15, 364–368, 2003.
6. FENAUX, M.; OPRIESSNIG, T.; HALBUR, P.G. Two amino acid
mutations in the capsid protein of type 2 porcine circovirus (PCV2) enhanced PCV2 replication in vitro and attenuated the virus in vivo . Journal of Virology. 78, 13440 – 13446, 2004.
7. FRANÇA, T.N.; RIBEIRO, C.T.; CUNHA, B.M.; PEIXOTO, P.V.
Circovirose suína. Pesq. Vet. Bras. 25(2):59-72, abr./jun. 2005.
8. FORT, M.; FERNANDES, L.T.; NOFRARIAS, M.; DIAZ, I.,; SIBILA, M.; PUJOLS, J.; MATEU, E.; SEGALES, J. Development of cell-mediated immunity to porcine circovirus type 2 (PCV2) in caesarean-derived, colostrum-deprived piglets. Veterinary Immunology and Immunopathology, oi:10.1016/j.vetimm.2008.12.024, 2009.
9. GADD, J. PMWS. John Gadd descubre Lo que los libros de texto no
cuentan. (pp. 217-224). In Producción Porcina. Saragoca, Espanha: SERVET, 2006.
10. GIBBS M ,; WEILLER G. Evidence that a plant virus switched hosts to
infect a vertebrate and then recombined with a vertebrate-infecting virus . Proc Natl Acad Sci USA 1999 ; 96 : 8022 – 8027.
24
11. GRAU-ROMA, L.; CRISCI, E.; SIBILA, M.; LOPEZ-SORIA, S.; NOFRARIAS, M.; CORTEY, M.; FRAILE, L.; OLIVERA, A.; SEGALES, J. A proposal on porcine circovirus type 2 (PCV2) genotype definition and their relation with postweaning multisystemic wasting syndrome (PMWS) occurrence. Veterinary Microbiology, 128, 23-35, 2008.
12. GRAU-ROMA L.; CRISCI E.; SIBILA M.; LÓPES-SORIA S.;
NOFRARIAS M.; CORTEYM.; FRAILE L.; OLVERA A.; SEGALÉS J.. A proposal on porcine circovirus type 2 (PCV2) genotype definition and their relation with postweaning multisystemic wasting syndrome (PMWS) occurrence. Vet. Microbiol. 138:53-61. 2009.
13. GRAU ROMA, L.; FRAILE L.;, SEGALÉS, J. Recent advances in the
epidemiology, diagnosis and control of diseases caused by porcine circovirus type 2. The Veterinary Journal. 187, 23–32, 2011.
14. HA, Y.; AHN, K.K.; KIM, B.; CHO, K.-D.; LEE, B.H.; OH, Y.-S.; KIM, S.-
H.; CHAE., C. Evidence of shedding of porcine circovirus type 2 in milk from experimentally infected sows. Research in Veterinary Science, 86, 108–110, 2009.
15. HAMEL, A.L.; LIN, L.L.; NAYAR, G.P.S. Nucleotide sequence of porcine
circovirus associated with postweaning multisystemic wasting syndrome in pigs. Journal of Virology, 72 (6), 5262–5267, 1998.
16. HASSLUNG F.; WALLGREN P.; LADEKJAER-HANSEN A.S.;
Experimental reproduction of postweaning multisystemic wasting syndrome (PMWS) in pigs in Sweden and Denmark with a Swedish isolate of porcine circovirus type 2 . Vet Microbiol 106, 49 – 60, 2005
17. KATO, A.; FUJINO, M.; NAKAMURA, T.; ISHIHAMA, A.; OTAKI, Y.Gene organization of chicken anemia virus. Virology,v.209, n.2, p.480-488, 1995.
18. KAWASHIMA, K.; TSUNEMITSU, H.; HORINO, R.; Effects of
dexamethasone on the pathogenesis of porcine circovirus type 2 infection in piglets. J Comp Pathol 129:294–302, 2003.
19. KEKARAINEN, T.; MCCULLOUGHB, K.; FORTA M.; FOSSUMC C.;
SEGALÉS J.; Allane G.M. Immune responses and vaccine-induced immunity against Porcine circovirus type 2. Veterinary Immunology and Immunopathology 136,185–193, 2010.
20. KIM, J.; CHOI, C.; H AN, D.U.; C HAE, C. Simultaneous detection of
porcine circovirus type 2 and porcine parvovirus in pigs with PMWS by multiplex PCR. Veterinary Record. v.149, n.8, p.304-305, 2001.
21. KRAKOWKA S.;, ELLIS J.A.; MCNEILLY F. Immunologic features of
porcine circovirus type 2 infection. Viral Immunology 15:567–582, 2002.
25
22. LIU, J.; CHEN, I.; DU, Q.; CHUA, H.; KWANG, J. The ORF3 protein of porcine circovirustype 2 is involved in viral pathogenesis in vivo. Journal of Virology, 80, 5065-5073, 2006.
23. LÓPEZ-SORIA S.; SEGALÉS J.; ROSE N.; VINAS M.J.; BLANCHARD
P.; MADEC F.; JESTIN A.; CASAL J.; DOMINGO, M. Exploratory study on risk factors for postweaning multisystemic wasting syndrome (PMWS) in Spain. Prev. Vet. Med. 69:97-107, 2005.
24. LOPEZ-SORIA, S.; GRAU-ROMA, L.; SEGALES, J. Epidemiologia de la
circovirosis porcina.Suis, 49, 14-23, 2008.
25. LYOO, K.; JOO, H.; CALDWELL, B.; KIM,H.; DAVIES, P.R.; TORRISON, J. Comparative efficacy of three commercial PCV2 vaccines in conventionally reared pigs. The Veterinary Journal, doi: 10.1016/j.tvjl.2010.06.015, 2010.
26. MADEC, F.; EVENO, E.; MORVAN, P.; HAMON, L.; BLANCHARD,
P.;CARIOLET, R.; A MENNA, N.; MORVAN, H.; TRUONG, C.; M AHÉ,D.; ALBINA, E.; JESTIN, A. Post-weaning multisystemicwasting syndrome (PMWS) in pigs in France: clinical observation from follow-up studies on affected farms. Livestock Production Science, v. 63, p. 223-233, 2000.
27. MADEC, F.; ROSE, N.; GRASLAND, B.; CARIOLET, R.; JESTIN, A.
Post-weaning multisystemic wasting syndrome and other PCV2-related problems in pigs: a 12-year experience. Transboundary and Emerging Diseases, 55, 273-283, 2008.
28. MADSON, D.M.; PATTERSON, A.R.; RAMAMOORTHY, S.; PAL, N.;
MENG, X.J.; OPRIESSNIG,T. Effect of porcine circovirus type 2 (PCV2) vaccination of the dam on PCV2 replication in utero. Clin. Vac. Immunol. 2008.
29. MADSON, D.; PATTERSON, A.; RAMAMOORTHY, S.; PAL, N.; MENG,
X.J.; OPRIESSNIG, T. Reproductive failure experimentally induced in sows via artificial inseminationwith semen spiked with porcine circovirus type 2 (PCV2). Veterinary Pathology 46, 707–716, 2009.
30. MCCULLOUGH, K. C.; RUGGLI, N.; SUMMERFIELD, A. Dendritic
cells—At the front-line of pathogen attack. Veterinary Immunology and Immunopathology, 128, 7-15, 2009.
31. MEEHAN, B.M.; MCNEILLY, F.; TODD, D.; KENNEDY, S.; JEWHURST, V.A.; ELLIS, J.A.; HASSARD, L.E.; CLARK, E.G.; HAINES, D.M.; ALLAN, G.M. Characterization of novel circovirus DNAs associated with wasting syndromes in pigs. Journal of General Virology, 79, 2171–2179, 1998.
26
32. PALLARES F.J.;, HALBUR P.G.; OPRIESSNIG T.. Porcine circovirus type 2 (PCV-2) coinfections in US field cases of postweaning multisystemic wasting syndrome (PMWS) . J Vet Diagn Invest 2002 ; 14 : 515 – 519 .
33. OPRIESSNIG, T.; MENG, X.J.; HALBUR, P.G.; Porcine Circovirus Type
2Associated Disease: Update on Current Terminology, Clinical Manifestations,Pathogenesis, Diagnosis, and Intervention Strategies DOI: 10.1177/104063870701900601 J VET Diagn Invest 2007 19: 591
34. OPRIESSNIG, T.; PATTERSON A. R.; MADSON, D. M.; PAL N.;
ROTHSCHILD, M.; KUHAR, D.; LUNNEY, J. K.; JUHAN, N. M.; MENG X. J.; HALBUR, P. G. Difference in severity of porcine circovirus type 2 (PCV2)-induced pathological lesions between Landrace and Pietrain pigs J ANIM SCI. 2009.
35. OPRIESSNIG, T.; PATTERSON, A.R.; MADSON, D.M.; PAL, N.;
HALBUR, P.G. Comparison of efficacy of commercial one dose and two dose PCV2 vaccines using a mixed PRRS-PCV2-SIV clinical infection model 2-3 months pos vaccination. Vaccine 27, 1002 – 1007, 2009.
36. RADOSTITS, O.M.; GAY, C.C.; HINCHCLIFF, K.W.; CONSTABLE, P.D. Disease associated with viruses and Chlamydia – I. In Veterinary Medicine (pp. 1185-1193). Espanha: Saunders Elsevier. 2007.
37. RODRIGUEZ-ARRIOGA G.M.; SEGALES, J.; ROSELL, C.; ROVIRA, A.;
PUJOLS, J.; PLANA-DURAN, J.; DOMINGO, M. Retrospective study on porcine circovirus type 2 infection in pigs from 1985 to 1997 in Spain. Journal of Medicine Veterinary, 50, 99-101, 2003.
38. ROSE, N.; BLANCHARD, P.; CARIOLET, R.; GRASLAND, B.; AMENNA,
N.; OGER, A.; DURAND, B.; BALASCH, M.; JESTIN, A.; MADEC, F. Vaccination of porcine circovirus type 2 (PCV2)-infected sows against porcine Parvovirus (PPV) and Erysipelas: effect on post-weaning multisystemic wasting syndrome (PMWS) and on PCV2 genome load in the offspring. Journal of Compared Pathology, 136, 133-144, 2007.
39. ROYER, R.L.; NAWAGITGUL, P.; HALBUR, P.G.; PAUL, P.S.
Susceptibility of porcine circovirus type 2 to commercial and laboratory disinfectants. Journal of Swine Health and Production, 9 (6), 281-284, 2001.
40. SEGALES, J.; ROSELL, C.; DOMINGO, M. Pathological findings
associated with naturally adquired porcine circovirus type 2 associated diseases. Veterinary Microbiology, 98,137-149, 2004.
41. SEGALES, J.; ALLAN, G.M.; DOMINGO, M. Porcine circovirus diseases.
Animal Health Research Reviews, 6 (2), 119-142, 2005.
27
42. SEGALES, J. (2007). Historia y controversia de la enfermedad. Disponível em http://www.3tres3.com/buscador/noti.php?sec=circovirosis_porcina&id=2040&palabra_clave=historia%20y%20controversia%20de%20la%20enfermedad&b_seccion=todo&ajax=2. Acessado em 12 de setembro de 2011.
43. SHIBATA I.; OKUGA Y.; YAZAWA S.; ONO M.; SASAKI T.; ITAGAKI M.;
NAKAJIMA N.; OKABE Y.; HIDEJIMA I. PCR detection of porcine circovirus type 2 DNA in whole blood, serum, oropharyngeal swab, and feces from experimentally infected pigs and field cases. J. Vet. Med. Sci. 65(3):405-408, 2003.
44. SORDEN, S.D. Update on porcine circovirus and postweaning
multisystemic wasting syndrome (PMWS). Swine Health and Production, 8 (3), 133-136, 2000.
45. SUINOCULTURA EM FOCO. 2005. Disponível em
http://suinotec.com.br/suinofotos_dados_indices.php?id=25. Acessado em 05 set 2011.
46. TISCHER, I.; RASCH, R.; TOCHTERMANN, G. Characterization of papovavirus and picornavirus-like particles inpermanent pig kidney cell lines. Zentralblatt furBakteriologie, Abt.1 Originale A, v.226, p.153-167, 1974.
47. TISCHER, I.; GELDERBLOM, H.; VETTERMANN, W.; KOCH, M. A. A
very small porcine virus with a circular singlestranded DNA. Nature, v.295, p.64-66, 1982.
48. TISCHER, I.; MIELDS, W.; WOLFF, D.; VAGT, M.; GRIEM, W. Studies
on Epidemiology and Pathogenicity of Porcine Circovirus. Archives of Virology, v.91, p.271-276, 1986.
49. TODD, D.; WESTON, J.H.; SOIKE, D.; SMYTH, J.A. Genome sequence
determinations and analyses of novelcircoviruses from goose and pigeon. Virology, v.286, n.2, p.354-362, 2001.
50. TODD D.; BENDINELLI M.; BIAGINI P. Circoviridae.In: Ball virus
taxonomy, Eighth report of the international committee on taxonomy of viruses, ed. Fauquet MA, Mayo J,Maniloff U, Desselberger LA, pp. 327–334. Elsevier Academic Press, San Diego, CA, 2007.
51. VIRALZONE. 2008. Disponível em
http://viralzone.expasy.org/all_by_species/118.html. Acessado em 03 de set. 2011.