USP · . UNIVERSIDADE DE SÃ9 PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS Programa de...
Transcript of USP · . UNIVERSIDADE DE SÃ9 PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS Programa de...

. UNIVERSIDADE DE SÃ9 PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS
Programa de Pós-GradUação em Farmácia · 'Área de Análises Clínicas
Cryptosporidium 'parv~m: es~abe.leci~ento de modelo experimental em . .
camuridongo ir'nunossuprímido com dexametasona
Matheus Diniz Gonçalves Coêlho
Dissertação para obtenção do grau de MESTRE
Orientadora:
Profª Di<!Hermínia Yohko Kanamura
São Paulo 2004
(Nota da BCQ: Não foi possível ca pturar fie lmente a im agem das fig uras desta dissertação)

Fi llYIOi út de Ciencias Farmacêutieq$ Universidade de São Paulo 1
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS
- Programa de Pós-Graduação em' Farmácia Área de Análises Clínicas
. r '
Cryptosporidium parvum:__estabetecimento de modelo experimental em
-'
camundongo ímunossuprimido com dexametasona
/ Matheus Diniz-Gonçalves C~lho ·
Dissertãção para obtenção do grau de . · MESTRE
. '
Orientadora: ·: lPror- brªHermínia Yohko Kanamura :
São Paulo 2004

,j
DEDALUS - Acervo - CQ
11111111111111 30100006172
(
Fi cha Catahrgráfica ElaborJ,!J pda Divisão de Biblioteca e
Docurrientação do Conjunto das Químicas da USP.
Coêlho , Matheus Diniz Gonçalves
' ,,
C(i 72c Cryptosporidium parvum : estabelec imento de modelo expe r imental em camundongo imunossuprimido com dexametasona / Matheus Diniz Gonçalves ·Coê lho. São Pau lo, 2004.
57p.
Disse rtação (mestrado) - Faculdade de Ciências Farmacêuticas da Uni'versidade de São Paulo. Departamento de Análises Clínicas e Toxicológicas.
Orientador: Kan a mura, Hermínia Yohko
1. Parasitologia 4 . Anti inflamatório orientador.
2. Imunologia 3. Protozoa: Zoo logia J. T. II. Kanamu ra ,, Hermínia Yohko,
616.96 CDD

Matheus Diniz Gonçalvês Coêlho
Cryptosporidium parvum: estabelecimento de modelo experimental em
camundongo imunossuprimido é:om dexametasona
Comissão Julgadora da
Dissertação para obtenção do grau de Mestre
ProfªDrª Herminia Yohko Kanamura ·orientador/Presidente
Profª Drª Irene da Silva Soares 1Q examinador .
Profª Drª Solange Maria Gennari ' 2• eiraminador
São Paulo, 27 de Agosto de 2004.

. l
'
'\
L~ s<i&~~<V~$ã.o
ól--"P~ ~(U/q~~ól-'
~~nã&~\~~-
~ _qt.U!I~~~~~
~ se, -nã&~oi,
~~~ ~q~~i.anll~
~~C0114t°YUÇÕEWl&nâo--{(me,
. . . ~t'yolc-Lá;c.ólccadc: ..
_ ~~~p~em.,cultwar
~~ \l~qae,, por menor
~ q~~Q./, ~~ar~~~
~ores <V frtA:'c,fi-ca,-.

' !
,
•
Dedico este trabalho
a meu pai, Heitor Gonçalves Coélho, porque . f0i mais do que um pai para mim, me
incentivando a caminhar sempre à frente e a seguir seu exemplo
à minha mãe Eunice Diniz Coêlho, "in memoriamn por ter sido um exemplo
incomparável de máe e ter me doutrinado da , maneira que o fez
a meu irmão Thiago Diniz Gonçalves Coêlho. por ter me incentivado a enxergar o caminho
da ciência
à Iara Bezerra Rodrigues Coelho por ter me incenUvado a ter paciência
à minha amada esposa Francine Alves-da Silva Coélho, por ter me apoiado de todas as
maneiras possíveis, sendo minha fiel companheira de todos os momentos e ter me
ajudado em tantas ocasíôes, durante a execução do mestrado

,
. )
/
\
'-
• 1 Trabalho realizado no Laboratório de Parasitologia da . Universidade de Taubaté e na Seção de
Ent~roparasitoses _do Serviço de Parasitologia da Divisão de-Biologia Médica.do Instituto Adolfo Lutz de
São Paulo, SP.
, Apoio Financeiro: ·Fundação de Amparo a Pesquisa dó Estado de São· .
Paulo (F APESP).

AGRADECIMENTOS
À . Prof- Dr2 Herminia Yohko Kanamura, por ter se disposto.a me orientar em um difícil momento do Mestrado e ter compartilhado dos seus conhecimentos e experiência.de vida; ·
À Prof- Drª- )\na. Júlia Urias dos ·santos pela amizade .e apreço que sei que tem por mirn, por ter praticamente me co-orientado durante_ todo este· período e pelo inquestionável apoio científico, emocional e profissional;
Ao professor Heitor Gonçalves Coelho, por ter me apoiado e incentivado desde o início do Mestrado; · · ·
Á bióloga Francine Alves da Silva Coêlho, por ·todo o seu apoio fundamental .no decorrer de todas as etapas do Mestrado; .
· Ao Prof. Dr. Pedro Luís da Silva Pinto, pelas ~µgestões apresentadas no exame de qualificação e por ter compartilhado dos seus conhecimentos teóricos e práticos sobre vários aspectos que foram abordados nos experimentos . que ~~; .
À Prof- Drª- Mana Helena de Arruda Leme, pelo auxílio na realização do~ testes estàtísticos;
À Prof- Drª- Irene da Sil~a Soares pelas sugestões apresentadas no exame de qualificação; ~ ·
À Prof- Drª- Raquel dos Anjos Fazioli, pela paciência e auxílio na realização de algumas etapas. do projeto; . ' .
À Prof! Drª- E!izabeth Na~I de. Gaspari, por ter indiretamente me ajudado a encontrar o caminho certo para minha realização acadêmica, posto que pude
/
passar a desfrutar do prazer de · estudar · . Parasitologia, em particular - . Cryptosporídium, parvum; ·
Ao Mestre José Márcio Cardoso, pela grande assistência quando da· -obtenção do tão. esperado bezerro infectado par~ isolamento do inóculo inicial - o começo de tudo; ·
Aos funcionários da Secretaria de Pós Graduação da F acuidade de Ciências Farmacêuticas da Universidade de São Paulo, Jorge Alves Lima e Elaine Midori Ychico; por todo o auxílio e apoio prestados no decorrer do mestrado;
Ao meu amigo Otávio Ricardo de Oliveira, pelo incentivo constante e compartilhamento da indignação, como o pão de cada dia;
Aos meus colegas d~ Pós-graduação: Angélica, Sílvio, Edward e Claudinho, por terem compartilhado experiências e conhecimentos durante todo este período;
/

' Aos estagiários, alunos de pós-graduação ·e funcionáríos (;ias seções de
Imunologia (Teresinha, Ana Patrícia, Lígia, Elza e Aline) e Parasitologia do Instituto Adolfo Lutz (lvete, Jefferson, Otávio e Fá_bio) pelo constante incentivo;
Aos estagiários do Laboratório de Parasitologia da UNITAU, em especial à Priscila Figueira Miranda, Wilsa Renata Soares. Eliane de Carvalho Lopes e Juliana Guimarães_ Cardoso pelo auxílio prestados na realização de alguns experimentos;
Aos funcionários da UNITAU que me incentivaram a-seguir em frente na realização desse mestrado e a todos os técnicos, funcionários, alunos, estagiários, enfim, · a todas as pessoas que direta ou indiretamente me ajudaram na realização · d~e trabalho; · · · · ·
\ ·
../

Lista de abreviaturas
Lista de Tabelas e Figu-ras ,
Resumo
Abstract
ÍNDICE
11
IV
V
, . 1. INTRODUÇÃO . 01
01
02
03
03
. . · 1 .1. Aspectos gerais da criptosporidiose
' .
:1.2. Ciclo biológico de Cryptosporídíum parvum·
1.3. Aspectos clínicos da criptosporidiose .
1.4. Aspectos epidemiolé>9icos da criptosporidiose
1.5. Tratamento da criptosporidíose 05 \. \
1.6. Resposta imune ao Cryptosporídíum 06
·1.6.1. Participação dos linfócitos TCD4+ na resposta imune a Cryptosporidium spp
~I~~ ITT / . 1.6.2. Participação de outras citocinas na resposta imune a Ciyptosporidium 08
1. 7. Módelos experimentais 11 . '
1. 7.1. Cultivó"in vitro" 11
1.7.2. Modelos "in vivo" 12
1:7.2.1. Modelo bovino: bezerros recém-nascidos 12
1.7.2.2. Modeto·primata 12
1.7 .2.3. Modelo suíno 13
1.7.2.4. Modelo murino .13
1.8. Modelo murino imunossuprimido com gliCÓCOrticóides 15
2. JUSTIFICA TNA 19
3. OBJETIVOS 20 r
4. MÀTERIAL E MÉTODOS
. 4.1. lmunossupressão dos camundongos /
21
21

r .
4.1.1. Avaliação da imunossupressão
~.1.2. Manutenção de camundongos imunossuprimidos \
4 .2. Obtençã9 de Cryptosporidium parvum a partir de bezerro
4.2.1. Purificação de oocistos e preparação dÓ ínocuk> para infecção . . .
dos camundongos
4.3. Infecção de camundongos e coleta dos oocistos
4.3.1. Acompanhamento da infecção dos camundongos
4 .3.2. Recuperação de oocist9s das ·fezes dos camundongos infectados ·-4.3.3. Quantificação dos oocistos de C. parvum recuperados âas fezes
dos camundongos infectados . .
4.3.4. ManutençãQ da cepa de C: parvum isolada
4.4. Análise estatística ).
22
23
23
i4 24
26 \
26
27 .
27-'
28
5. RESULTADOS 29
5.1. Avaliação da imunossupressão dos camundongos 29 .
5.2. Quantificação dos oocistos recuperados de camundongos infectados 35 '
5.3. Manutenção da cepa de C. parvum em camundongo 38
6. DISCUSSÃO /
·40
7 . CONCl,.USÕES 44
8. REFERÊNCIAS BIBLIOGRÁFICAS 45
ANEXOS '· 58
,/

LISTA DE ABREVIATURAS
' -AIDS· - Acquired· lmmunodefieiency -5yndrome
· HIV - Human ··lmmunodeficiency--Virus
-·tFN-v·...:. interferon ~
·IL .. :: interreucina
·1EL ..:. linfócitos intra epiteliais
IClf - ·receptor de célula, , TNF-a - fâtor de .necrose tumoral alpha
-células NK -células Natural Ki1ler SN· - Simians -tmmunodeficiency Virus
A:I. :_ Antes da imunossupressão
VA - Valor Absoluto
VR - Valor Relativo
rn_g - miligrama
. ml - . mililitr:o
· -~ - microlitro
· · M ..; Molaridade
,'
1

. ,
n USTADE TABELAS.E.FIGURAS ,
··Figura ·1. -Número ·-.de · leucócitos/,mm3 ·.·de ·--sangue · de · camundongos,
·expres~~- ·em ·medianas:· ·Grupo ·A ·- 20 ·camundongos ---BAtB/c
imunossuprimídos com -1s>mg de dexametasona; ·Grupo · s - -10 1 . ,
camundongos· BALB/c imu~ssuprimídos com U,"5mg de dexametasona e
·e - .10 camundongos ~C57BU6 imunossuprimidos com· -o:smg de
dexametasona 30 . ,.,
Tabela ·1. · Resultados · do -·teucograma · do --sangue · periférico · de 20 . ' '. (
-ca-mundongos ··BAl::.B/c· fêmeas (grupo A) · submetidas· à:·imanossupressão •
com dose diária de -1 mG de· dexametasona, antes (A.I:) e após · a
primeira, segunda e terceira semana da imunossupressão
I •
Tabela · -2. . Resultados .do . leucograma do .sangue .. periférico ·.de .W
-camundongos-BALB/c -fê~eas -(grupo-B) submetidas -à-imunossupressão
com dose ·diária ·de ·0,5 mG' ·de ·de~me~sona, -antes ·{A.I:) -e -após -a
primeira,' segunda e terceira- semanada imunossupressão- . 33
1abela '"3 . . Resultados' ·de ieucograma do sangue pe'riférico de ·1u 1
' ' camundongos C57BU6 machos .(grupo C) submetidos ·à imunossupressão
.. com .dose .diária .de .0.,5 .mG .de .dexametasona, .antes .(A.l..) .e .após .a
. pr:imeira:e segunda semana .da .imunossupressão .34
-Figura 2. · Número ·totaJ ·de ·ooeistos, -expressos ·em ·média -aritmética, 1
recuperados a partir das ··fezes de camundongos ·C57BL16
· imunoss~primidos com dose 'diária de 0;5m__g de dexametasona _(grupo 3),
até ·o 1712. dia da infec:ção 35
,' Quadro .1. ·-Resumo .dos .procedimentos .de .imunossupressão .e .infecção ·
-realizados-e:do dia-de-ébito:dos animais ' 36
· ,

Ill
Tabela 4 . . Número .de .oocístos .de .e . . parvum .recuperados .das .fezes .de . '
.camundongos .05.78L/6 .imunossuprimidos .com .dose .diária de .0,5 .mg .de • 1
. dexametasona,. do -12 ao 2~ dia-do. experimento · 3-7
Figura 3. Número total de oocistos inoculados e número total de oocistos
recuperadÓs do grupo 3 (10 camundongos C57BU6 imunossuprimidos ,_.
com 0,5mg de dexametasona e inoculados com -2x104 oocistos de I
. çryp_tp~P,f>_rf.Pf'!mp~r.v,u_,m 38
. Figur:a. 4. Nú~ro, total, qe ooçistos inoculados _:e núm_ero .total ~e oocistos
. recuperados .do grupo 11 (-5 camundongos , C57BU6 imunossuprimidos
coi:n 0,5mg de dexametasona e inoculados com 2x104 oocistos de
-.-Cryptosporidíum parvum récuperados dos camundongos do grupo·3) · -39
'

IV
RESUMO
Estudou-se no presente trabalho a susceptibilidad~ de camundongos das I
linhagens C57BU6 e BALB/c à infecção por . Cryptosporidíum parvum, com o
intuito de se estabelecer mode~o animal para obtenção de massa de oocist~.
Para isto os_camundongos foram submetidos.a procedimento de imunossupressão·
com o corticosteróide dex~metasona em diferentes doses, pela via subcutânea e,
após estabelecida a imunossupressão, · infectados com 2x104 oocistos de C.
parvum pela via intragástríc.a. Apenas os camundongos da linhagem C57BL/6, que
'foram imunossuprimidos 'com 0,5mg de dexametasona por, animal, liberaram uma . .
apreciávef quantidade de oocistos nas fezes, sendo deste modo considerados . . \ .,.-'
como um modelo 'si!llples e prático para ampfificação deste parasito .
. \

V
ABSTRACT
" BALB/c and C57BU6N mice were evaluated for susceptibilíty to
Cryptosporidium parvum infection wrth the purpose of establishing an animal._!nodel
for obtaining large amount Qf oocysts. For this, mice were imunossupressec:l by
subcutaneous application, witt1 different doses of the corticosterrnd
dexamethasone, and after establishfJ1ent of the imunossupression, they were
inocutated, by intra-gastric route, with 2x104 C. parvum oocysts. Only -C57BUS
mice, which w,ere imunossupressed wíth 0;5 mg of dexamethasone, relej:ised a ' .
substantial amount of oocysts in teces, showing that this can constitute .. a ~imple
and feasible model for amplification of this parasite.
. •' . .
\
. . .\
. \ ·
I
'\


\ l
1. INTRODUÇÃO
1.1. As~os gerais da criptosPQ__ridiose
I
Em 1907, Tnzer fez a. primeira referência ~o. gênero· Cryptosporidíum para
um -~protozoário parasito que comumente observava nas glândulas gástricas de
camundongos. , Em 1912, o mesmo . pesquisador _sugeriu uma nova espécie,
Cryptosporidium ~rvum, para u~. organismó semelhante,que passou a observ,ar
. no intestino de camundongos. Este protozoário parecia ser raro; permanecendo
. sem importância médico-veterinária por cerca de 40 anos, até que foi ' . .
responsábiliz~do por surtos de diarréias em beierros e, com o advento da AIDS, • e
reconhecido ~mo importante patógeno oportunista (SLAVI~, 1955; _PANCIERA et
ai., 1971; PETERSEN, 1992)_
Cryptosporidii.Jm spp são protozoários coccideos que infectam as células . . . . \ .
epiteliais dos ~atos digestivo-e respiratório de ur.na grande variedade .de animais \ . . .
vertebrados, sendo · . par«1sitos' intracelulares obrigatórios. Várias espécies '
morfologicamente ~~milar:es f9ram de~ita~ e riorneadas segundo o hospedeiro
em que foram encontradas, no entant~ pàra se identificar e nomear espécies, faz-. . . ,.
1 se necessária uma combinação de métodos_ morfológicos, biológicos e genéticos
(ZU et ai., 1992; FAYER et ~/., 2000; EGYEQ et a/.;'2003).
Com rela~o a e. pa_rvum, aná_lises genotipicas de isolados,'-de humanos e,
de animais, revel~ram a existência de dois diferentes subgrupos genéticos ' ' '
(AWAD-EkKARIEM et ai., 1995; WIDME_R et ai., · 1998). Este·. fato foi . ) . . ' .
primeiramente comprovado por PEN~· et ai. (1997) que, ao estudarem 39 isolados
de e. parvum de· humanos e ' bovinos, demonstraram a existência de um
poi;morfismo genético, pela análise moieculàr . de ~ma região. de 369 pares de
base do gene que · codifica para uma proteína de adesão relacionada a • I
tromoospondina (TRAP-C2), definindo deste modo dois genótipos distintos: o . . genótipo 1, e_ncontrado exclusiv~me11te em infecções humanas, e o genótipo 2,
presente tanto em hospedeiros humanos quanto em animais. Ao realizarem testes
de infeçção experime'ntal, os autores observaram que os isolados do genótipo -1
não foram capazes rde infectar camundongos recém nascidos das linhagens

··/
· 2
BALB/c 1e SCID ou bezerros neonatos, ao_contrário dos·isolados do genótipo 2; · 1 - •
1devido a diferençàs genotipicas, fenotfpicas, epidemiológicas e patqgênicas entre . ) . esses dois genótipós, MORGAN et ai. (2002) propuseram a denominação_
Cryptosporidium hominis ao genótipo 1, ~nsiderando-o assim uma nova espécie ..
Revisões bibliográficas recentes réconhecem 13 espécies, a saber_: . C.
andei'soni, C.baiteyi, e. cannis, C. felis, . e. galli, e. homfnis,· e. meleagridis, e. ' ,. . .
mo/nari, C. muris, C. parvum, C. saurophilum, C. serpentis e e. wrairi, previamente
diferenciadas com o uso de critérios in~rfoÍógicos, moleculares e especificida<;fe de
hospedeiros (MONIS & THOMPSON, 2003; XIAO et ai., 2004). I
1.2. Ciéto biológico de Cryptosporidíum parvum '
. \ .
Nos mamíferos, quando oocistos de Cryptosporidíum-spp , são ingeridos, a
excistação · ocorre no intestino delgado coi;n liberação de quatro esporozoítos que ·
penetram as ' vilosidades dos enterócitos, e se desenvolvem no vacúolo ' ' . t
citoplas!Jlático; um compartimento extracitoplasmático que permite que o parasito . ..
se localize numa ·região intracelular. e_ extracitoplasmática: · No vacúolo,, os
· ..esporozoít95 se desenvolvem em · trÓfozóítos e ~ste~ origi~am o meronte tipo 1,
que são -formas com seis a oito, núcleos, que por, sua vez produzem seis a oito
merozoí~~s que invadem as células epite~iais adjacentes . e se de~nvolvem em
novos merontes tipo : 1, que são ~ma fonte. interna de auto-infecção com
. ampli~caÇão do parasitç. Uma população de merozoítos origina o merpnte tipo· li
que se dese~volve _· em microgamonte' ou macrogamonte com liberação dos
microgametas e . macrogametas. A . re~rodução sexuada inicia-se quando
microgametas maduros se fundem com macrogametas, · OriQinando · após
fertilização bo zigoto que ~e se desenvolver em dua~ populações de oocistos:
os de parede delgada (aproximadamente_ 2Ó% dos oocistos formados), que são
uma -segunda fonte .de' auto-infecção 1ihterna, ou oocistos de parede espessa .
{aproximadam~nte 80% dos oocistos formados), que podem ser excretados no
meio ambiente (KO_SEC et ai., 2001 ).

. 3 .
1.3. Aspectos clínicós da criptosporidiose
. Os sint?rnas clínicos da criptosporidiose são amplamente dependentes do
hospedeiro. Três populações de hospedeiros têm sid9 desc~s: indivíduos em ,-·
surtos de áreas"industrializadas, crianças de áreas tropicais em dese~volvirnento e·
pacientes irçiunocomprometidos. Dados de surtos nos Estados Unidos descrevem
um · período de latência 'de . uma semana após infecção e · uma doença . .
caracterizada por_ diarréia aquosa, ocasionalmente com dores abdominais,
. náuse~s. vômito, perda de peso ou febre moderada, podendo durar até nove dias.
Este mesmo quadro clínico é observado em crianças com criptosporidiose nas
áreas . em d~nvolvimento. Já em pacientes imunoco.mprometidos, a
criptosporidiose pode se manifestar de quatro maneiras: a) infecção·autolimitada .,
com dores abdominais, náuseas, . vômito, perda de peso ou febre moderada; b) .
síndrome da desidrataçao diarréica aguda, com 20 ou mais evacuações diarréicas
por dja; c) _síndrome da diarréia crônica e d) diarréia com envolvimento sintomático
dos ,.duetos biliares e pancreáticos (TAGHI-KILANI et ai., 1990; MORGAN et ai., .
1995; LAURENT etal. , 1997; FRANZEN & MULLER; 1999; KOSEC eta/., 2001). 1 ' • ~ • •
' 1
. . . 1.4. As~os epidemiológicos da criptosporidiose
" Apesar do gênero Cryptosporidium ter sido descoberto em 1907, a maioria. . . . ' ' ·- das informações sobre sua biologia, infecções em humanos e epidemiologia foi 1
acurri~lada apenas na última década. Nesse período, qryptosporidium"'parvum
passou a· ser reconhecido como uma ·causa comum de diarréia tanto em humar:ios f • • ' - j " '
como em outros animais (TZ_IPORI & WARD, 2002b; PENG" et ai.;· 2003).
Fatores determinantes da epidemiologia e da ocorrência de infecções ·por
Cryptosporidium parvuf"(I. relacionam-se ao seu pequeno tamanho, que d_ificulta o
seu diagnóstico, à baixa .dose infectante, à resistência aos procedimentos de .
cloretação utilizados no. tra~mento convencional de água e ao potencial zoonótico
(KOS~C et ai., 2001).
A transmissão da criptosporidiose pode ocorrer ~r contato direto entre 1
humanos e destes com animais infectados e por consumo de água potável ou

4 • • 1 _ I
contato com água recreacionaf contaminada; no entanto, a transmissão também
pode se dar pelo consumo de alimentos contaminé;ldos e possivelmente pelo ar,
sendo considerados. grupos de risco: c::rianças, pessoas mal-nutridas e indivíduos_
imtmocomprometidos, ihciuii:tdo pacientes com AIDS (AcquÍred lm~unodeficiency ' .
Syndrome), transplantados, pacientes -submetidos à quimioterapia ·para câncer, ' • I
pacientes institucionalizados · e . pacientes · com doenças infecciosas
imúnossupressoras (AWAD-EL-KARIEM et ai., 1995; FAYER et ai., 2000).
Em 1976, os primeiros . dois ~casos ~e criptÓsporidiose hum~na foram
rel~~dos por dois grup~s:· indepe~dentes e ~m 1981 , foi rel_atado o primeiro caso
de criptosporidiose em paciente com AIDS, (FRANZEN & MULLER, 1999). Um ano
depois a epidemia de AIDS deu à criptosporidióse humana um 'novo significado,
quando, nos El)A, o CDC (Centers for°Disease Contrai and Prevention do Ncltional • . 1 ' ' ' '
Center for lnfectious Disea_ses) relatou que de ~m total de 21 r;>acientes com Aios,
_ 14 desenvolveram um quadro diarréico fulminante e evoluíram ao óbito
(PETERSEN, 1992).
Desde então, úm grande número de pesquisadores vem investigando a
prevalência e epidemiologia dessa · infecção em pacientes com AIDS,
. apresentando resultados estimativos que djferem marcadamente de acordo com a
populaçã~ estudada, com uma freqüência média- de 32%; porém sabe-se que
pacientes · com imunod_epr~o mais severa têm uma. maior predisposição a
adqui_rir cript9spo~idiose (HUNTER & NICHOLS, 2002).
O primeiro surto de· infecção por parasito . do gênero Cryptosporidium,
identificado na · época como · C. parvum, , através de métodos sorológico~ e . 1 ' . , • .
parasitológicos, se deu no verão de 1984 _em Braun -Station, um subúrbio com . / ' . -
cerca. de 5900 pessoas a 32 Km de Santo Antônio,· Te.xas. Porém, o surto de , , . . . . , . . r
maior repercussão ocorreu em 1993 na cidade de Milwaukee, W!_sconsin, Estados ' '
Unidos, no q~al 403.000 pesso~s, de um total de 1:610.000! desenvolveram
criptosporidiose devído ao consumo de, água contaminada do reservatório da
cidade (ERÁNZE~ & MULLER, 1999; DILLINGHAM et ai. , 2002).
Em estudos conduzidos em países em desenvolvimento como, por exemplo, ( . . . . .
Nigéria, Méx~. Peru, Guiné-Bissau e Uganda, foi demonstrada a importância de
parasitos do gênero Cryptosporidium como freqüente causador de diarréia,
\
( ,_

relacionando a elevada ocorrência a fatores clínicos, ambientais, higiênicos e
nutricionais (OKAFOR & OKUNJI, 1996; ENRIQUEZ, et ai., 1997; CHECKLEY et
ai., 1997; PERCH etal., 2001;.TUMWINE etal., 2003).
HOJL YING et ai. (1986) r~alizaram um estudo com 374 crianças !iberianas, . .
com idades de 6 a . 59 meses, com o intuito de · investigar o papel de
Cryptosporidium spp como agente .etiológico de diarréia, e verificaram uma \
ocorrência de 8,4% em crianças com diarréia no ambiente doméstico e 14,6% em
crianças hospitalizadas; a aglomeração populacional e a alimentação de recém- • \
nascidos. com leite não materno for~m considerados os principais fatores de risco
para contrair criptosporidiose nessa comunidade.
Em estudo epidemiológico reali~do em um . hospital próximo a ·cidade de \
Jerusalém; Israel, SALLON et ai. (1988), ao realizarem ~xame parasitológico de_ 1 .,. ' '
fe~es ·,de 221 crianças com diarréia, demon.strararil a presenp de oocistos de
CryptoSporidium spp eni 13% das amostras analisadas; a maioria das crianças • 1
com criptosporidiose eram significativamente mais desnutrjdas do que as crianças . . ,
que. não liberavam oócistÓs nas ·fezes. Sendo assim, os autores conduíram que, . ' . .
nos países em desenvolvimento, a elevada prevalência de criptosJ>?ridiose em .
crianças com diarréia estaria associada com a desnutrição.
No Brasil, Mangini et ai. (1992) demonstraram uma incidência de 17,43% de
criptosporidiose em . crianças de o à ~ anos de idade com quadró de diarréia e . . ' . \
internadas no Hospital das Clínicas em São Paulo. Surtos de criptosporidiose
também foram ·observados em outros estados do Brasil, com incidências variando . .
d.e 72%, em criança~ çom diarréia, na cidade de_ Fo~leza - Ceará (Agnew et ai.,
1998), até ·1,1% em crianças, com men~s. de 5 anos de _idade, na cidade de
Càmpo Grande - Mato Grosso do Suf' {Oshiro et ai., 2000).
1.5 .. Tratamento da criptosporidiose
, I 1
A falta · de tra~mento efetivo na infecção causada por _parasitas do gênero
Cryptosporidum freqüentemente contribui para a morte de pacientes com AIDS ou • \ ' 1 •
com imunodeficiência"s de outras etiologias (WOODS et ai., 1996). Observa-se -

. \
6
pouco a.vanço n~ste sentidd, em parte devido à. falta de um modelo de. infecção · in
' vivo" e ·in v.itró" bem definido (BJORNEBY et ai., 1991; MEAD, 2002).
Têm-se estudado vários esquemas de terapia para criptosporidiose ta.is '
como: imunoterapia com anticorpos policlonais ou monoclonais (ARROWOOD et /
ai., 1989; DOYLE ef ai., 19~3; RIGGS et ai., 2002), terapia com agentes . 1
-antimicrobianos (HEA~EY et a,I., 1995; WOODS _ et ai., 1996, BLAGBURN et al, . '
1998), uso de microorganismos da m~croflora intestinal {WATERS et ai., 199~). e
terapia com colostro imune bovino (PERRYMAN et ai., 1999), algumas delas se
moslrando · eficazes no controle <:ia criptosporidiose, mas não no estabelecimento
da cura definiüva.
, O uso de · terapia anti-retroviral tem resultado em um decréscimo de
infecções oportunistas em pacientes com AJDS nos últimos anos; IVES et ,1. . (2001)-demoostraràm qÚe a incidência de criptosporidiose diminuiu cerca de 60%
. '
em pacientes inf~ados pelo HIV (Human lmmunodeficiency Virus) durante o uso
.. dos coquet~is de drogas anti-retrovirais. No entanto, seg~ndo MEAD (2002), não
se sabe ao certo até que ponto este tratamento será ·· efetiv?, devido a
P,9S5ibilid~de . de · recombinação virai, o que anularia o efeito da . terapia anti-.. retroviral, resultando· numa maior pré-d_isposição dos pacientes às infecções
oportuni$tas.
1 ~6. Resposta imune ao Cryptospondium
Tanto em estudos realizados em humanos.quanto em estudos com modelos
experimentais é re~ltada a importância da resposta imune humoral e celular .. . , . -
para atenuar ou resolver .ª infecção . causada_ por Cryptosporidium parvum .
. Atualmente existe ~rto :cons(!nso de que os dois component~ fundamentais para
preyenção ou ·resoluç:ãq da criptosporidiose são a dtocina interferon gamma (IFN
y) e os linfócitos T CD4+ (HAYWARO·~t ai. , 2000; HUNTER & NIÇHOLS, 2002; . ~ , -
.LACR.ÓIX-LAMANDÉ, 2002).
1.6.1. , Participação dos linfócitos T CD4+ na resposta· imune à
Cryptosporidium spp, via IF N--y _ -

7 1 . ,
BLANSHARD et ai. (1992), ao analisarem a contagem de linfócitos T ·c04+
em ~cientes com -1
AIDS e cciptosporidiose, dem~rí~~~m qÜe~ só ~ -pacien~
· com contagem -de linfócitos TCD4+ inferior a 50 célutas/mm3 de sangue
apr~sentar~m doença fulminante; segundo CHEN ·e~ ai. (1993) esta pequena
quantidade de linfócitos T CD4+ provavelmente leva a uma diminuição na . .~ .
hábilidade destes pacientes de resistirem ou se curarem de uma infecção por \ ( . -
Cryptosporidium spp. Da rnes~ mâneira, estudos com camundongos comprovam
a hipótese · de que ··os linfócitos T CD4+ são de g·rande · importância no
estabelecimento de resistência a crip~osporidíose neste modelo experimental
(B~NSHARO et ~/.,.1992; HAYWARD et ai., 2000; LAURENT et ai., 2002).
· Para delinear ~ :1importância das células T CD4+ e da citocina- !FN-y na ' .
· imunidade protetora em camundongos, UNGAR et ai. (1986) iniciaram uma série < -
de experimentos nos quais anticorpos monodonais (Mab) anti-CD4 e anti-lFN-y
foram administrados a camundongos BALB/c recém-nàscidos e . imunocompetentes infectados co~ C. pàrvum. Neste. estudo demonstrou-se que a
co-administração d~ Mab anti-CD4+ e ariti-lFN-y resultaram numa infecção crônica
por C. parvum, corn .grande número de oocistos liberados nas fezes. A remoção ' . '
· do Mab anti-lFN-y em qualquer ponto do experimento levou a redução do número
de oocistos liberados. Por outro làdo, para que se mantivesse uma liberação
crônica de oocistos houve a necessidade de se manter o tratamento com Mab anti-CD4+. Parti.ndo destes resultados os . ·autores concluíram ·qoe IFN-y limita a . '
' " severi<jade da inJecção. mas não é ·-responsável .pêla resolução final, sugerindo
\ . haver outros mecanismos dependentes das células T C04+ na cura definitiva da
. J
criptosporidíose. ·
AGUIRRE et ai. (1994) ao analisarem a susceptibilipade de camúndongos . deficientes de moléculas MHC-classe I e MHC-classe li, .demonstraram qu~ só os
camundongos de~cíentes de MHC-classe li são susceptív~s à -infecção por é. _, parvum, já que desenvolveram infecção crônica · pelo parasito. Estes camundongos
possqiam quantidades pe linfócitos B e linfócitos T coa+ normais, e a_
ctiptosporidiose persistente observada foi atribuída a deficiência d~ linfootos T
CD4+ funcionais no ·tim9, baço e Iinfonodos dos anímais . . --.

8
Co~ o intuito de determinar a' competência de camundongos de se curarem
de criµtosporidiose na total ausência de IFN-y, THEODOS et ai. (1997) realizaram
estudo ~ülizando _camundongos da linhagem C57BU6, com uma disfunção ·no
gene do IFN-y (camundongos nocauteados de IFN-y). Neste estudo também
· foram analisados camundongos C57BU6 com urría neutralização temporária da
·atividade do IFN-y, obtida pelo uso de anticorpos anti-lFN- y. Esses pesquisadores
demonstraram , que, enquanto a neutralização temporária da atividade . do IFN-v
induzju uma _ criptesporidiose apenas "temporária, na sua completa ausêncià os
camundongos não foram capazes de se curar..
MEAO & YOU ·(1998) demo.nstr-aram haver uma. marcante diferença de
susceptibilidade entre as linhagens de ~mundongos C57BU6 e -BALB/c, quando / \
nocauteados de iFN-y. Ao inocularem camundongos adultos .(com a a 10 semanas
de idade), fêmeas, das· duas linhagens, com _ 105 oocistos de C. parvum
demonstraram que a in!ensidade âe infecção nos camundongos_C57BU6 foi bem / '
maior do que nos camundongos BALB/c. Enquan~ os camundongos da primeira
linhagem liberaram. uma grand~ quantidade de oocistos. nas fezes, que auméntou
marcan~emente no quarto dia e contin~ou a aumentar nos dias consecutivos, os , ' 1
camundongos da 'linhagem BALB/c desenvolveram uma infecção moderada, com \ - - -
liberação de oocistos 100 vezes menor que os da outra linhagem, evoluindo para , ' '
cura.
TZIPORI et ai. (2002), ·ao estudare111. a ·infectividade de um isolado de / ' . '
C. parvum obtido de um bezerro de cervo vermelho (Cervus elaphus). observaram •' ' .
que ca'mundongos da linhagem C57BU6 nocauteados de IFN-v, após inoculação
com 300 oocistos, desenvolveram sintomas de criptosporidiose como letargia, , anorexia e reduzido ganho. de peso e liberaram grandes quantidades de oocistos
nas fezes, apesar de não haverem desenvolvido d.iarréia. . .. '
1.6.2. Participação de outras citocinas na resposta imune a Cryptosporidium
Para explicar a acentuada diferença de susceptibilidade à infecção por
e. parvum de camundongos das linhagens C57BU~ ~ BALB/c, nocauteados de

9 .,.
IFN-y, SMITH et ai. _(2000) avaliaram o padrão de liberação de citocinas de célulàs
do baço desses animais, previamen1e infectados com 2x106 oocistos de C.
parvum, após eStífnulação "in vitro" com antígenos de esporozoítos. Os
esplen~itos dos_ camundongos BALB/c produziram -maior quantidade de
interleucinas 12, 4 e 5 (IL-12, IL-4, IL-5) e do fator _de necrose tumoral, e os
camundongos. da linhagem C57BU6 produziram apenas maior quantidáde de IL-5; '
deste modo, os autores concluíram que na ausência ~e IFN-y, a resolução da l I • . . •
. criptosporidiose -é dependente em parte da expressão de citocinas Th2. ,•
Em tontraste ao observado nos camundongos nocauteados de IFN-y, o~
camundongos da linhagem C57Bl16 atimizados são resistentes. à infecção por' C.
parvum, e os ~m~ndongos da iinhagem BALB/c são susceptíveis (ADJEI et ai.,
1997). Com o intuito de esclarec~r a diferença d~ susceptibilidade das duas
linhagens de camundongos atimizados, ADJEI et ai. (2000) inocularam ' . -..._
camundongos fêmeas, adultas, com 106 oocistos de C. parvum e analisaram a
porcentagem de linfócitos T CD4+, CD8+, a.~+ e yô+ do baço e do epitélio - ' , - ' intestinal. Esses pesqui~dores observaram que não houve diferença entre as
linhagens, com relação- aos linfócitos do baço, · no entanto, com relação aos . . . '
linfócitos intra-epiteliais_ {IEL), os camundongos da linhagem C57Bl16 tiveram_ uma
maiç,r porcentagem de _linfócitos --CD4+, CD8+yô~ e TCRyô+. Sendo assim, os . .
autores -·concluíram que na ausência de resposta imune celular sistêmica, os
linfócit~s_ intra-epiteiiais CD4+, _. CD8+yô e TCRyô+ parecem ter uma importante
função regulatória na resposta imune ao C. parvum, com produção de citocinas do
tipo Th-1 e Th-2.
A impo_rtância do fator de necrose tumoral alpha (TNF-a.) nà resposta imune
ao C. ·parvum, foi. ,analisada ·primeiramente em estudo realizado por' CHEN et ai.
(1993b); neste estudo se observou que a, administração de uma preparação de . '
anticorpos policlonais anti-TNF=a., antes e· durante o experimento de infecção, não
induziu maior susceptibilidade ao C. parvum. ~esultados semelhantes_ fo"ram
observados· por MACDONALD & BRANCOFT (1.994), contudo administrando um
anticorpo monoêlonal que' neutraliza o . TN_F-a. (Mab TN3-1R12). Esses d_ados ' ·•
sugerem que o TNF-a. não é um' ir:r,portahte · mediador na resi~tência inata ao C.
parvum, apesar de ser uma c!tocina capaz de induzir a produção de IFN-y.

10
·.A IL-12 é considerada importante no combate à cHptosporidiose,
principalmente porque ta! componente pode induzir a produção dê tFN-y pelas
células . NK (Natural Killer) e pelos linfócitos T e é um importante mediador de ' \
resistência inata dependente de IFN-y · para um grande número de '
microorganismos, incluindo outros protozoários do , Filo Apicomplexa como
Toxoplasmq_gondíí (HÚNTER etal., 1994; KHAN et ai., 1994). ·
Para verificar a ação da IL-12 como modelador da susceptibilidade de
camundongos imunocompetentes e imunodeprimidos à infecção por e. parvum. , URBAN et ai. (1996) administraram anticorpos policlonais anti IL-12 a
camundongos . BALB/c I recém-na$cidos e camundongos C.817 SCID
(camundongos com imunod.eficiênci~ severa combinad~). antes e após infecção( e
· observara_m .que houve aumento significativo da infecção nas mucosas intestinais
dç1s duas linhag~ns ,,e_studadas. Com esses resu~dos, os pesquisadores
sugeriram que a ·1L-12 _participa da resistência inata ao 'e. parvum tanto em .
Gamundongos imunocompetentes quanto em camundongos imunodeprimidos. · ' ' '
A . capacidade er9.tetora da IL-12 foi confirmada em ~utro experimento
realizado.no mesmo trabalho, no Ql:Jal se administrou ll-12 recombinante nas duas
linhagens de camundongos estudadas, um dia antes da inoculação com oocistos,
demonstrando-se que n~nhum dos camundongos das d_uas linhagens adquiriu
criptospori~iose. Os _ autores concluíram que a cura da criptosporidiose nestes
mopelos experimentais talvez .esteja associada a uma resposta i_mune.do tipo Th2. •,
No_ entanto, AGUIRRE et ai. (19~8) demonstraram que camundongos da
linhagem C57BU6, nocauteados de IL-4, desenvolveram infecçã~ prolongada por
e. parvum, sugerindo qtie a cura da çriptosporidio~ está ligada a resposta imune
dQ tipo .Th-1; contudo, alguns camundongos ·eventualmente se curaram da
infecção com ou sem a presença de IFN-y.
Para determinar o efeito da adição ou · de uma citocina Th-1 ou de uma .
citocina Th-2 na' infecção por C. parvum, , SMITH ·et ai. (2001) infectaram
- camundongos C57BU6 nocaute,ados de IFN-y, com oocistos de C. parvum e
. adminisv,aram IL-12 ou IL-4 recombinantes por via intraperitoneal e, durante o
período da infecção, demonstraram que tais camundongôS não se curaram da . \
ériptosporidiose es~t,elecida; . pelo contr~rio, · apresentaram uma exacerba~o da ' ' 1 ' -· À

11
doença. Com estes -resultados os pesquisadores concluíram que a resistência e
recuperação de infecções causadas por C. parvum dependem de um balanço - /
refinado na quantidade e sincronizáção de citocinas Th1 e Th2.
1. 7. Modelos experimentais
Para estudo dos aspectos· bioquí(!liCOs, imunológicos e da biologia celular e . .
molecular de qualquer microorganismo, é essencial que se obtenha um grande ,.... . . .
estoque do m~smo e no caso do C. parvum, alguns fatores precisam ser melhor
estudados tais como: o estabelecimentq de. uma. fonte de. oocistos de fácil
obten~o; a padronização de métodos reprodutíveis de purificação de oocistos e a
otimização das condições- de crescimento "in vitro" (MORGAN et ai., 19.95;
MELONI & THOMPSON, 1996).
' 1. 7 .1. Cultivo ªin vitro·
No. que d~ res~ito ª? cultivo de .e. parvum "in vitro·, vários· pesquisadores
(FLANI.GAN et al.1
1991; GUT et ·a1. , 1991·; HEALEY et ai., 1993; UPTON et ai.,
1994; UPTON et ai., 1995; LAWTON et ai., 1997_; DENG & -CLIVER, 1998) -· • < • ..
tentaram produzir infecções em monocamadas de células com este parasito, tanto . .
com, isolados humanos como de bezerro, observando-se resultados pouco • • - • i •
satisfatórios com as várias linhagens celulares, entre elas. MDBK. MDCK, caco-2
,eHCT-8.
De' acordo com WIDMER et ai. (2000) a falha em perpetuar a infecção ·in
vitro" é atribuída à apoptose, que em· diferentes sistemas de cultura celular, afeta _a
maioria das células infectadas, sendo um fenômeno responsável por uma drástica - .
redução no número ~e parasitas in~celula~es ..
Apesar dessas dificuldades, HIJAWI et ai. (2001) descreveram o : . , .,
desenvolvimento completo e manutenção em longo prazo de C. parvum "in vitro·
em cultura de células -da linhagem HCT-8. O ciclo completo do parasito foi mantido
durante 25 . dias, por subcultivo; : todavia, apesar dos resultados promissores '
é!Presentados, a pouca reprodutibilidade da técnica utilizada e_ o alto investimento
- BIBLIOTECA Faculdade de Ciências Fa,mac~ t· , 1cas
Universidade de Sào Pauto· •

12
necessário para manutenção de culturas celulares constituem séria limitação para
a implantação desta metodologia na rotina.
1.7 .2 . ~odeios "in vivo"
Para es~belecimento de uma fo~te · de oocistos, ~e Cryptosporidium parvum,
. pesquisas têm sido conduzidas inicialmente com algumas espécies de mamíferos
como primatás, suínos ·e camundongos, infectados experimentalmente com
· oocistos obtidos de bezerros naturalmente· infectados,· no entanto a maioria das
espécies de mamíferos)á ~studadas adquire resistência natural ao C. parv_u_r;n, nas
semanas iniciais de vida (SHERWOOD et ai., 1982).
1.7.2.1. Modelo bovino: bezerros recém-nascidos
,,
Para se ,obter parasitos em massa . em condições experimentais, vários
pesquisadores infectam bezerr:os recém-;-nascidos, utilizando como fonte de
' inóculo, oocistos isolados de bezerros e cordeiros naturalmente infect~dos. Os . '
bezerros são infectados imediatamente após o. nascimento, preferencialmente - . ' .
. antes de terem · sido alimentados com colostro. Estes devem ser alojados em
completo isolamento a fim de se ~vitar a exposição a outros patógenos, incluindo
Cryptosporidium spp de outras fontes, bem como para impedir contaminação do
meio (MELONI & THOMPSON, 1996; BAKER et ai. , 1998). 1
Vale salientar que esse , modelo animal requer recursos de instalação e
supervis~o · por pessoas capacitadas-ao atendimento de animais de grand~ porte e
que o risco de infecção para humanos é bastante elevado, em função da grande
quantidade de qocistos liberados· pelo~ bezerros infectados. Exist~rn vários relatos . .
de manipuladores de_ ~zerros e estudantes de veterinária que adquiriram
criptosporidiose pelo contato com bovinos infectados _(BAKER et ai., 1998) .
. 1. 7.2.2. Modelo primata

• 13
O modelo básico que simula muitos dos aspectos da criptosporidiose
observada em humanos com AIDS é o do primata com AIDS; enquanto primatas
imunocompet~ntes desenvolvem diarréia aguda auto-limitada, que pode ser
duradoura ·nos . - _ prima~s jovens, macacos infectados com SIV (Simious ' - '
lmmunodeficiency Vírus) desenvolvem criptosporidiose de prognóstico progressivo . . .
e fatal, envolvendo os tratos ~igestivo, biliar -e respiratório (RIGGS, 1990;
BASKERVILLE et ai., 1991). .
·. Apesar de existirem alguns aspectos da criptosporidiose que só podem ser 1
bem estudados em _primatas, tais como o delineamento dos vários defeitos
imunológicos na mucosa do trato gastrintesfinal, associados à progressão da
infecção pelo SIV, que contribui para a persistência da infecção e ao dano de
mucosa observad...o na criptosporidiose, esse modelo experimental é_ de custo
elevado, de pouca acessibilidade, e outros fatores, incluindo as considerações
éticas, limitam a praticidade 9e se usá-lo (RIGGS, 1990).
r
· 1.7.2.3~ Modelo suíno
Porcos recém-nascidos são altamente susceptíveis · à criptosporidiose,
podendo desenvolver diarréia aquosa, desidratação, · má absorção e freqüentemente, morte súbita (TZIPORI et ai., 1994). Já suínos adultos raramente
. . ....__ . desenvolvem diarréia, mas · pddem excretar oocistos intermitentemente por longos . . períodos de tempo (SCOTT et ~I., 1995).
As limitações -desse modelo incluem o fato de que a susceptibilidade dos
porcos é variável, podendo a criptosporidiose durar curtos períodos de tempo, ter uma longa duração ou resultar em morte súbita .e o fato da manutenção desses
animais ser tão dispendiosa quanto à de outros animais de grande e médi_o porte.
1-.7.2.4. Modelo murino
Diferentes linhagel)s de camundongos têm sido utilizadas para realização de
experimentos com C. parvum, tais como: o estabelecimento de c,riptosporidiose
crônica e obtenção de· massa de oocistos (HEINE et ai., 1984; UNGAR et ai.,

14
1_990; RASMUSSEN . & HEALEY, 1992; PETRY et ai,, 1995; MELONI &
THOMPSON, 1996; YANG et ai., 2000); estudo da-·susceptibilidade de diferentes
linhagens de camundongos à infecção por C. parvum (AGUIRRE et ai. . 1994;
MEAD & YOU, 1998); estudo da viabilidade e infectividade de isolados de C. ~ 1
. ' ' ' '
parvum (AYDIN & ôZKUL, 1996; VE~GARA-CASTIBLANCO et ai., 2000; I •
NEUMANN et ai.; 2000; DELAUNAY et al, 2000; OKHUYSEN et _ai., 2002);
avaJiação de ~gentes qúimioterápicos para combate à cliptosporidiose (HEALEY . .
et ai., 1995; BLAGBURN et ai., 1998) e estudos do mecanismo imune envolvido
na susceptibilidade ou não ao C. -p~rvum·(UNGAR et ai., 1986; B~NSHARD_et
a/., 1992; CHEN et ai.,· 1993b; AGUIRRE et ai., 1994; MACDONALO & . . '
BRANCOFT, 1994; URBAN et.al., -1996; THEOOOS et ai., 1997; AGUIRRÊ et ai., I
1998; ~AKER et ai.; 1998;. HA Y_WARD et ai., 2000; SMITH ~t ai., 2001; LACROIX
LAMANDÉ et ai., 2002; LA~RENT et aL, 2002~-TZIPORI et ai., 2002).
Quanto à obtenção de oocistos em massa, experimentos utilizando
·~m!,Jndongos , recém-nascidos das linhagens '?57BU6, ARC/Swiss, ~ALB/c ' .
demonstrara~m resulta~os s·atisfatórios na indução de infecção por C. pawum
(SHERWOOD et ai:, 1982; PETRY ef ai. , 1995; MELONI e THOMPSON, 1996),
mas dific1.;1ldades de manuseio pelo reduzido tamanho dos animais, baixo número
de oocistos recuper~dos e . auto-limitação da infecção tornam esse modelo pouco
prático para obtenção de· ~stos em massa, embora apropriado para estu~os de
infectividade de cepas de e. parvum (NEUMANN et ai., 2000; VERGARA
CASTIBLANCO etal., 2000).
HEINE et a/., (1984) inocu·larani camundáng~s da linhagem BALB/c, recém -
nascidos e congenitamente atimizados (nude), que são deficientes de 'células T,
com 105 oocistos de C. parvum e, apesar de.não haverem quantificado o número \ . .
de oocisto~ recuperados, estabeleceram infecção persistente em . todos os -\
camundongos utilizados_ no experimento; todavia, falharam em induzir infecção em
camundo9gos BALB/c núde adultos (40 dias).
Com o intuito de estabelecer infecções por C. parvum em camundongos nude
adultos. UNGAR et ai. (1990) inocularam .14 camundongos da 'linhagem BALB/c
com 30 dias de idade, com 107 oocistos e observaram três padrões diferentes de ) , ,
infecção: quatro camundongos morreram no quarto dia após a infecção; três

/
15
desenvolveram um declínio gradual e morreram após quatro. semanas e · três
adquiriram criptosporidiose e· liberaram ?OCistos nas fezes durante 16 semanas.
Os outros quatro camundongos morreram de causas não relacionadas ao C.
paNum. No mesmo trabalho os putores a~ministrar'am anticorpo monoclonal
anti-CD4 a um .outro grupo de camundongos BALB/c imunocoirlpetentes e recém-, , '
I .
nascidos, e, durante o período que durou a imunossupressão, todos os • 1 , .. • •
camundongos do grupo liberaram oocistos nas fezes; dessa forma os autores,
apesar de não haverem quantificado o número de oocistos recuperados nas fezes
dos camundongos, assinalaram a praticidade dos dois modelos estabelecidos, ' '
para obtençao de· o~éistos de C. paivum, porém, os autores ·não· conseguirám • 1 . . ,
estabelecer infecção por C. parvum após administrarem o anticorpo monoclonal
anti-CD4 a camundongos BALB/c imunocompetentes.adultos.
Vários experimentos foram realizados com camundongo~ adultos
geneticàment,e imunodepri~idos, como camundongos SCID (camundongos com
imudeficiêr:1cia co~binada ·severa), camundongos congenitamente atimizados ou
camundongos. nocauteados P8ira determinadas citocinas, contudo, a maioria deles ·, -
direcionados ao estudo de aspectos referentes à resposta imune e à biologia de
C. paNum, não sendo direcionados à obtenção de massa de oocístos.
O uso de linhagens susceptíveis de....._ camundongos parece ser promissor,
principalmente devido à faéilid~de de manuseio d~ste modelo e a possibilidade de.
·se desenvolver ·um quadro clínico · bastante semelhante ao observado na
criptosporidiose humana (YANG et ai..! 2000).
1.7.3. Modelo murino imunossuprimido com glicocorticóides
Já para se obter produção em- massa de oocistos, vários pesquisadores . '
empregaram_ camundongos adultos · da ~inhagem C57BU6, por serem mais
susceptíveis do que camundongos de outras li_nhagens, subr:netidos à terapia c(?m
o corticosteróide dexametasona, em diferentes dosagens e vias de administração • j •
. (RASMUSSEN & HEALEY, 1992; PETRY et ai., 1995; YANG et ai., 2000) .
•

16
O córtex d.a supra-renal sintetiza duas élasse~ de hormônios esteróides, a
saber, os androgên!os. e os corticosteróides. Os corticosteróidés são divididos, de
acordo com-- seu mecanismo de ação, em glicocorticóides, · reguladÓres do
metabolismo de car,boidratos, e · mineralocorticóides, reguladores do equilíbrio .
eletrolítico.
Os efeitos farmacológicos ·dos ~rticosteróides . são amplos, incluindo
alterações no metàbolismo dos carboidratos, lipídios e proteínas, manutenção do
equilíbrio eletrolítico, preservação da função normal do sistema cardiovascular, do
. sistema imunológico,, dos rins, da muscul~tura esquelética, do sistema endócrino e ' . ' . /
do sistem~ nervoso, sendo bem ~nhecida a ação · imunossupressora dos glicocorti~ides.· Os glicocorticóides podem evitar ou suprimir a inflamação em
\ . - - / - .
resposta a vários eventos estimulantes dentre os quais estímulos radiantes, . .
mecamcos, químicos, ·· infeccio59s .. e i'!'unológicos, estando as ~ções_
antiinflamatória e. imunossupressora indissoluvelmente ligadas, já que ambas
resultam, em . sua· maioria, d~ inibição de · funções_ específicas dos leucócitos
(CHROUSOS., . 1995).
Os efeitos imunossupressores dos glicocorticóides estão relacionados com a
indução de linfopenia e 'diminuição da função linfocitária Cóm perda da _capacidade . . _, .
prolíferativà das células frente a mitógenos específicos (PINTO, 1991). Além disso, J ~ - • 1
os glicocorticóides apresentam efeitos s~bré a resposta imunológica específica do
hospedeiro, _pelos efeitos· sobre a produção de citocirias dentre as quais o IFN-y,
fator. estimulador d~ colônia de. granulócitos e monócitos, interteucinas (IL-1 , IL-2, ' • 1 •
IL-3, tl-6) e TNF-a. (GQODMAN & GILMAN, 1996). . ·
. A indução de lir)fopenia foi inicialmente observada por FAUCI & DALE (1974)
ao ad.ministrarem o_ glicbcorticóide h1drocortisona a. humanos normais por via
intraven_osa, verificando · que os valores absolutos de linfócitos e monócitos da
circulação sanguínea diminúem após um período de 4 a 6 !'oras da administração . .
da droga, retom~ndo ao normal após 24 horas, ocasionando uma depleção
seletiva no número de linfócitos. . -.. .,..-
FAUCI (1975) aiQda investigou o efeito do glicocorticóide acetato de cortisona
quando ad~inistrapo em cobaias, demonstrando que esta droga causa profunda,
mas transitória linfoper,ia, . que atingia um pico após 4 horas, retomando a
B I BLIOTECA Faculdade de Ciências Farmacêuticas
Universidade de São Paulo
'

1 •
17
contagens normais em 24 horas. Verificou ainda que havia uma diminuição
proporcional do número de linfócitos T totais, quand9 comparados aos linfócitos·T
_ circulantes e que a -linfopenia sanguínea era resultante da redistribuição ' dos . ,
linfócitos cirpulantes para a medula óssea.
Com relação ao uso de ·glicocórtícóide como droga imunossupressorà, parà - .
posterior. indução de criptosporidiose em modelo murino, RASMUSSEN & v ' \
HEALEY (1992) determi.naram a sus~ptipilidade de camundongos fêm~as,
. adultos, de cinco diferentes linhagens (C57BL/6, C3H/t:ieN, BALB/nAnN, DBA/2N
~ CBA) imunossuprimidos com o glicocortícóide dexametasona, empregando . ' .
· vários regimes de administração da droga. un:1 Qrupq de camundongos adultos {10 . (
por linhagem} recebeu dexametasona na água potável, numa concentração
equi\ralente ~ Sµg/dia, que, segundo REHG et ai. (1988), seria efetiva para
indução de imu_nossupressão em ratos; contudo os autores não observaram
liberação de grande~ quantida_des de oocist0s neste gr.upo. Um segundo grupo de . ! ~
camundongos adultos (20 por linhagem) foi dividid,o em quatro subgrupos e cada
· um_ dos subgrupos recebeu d~xametasona por via intraperitoneal nas dose~ de . .
. 62,5; 125; 250 ou 500µg/dia. A droga {oi administrada durante 83 dias, e, neste ' ,
período, observ(?U-se que apenas os camundongo~ da linha~ern C57BL/6, quandp ' . .
imun_ossuprimid~s ·com 1.25µg/día por via intraperi~oneal, demonstraram-se
susceptíveis a infecção por C,yptosporidium parvum, já que liberararn uma grande
quantidade ·de oocistos nas fezes, ·até o fi_nal do período no qual foi realizado o
-experimento. Os animais de tódas as cinco · linhagens estudadas, quando Joràm . . . .
imunossuprimidos com doses superiores a 125µ9/dia chegaram a óbito.
Neste mesmo sentido, PETRY et ai. (1995) induziram imunossupressão em '
camundongos adultos, fêmeas da linhagem C57BL/6, injetando dexametasona
durante quatro dias alternados, por via subcutânea, nas doses de 250, 500 ou
1000µg por: animal. Após infecção com 106 oocistos de C. parvum ·por animal, os
autores· constataram que os camundongos , imunossuprimidos com 1 OOOµg de
dexametasoná liberaram maior quantidade de oocistos quando comparado aos
outros grupos.
\.
/

/ 18
/
YANG . e( . ai. (2000) demonstraram que camundongos C57BU6 1 • •
imunossuprimidos com 16µg/ml de dexàmetasona, administrados na água potá~el,
e infectados com apenas um oocisto, desenvolveram infecção patente: porém sem
li~ração de oocistos nas fezes; · a infecção só foi constatada em cortes
histológicos de íleo terminal (2cm 'distais) corados com hematoxilina e eosina. Ao
se examinarem as lâminas, v~~cou-~ C. parvum produzindo atrofia e ·fusão das ' . \
vilosidades e dilatação das ·crip~s· intestinais. Apesar disso, em trabalho anterior,
,, YANG & HEALEY (1993) demonstraram que a 'administração de dexametasona na
água potável a camundongos C57BU6 induziu uma maior mortalidade, com sinais . . '
de toxicidade ~ais evidentes, em relação à administração por via intraperitoneal.
( .
/
j '


\
J
19
2. ,JUSTIFICATNA
Dificuldades na realização de estudos que requerem oocistos de
Cryptosporidium_ pa,vum em massa justificam,· a necessidade d~ se
desenvolver modelo experimental ~dequado para manutenção do parasito,.
já que a maioria dos modelos animais não é susceptivel à infecção por este I •
prot(?zoário:
Exi~te·m estratég_ias descritas na literatura para a obtenção de oocístos ' ' .
de C. parvum a partir da infecção de bezerros neonatos, todavia, o .
estabelecimento de um esquema para indução de imunossup~o com
corticosteróide, em camundongos adultos, em nível adequádo para se
.estabelecer um modelo experimental de . infecção, parece ser uma
alternativa ·de grande interesse para aprofl,Jndar aspectos referentes à
biologiá dest~ parasito; e, princi~lmente, obter massa de oocistos a sere;., • ' 1 • • ~
empregados em f{Jturos esludos bioquímicos, moleculares ~ imunológi~s e . . .
êomo fonte d~ antígeno~ na produção de imunoreagentes.
'
r ,
/ < •


3. OBJETIVOS
Geral
Esta~lecer modelo .animal para obtenção de ooci~os dé Cryptospbrid[um
parvum . infectando ~mundongos adultos das linhagens BAl,.B/c .e C57BLJ6,
imunossuprimidos com _glicocorticóide.
Específicos ~
Verificar as condições adequadas para a indução de imunossupressão em
camundongos das· linhagens C57BLJ6 e BALB/c, com e~prego do glicocorticóide
dexametasona, comparando a contagem global e diferencial de leucócitos no . .
sangue perifériÇ9; - ·
Acompanhar a ·infecção em camundongos das linhagens C57BLJ6 e BAl,..B/c:· • . " 1
. ~ . ) munossuprimidos con:i dexametasona e submetidos à inoculação intragástri~
com oocistos obtidos de bezerro experimentalmente infectado com C. parvum; '
Avaliár · a viabilidade· do mod~lo'. experimental murino para obtenção de
opdstos· em massa; quantificando -os oocistos liberados . nas ~zes dos . . -
camu_ndongos das -linhagens C57BLJ6 e BAlB/c infectados com C. parvum, para
análise de rendimento.


21 \
4. MATERIAL E MÉTODOS r
',. ,
4._1. lmunossupressão de camundongos
I
Camandongqs fêmeas da linhagem BALB/c com idade entre 2 e 3 meses e
peso ·variando de.·20 a 25 gramas e ma~hos da linhag~m C57BU6, com a mesma
idad.e e o n:,esmo· ~so. for~_m obtido~ nos biotério da Facu.ldade de Ciência~
Farmacêuticas e do Instituto de Ciências Biomédicas da Universidade de São . .
.Paulo, respeétivàmente.
Os camL.i~dongçs da linhage~ BALB/c foram ~scolhidos por pertencerem a uma-linhagem d~ maior acessib'il.idade,· com .grande dispo~ibiÍidade nos biotérios;
além disso, para estabelecer e verificar as condições dó efeito imunossupresSQr
dó corticóid.e· dexametasona. A escolh~ dos camµndongós da linhagem C57BU6 ' : . . . .
_baseou-se em-dadQs da _liter.a~ra indicando· grande susceptibilidade desses ao
desérwolvimento de criptosporidiose :após-imunossupressão com dexametasona e ~ .. ' . .. .
infecção com cocistos de C. parvum. Embora a maioria- das pesquisas costume , ·_ . . .
utilizar ,camundongos fêmeas, frente. às dificuldades encontradas para adquirir . \
, camundÓng0$ Ç57BU6 _fêmeas, optou-~ -pélo uso de camundongos . machos.
dessa linhagem. .
" Como droga imunossupcessora utilizou-se dexametasona injetável -adquirida . ~ -·.
en:, frasco ampola de 2,_51111, na concentração de 4mg/ mi, com o nome C?Omercial
· Decadron. (Merck). A via de .. administração utilizada foi ~ subcutânea, devido à . , .
· facilidade de padroniza~o d~ dosagem d~ imünossupressor admi~istrada para 'V -
cada camun.dongo e a m~nor toxicidade.
o corti~sterôide fpi administrado diariamente, nas dosagens de 0,5mg e L . - '
.1mg; J)Qr um período de 21 ,dias, nos camundongos BALBlc e na dose de 0,5 mg,
por um:período de 14 dias, n<;>s camundongos C57BU6.
'os camundong~ ~tilizados na ~se . de padronização do esquema de .' ' \ .
imunossupressão. (experimento 1) tc;>ram separados em grupos, da seguinte . .
maneira: ~ \
- grnpo A.: 20 can:,u~dongqs BALB/c fêmeas, im·unossuprimidos com 1 mg de
dexametaS9na por a~imal, di~riam~nte~ . . •

22
- grupo B: 10 camàndongos BALB/c fêmeas, imunossuprimidos com 0,5mg de
dexametasona por animal, diariamente; /~ ' '
- grupo C: 10,camundongos ·C57BU6 machos, im~nossuprimídos com 0,5mg de .
dexametasona pot a11imal,. diàriamente.
As. dosagens de· 0,5mg e 1 mg de dexametasona foram éscolhidas após, uma • • . • 1 .
análise CUidê!CÍOsa _ das . dosager:is . utilizadas por -Outros pesquisadó~es,' que
variaram a dose de imunossu.pressão de o, 175,:ng até 1 ,ng· por animal,· e apesar
das variaçõe~ no esquema de inJUOOSSUpressão e nos resultados de cada . um dele"s, preferif!19S realizar o~ experi~entos utiliza~qo estas duas doses. ·
,. • • #
· Vale salientar qu~. tendo em vista a di~culdade de obtenção de . ,., ' .
camundongos da linhagem C57BU6; a imunossupressão desses camundongos foi
· realizada a_penas ·na do~ge_m' de, 0,5mg de d_exametasona, para n~o correr o risco
de perder animais.utilizando uma dose.sabidamente elevada de corticóide. ~· , ' 0 ~ 1 ' • , , 1 : • ' •
4.1 .1. Avaliação ,d~ _imunossupressão · ' '
Para . anàlisãr a imunossupressão, f,oi . realizado leucograma, que permite a . ' . ~ . .
contagem do riümero relativo .e absoluto de leucócitos. Tal técnica foi realizada a • 1'
cada sei~ dias, até se observ,ar uma consiqer_ada diminuição do número absoluto . : . . .. j
de· leucócitos (50% em médi~) e inversão _do número relativo d_e linfócitos no
sangue perifé~i~ ·(contage)ll d~ .linfócitos eni torno de ·25%, em um total de 100
células).
·A ,Qua,ntidade de ··leucócitos tot~is ,por m~3 de sangue foi ~stimada pç,r
intermédio da contagem do · número absoluto, e através da ,contagem diferencial . J - • • ' • .,
pode-se acomp'a!1har o cÔmJ?Ortamento·des linfócitos após a~~ihistração da droga
imunossupreSSQra. ó leu~rama foi realizàdo somente até o dia da infecção, . .
para evitar que um soma!-9.Jio de procedimentos viesse a provocar o óbito dos
animais.
·Amostras. de 25µ1- de sangue dos. animais . submetidos à imunossupressão , . .
. foram diluídas na-propor~o 1:20 êm líquido de TüÍ1< e contada~ em câmara de
Neubauer, sendo a leitura da· contagem diferencial realizada em microscópio 1 •

23
óptico, através de esfregaço sangüíneo, corado pelo Leishman (Merck S. A.;
Indústria Quimica,,R. J.).
4.1 .2. Manutenção-de camundongos ·imunóssuprimidos /
Os a,nimais: imunossuprim,idos fqrai:n mantidos em condições rigorosas de
qualidade sanitária, sendo todo o material utilizado autoclavado e esterilizado
(gaiolas, bebedouro!i: m~r_ava;lha), ·COf!! o intuito de evitar a infecção dos ·
camundongos co~ outr~s patóg~nos: Para manutenção diária dos· camundon.gos,
os equipamentos de proteção individual incluíram · avental descartável, máscara .• ~ • ~ J
luvas e óculos de proteção.
·4.2. Obtenção de Cryptosporidium parvum a p~rtir de bezerro
. Para · obtenção de oocistos de C. __ parvum, um bezerro . da_ raça holandesa
· recebi_do por'. doação de uma ~àzenda do Município de_ Caçapava, Vale do Paraíba,
SP, .~m ·cinco dias de idade, sem te~ mamado colostro da sua progenitora! foi
infectado por yia oral com 2,5x107 oocistos. Estes foram obtidos a parti~ ·de um
outro bezerro natur~lmente infectado, proveniente da mesma fazenda que o . ·, . .
primeiro. O animal -permaneceu no biotério ~o Laboratório de Parasitologia da ' ' .
Universidade de 1aut,até (UNITAU), recebendo os devidos cuidados até cessar a
liberação dos;~istos. Para diminuir a _tjupntidade de gordura presente nas fezes,
durànte todo -~:>' períodq da in~o·o bezerro foi alimentado diariamente com dois . .
litros de leite desnatado. Após ter cessado a· diarréia e com o término da liberação 1 . '
'•
· dos oocistos, o animá! passou a receber diariamente dois litros de leite integral e 1 '/ I _
água.
Com ~ início do_ processo diarréico, as fezes passaram a ser armazenadas
em saco coletor , sem conservantes, sendo ' diariamente transferidas para
recipientes contendo sqluçã~ de dicromato de potássio a 5%, na proporção 1 :2.
Para verificàção da pr~sença ou ausência·de oocistos de C. parvum nas fezes, as
amostras foram analisadas pela técnfca de ~utuação em solução .de sacarose _,

24
·(SHEATE~. 1923). Este procedimento foi realizado até consta~ção da ausência
de oocistos nas fezes.do animal. 1 I
4.2.1. Purificaçã<? de oocistos e preparação do inóculo para infecção ~os
cam~ndongos , • ~ -- 1 •
. '
Os oocistos excretados nas fezes dos bezerros foram isolados pe_la técnica ' -
de purificação em ·grai!iente de sacarose. (Bl,.JKl1ARI & SMITH, 1995). Cer:ca de ' .. . ..
2ml de. fez~ preservadas. ~m dicroníato de potássio a 5% foram homogeneizados 1 '
ern ~bos de fundo cônico . de 151:ril -conte.ndó 10ml de solução de Sheater
(sacarose: densidade \~Og/ml); a '.su_spen~o 'obtida foi ~ntrifugada á 1500rpm . . ~ . por 1 o minutos. Após centrifugação foram removidos cerca de 2ml da camadá
. superior, contendo.os oocistos, e cotocados·em outro tubo cônico contendô~3ml ~ .
·de ág.oa destilada; sendo que a/suspensão ol)tida foi "centrifugadaa 3000rpm por '. . '
1 o · mint:1tos, para-. remoç~o da sacarose. Este· _procedimento · foi , repetido até 1 • ~ • • ' • •
completa remoção da sacarose. -Ao pr~ipitado.obtido foi adicionado hipoclorito de · . ' ..:.. .
sódio, para · remoção de contaminantes e a suspensão resultanté foi novamente · . ' ' ·. . .
cenfrifugada ~ 3000rpm por 10 ·minutos .e posteriormente ·1avada três vezes com ,
(igua bidestilada para remoção do hlpo_ciorito: -Os ·oocisto~. presentes foram
ressuspensos ern ~oluçã·o salina .ta~~nada com fo~fàtqs (PBS), 0,01M, pH 7,2. " ' ' ' -
para um volume.final de 1,5ml. . '
Para a prep~ração do inóculo · uti!izado na. infecção dos camundongos,
·procedeu-se a qua~tificaçã~ dos oocis~s obtidos no procedimento de purificação, ' . . ... ~
confeccionando-se e.sfregaço~ com 1 Oµ! da solu.ção de PBS contendo os oocistos. ' '
· Os .esfregaços foram corados pela técnica .de Kinyoun modjticada (metodo_logia
descrita no ~nexo 1) e o núméro de . oocistqs quantificado foi convertido para o
volume final de 1,5ml. ~osteriorrnente realizou-se diluição ·dessa suspensão de
oocistos, prepar~ndo-se_os inóculos empregados, nas infecções .
. /
4.3. Infecção de camundongos e coleta dos oocísto_s · . ·1
\
·--- · BIBLIOT ECA Faculdad_e de Ciências Farmacêoticas.
Univetsidade de São Paulo

25
Uma vez estabelecido o esquema de imunossupressã<;>, hovos grupos de
camundongos ·das duas linhagens estudadas fora~ imunossuprimidos com ,
dexametasona e infectados por inoculação intragástríca -com solução de PBS
contendo 2x104 oocistos purificados, em dose única, diluídos em o, 1 mi de PBS- _
0,01M (pH t,2). · À inf~o- foi realizada no 142 dia do procedimento de , .
imunossupressão sendo que à. adminisJração _diária de dexametasona foi mantida
até o final do experimento. · /
Os camundongos infectados foram divididos em grupos da seguinte maneira: ·
. . - grupo 1: 1 O camundongos BALB/c fêmeas im~nossuprimidos com 1 mg de
dexametasona_ pór animal, diar<ism~nte, ~ infectados com 2x104 ooctstos de e. parvum;
- grupo 2: _ 1 ó camundongos , BALB/c. fêmeas -imun9ssuprimidos ·com 0,5mg de
dexametasona por animal, diarian:iente,- e . infe~dos com 2x104 oocistos de e. ' ,
p~rvum; . '
- grupo 3: 10 camundongos C57.BU6 mact_los. imunossyprimido~ com 0,5mg por
animal, diariame~te, e infectados ~qm 2x104 oocistos de C. pa'rvum.
Com o intuito de acompanhar a infecção, para cada grupo de camundongo -- - - . > imu11ossuprimido e infectado (grupos· 1,. 2 e 3) foram utilizados grupos controle
distribuídos da seguinte maneira: 1 - ••
- grupo 4: ~ camundohg9s BALB/c não if11unossuprimidos e não infectados-. para
analisar as condições sanitárias ~o ambjente; ·
- g·rupo 5: 5 camundongos C57BU6 _não imunossuprimidos e não infectados - com . . -
a mesma função_ do grup_o 4; . ·
- gru·po 6: 5 camundongos· BALB/c-imunossuprimidos com 1 mg de dexametasona . . -diariamente e não· infectados - para analisar se o procedimento de
imunossupressão, isoladamente, não seria tatal.aos camundongos; . ' -
- grupo 7: 5 camundongos BALB/c imunossuprimidos com 0,5 mg de-
dexarnetasona diariamente e não in~ctados - ~m a mesma função do grupo 6;
- grupo 8: 5_ ca~undongos C57BU6 imunossuprimidos com 0,5 mg de ' ' '
dexametasona diàríamente e n~o infecta~os - com a mesma função-do grupo 6;_
! ·

,, 26 - • 1 •
- grupo 9: 5 caiTi~ndongos BALB/c.não imunossuprimidos e infectados com 2x104
oocistos de C. parvum - par~ .avaliar se o inóculo utilizado, sem a presença da
droga imurto~supressora,: seria suficiente para induzir ~ma infecção na linhagem
de camundongo estudada~
- grupo 1 Q:;' 5 -camundongos C57BU6 não imunossuprimidos e infectados 'com
2x104
oocistQS d_e Ç.' parvum - com á mesma função do grupo 9.
4:3.1. -Acompa~hamento ~~ infecção dos camundongos .· . .
. . Para acorhpanh'amento , da · inf~o. · os camundongos forani isolados
individu~lmente em g_aio~as ~terilizadas e· pavimentadas com a_~ame. As fezes .
liberadas diàriamente ·ficàram· sobre toalhas: de papel dispostas na parte inferior . \ . . ':"
das gaiolas, Joalhas ~tas que forárrf umedecidas com. água destilada e trocadas . • • , • . • - 1 •
diariamente (Anexp~2).:· O voluf!18 totaf de fezes eliminad?s diariamente por cada . -. . - . {
camundongo_ foi atm~Cj?nad<i·em tubos contendo dicromato de potássio â 5%, na
propo~O' de.- -1:3·( 9bte;do.:s~· ·su~pep~ ·-,~is que furam e~aminadas para • 4 t • '. • ' '
verifica~o da presença, de oocis~os de ç. paMJm. Em um tubo cônico com
capacidade para 1.5ml, 3m_l ·dà su,spensão de· fezes obtida foram dissolvidos em ' ~ . - . " . . .
10ml de solução . de '-~car~sé, · d_énsidad~ · 1,2g/cm3• sendo esta suspensão
• • ) • 1 ' ,, ., - 1 •
homogeneizad~ e centrifug~da .a '1500rpm por 1 o minutos. Com ·o auxílio de um~ ' ' '
alça de platina, duas . ,aroo§.tràs da película superficial do centrifugado foram ·- '
transferidãs para uma fâmi~a · de_ microscopia e recobertas separadamente com
lamíriulas _de vidro de ,1~\A pesquisa·:de oocistos de C. paNum foi ~ealizada em
microscópio_ ópti~. em a~nto de 400X. ·
4.3._2. R~cuperação de oocis_to~ das fezes dos càmundongos infectados
.Para se recuperar os . ~ist~ liberados nas fezes dos camundongos
infectados, alíquotas de 3ml da suspensão fecal obtida foram processadas em J •
tubo cônico, contendo 10ml de sólução de sacarose. sendo que . após . ,
centrifuga~o a 1500rpm por 1 O minutos, os 2JTII · da camada syperior da solução
!

27
foram recuperados: com o auxílio ~e pipeta · automáti~ e ·transfe~idqs para outro
tubo cônico com capacida~e --par~ 15ml; contendo 13ml de água destilada. A
· suspensão ~btida foi -submetida ·à ' cenbifugação a 3000rpm_, por 10 minutos, para
remoção ~a sacarose! permitindo assim · qu~ os oocistQs-,precipitassem. _ Este
procedim.ento de lavagem foi repetidó duas vezes. Finalmente o sedimento foi . . '
d_esinfectado com hipoclorito de sódio_ e lavado por três vezes com água destilada ' ' .
realizando-se centrifugação ç1 30qOrpm por. 1 o minutos e ressuspensão em 1,5ml
de PBS, pa~ .posterior quantificação.
4.3.3. 'Quantificação dos oocistos de ç. parvum. recuperados das fezes dos ' 1 •
camundongos infectados . ' '.;
Para ,quantificação-dos' ooç'is_to~· recuperàd.os das fezes dOS· camundong9s,
foram confeccionados· esfregaços:·d~·-10µ1, p~-rti-ndo ~a ·solução estocada em PBS,
sendo est~s . ,x;sfe~rm1::~té· ~rados . pela técnica de Kinyoun .. modificada.- o n_úmero de oocistos foi . contado e convertido para o volume final da suspensão de
. . r . .
fezes purificadas d_e. _câ~a .. ~mund~n90, _ é,· poàteriorménte, p~ra o total de fez~s
eliminada diaria~ente por cad~ ·~nim~I. _ .
f3.4. Ma~mtenção da cepa de C.p;1rvum i~olada
,, ~,
Após isolamento da ~pa de e. .parvum, real_izou-se inoculação de um novo ~ . '
grupo de cam_un~ongos ~a linhagem C57BU6,. imunossuprimidos diariamente com·
0,5mg dé dexam~~sona. po~ via subcutâneà, ·com ·O intuito de verificar a
intectividade dos ~istos.' recupef~dos dos ~mündong_os infectados inicialmente,
.bem como para veri~êar --~- viabilidade do ,- model9 . experimental utilizando
~mundongos imuno~~uprimidos com. dexameta~ona. .
Neste segu~dÔ ·e~rimento~. ci~co ca,murÍdongos . (grupo 11) da linhagem 1 • .... . ••• • • ' • _, ' /
C57BU6, irryunossupritnído,s com . dexameta~na, foram infectados com os
oocistos recuper~d~s dó primeiro .experimento de imunossupressão e infecção. O . . . . ,- . _/ . . . . 4
inóculo deste grupo de cam~nd:ongos foi o mesmo_ utilizado antenormente, 2x1 O

28
. oocistos por animal~ ,~este grupo, as fezes liberadàs diariamente por todos os
camundongos foram coletada$' é armazenadas em um mesmo tubo coletor. ' . - .
Os oocistos · recuperados ··toram purificados por flutuação em solução de ' .
sacarose, e a suspensão obtida foi submetida à ~esinfecção com hipoclorito de
' - sódio e ar.mazenada eni · dicromato, de potássio· pará manter a viabilidade do~
oocistos; a quantifiepçã~ dos oócistos .recupeFados foi realizada conforme descrito . . '
no item 4,3.3~ . "
4.4. Análise estatística ·
Os valores meqia.nos dos · 1eucócitos foram CQmparados empregando-se o
teste Kruskal-Wallis _ complementa~o · ,á posteriori pelo método de Student- r
Newr:nán-Keuls, que ~rmite, a C?mparação múlbpla,- para isolar o grupo ou grup9s -
que diferem estatisticamente dos outros, ao nível de significância de 5% (p< 0,05). • I ,. • •
' '


29
5. RES_l.JL TADOS . /
1 '
5.1 \ Avaliação da ;_mu~ossupressão dos camundongos
,. • • •••• • •. 1 • • • • • ,
Todos os.. camundong~s. ·· ,-c;J~ ·amt?as as . linhagens, ·que, foram ' . '\... - . ~; . \ .
imunossupriniidos·. :aJj~e~n~iaqi,_ um~ .. s_íntoff!attllógia ciínrca semelhante; tendo • ' ' ... t •.• ;- ~·. r("- J. • • • . t" . • ' . •
com_o s~htofn~s_ ~~is ·m,r.ça,n~~--~rd~; d~:-peso, inapetência e prostração .. _No
, .decorrer do pr,o~Ímeht9 ;de· Íniµh~upr~ô algÚns' camundongos também . ' ,• ' . ·À.· ~. .-~-.= -•. •• • - '
desenv?IVercJm_ e~râ1:,~â;~ -~ -~a-r-É}Qi~-ptóxíma-à. cauda, talvez_ devido à lesão -' ' '.. ' ·:-~-:i\ ~-j. •• • - .' • • •• • • -
causada pelas. te~tid_a's::ar>f ~ :~P ~coipçôide .no local. . '
N_ão hO"ui ~·.'°i>bltq_ :~é,:;:ça'm~~do~g~, ·da · linhagem ~· BALB/c dura·nte o , 1, • / ..1-·· _ f • • t "- , ,, _.,,,__ , ·- .. ~
procedimento' d~ · ijnu~ó~uP,re~sã?; pq,.-~n!:ânta os camu~ngos da lir:ihagem • f ' • • .. • '
C57BU6· iniunossupnrrÍidÇ>S:· éôjfleçaram ·à_,· morrer . após a- segunda semana . de • • ,... .• ' ••• • • • '. ·~ J • • •
corticoterapiâ', razão' ~ra ·qua(~r~âl~rrto~. 0
0JetJéograma:dessa Jinhagem apenas , • ~ ; ·1 :-· : 1 . • • \ ' :. ' /·· ·"· , ,., J ·, '. 1. • • :
nas duas ~iimeiras;~~ànas d(j e~pê,iimento-; .. ·_. 1_ ; · ' ,, •. . , 1 ., • , '·. .i • ' ' ,
. Nas Tabela~. t,.-:2:'ê!-'3,· ~st4'ô .. ~pre~.ntá'dm(os .resultados de le~cograma
, eXpfeSSOS ~~ valores~a~Ô.l.µtb~{~~ le~it~ (~·o de l~u~itê>~mm3
de_ sangue} e
valore~ relativos·(pottem,ag~m) ·c;1e·-rieuupfilbs s~me~tados e linfócitos d(? sa~gue_
periférico~- dos '·-~mY,n~-~~gbs-··.~ó-_gru~</ ·Á, · B. ~ e, -r~spectÍvamente, durant~ a
: administração de 5ieJm~tai.o,~a'.: os ·v.~iores·· m~cua~os dos 1eucócitos dos grupos . • • i . -~ ~- , • .- , •. 1 • - ) - ~ •
A, B e ·e, durante -o· procegimento . de imunossupressão, ;estão representados na . . . . . . . ~
figura 1'. ·· ' ' ·
, ·
' ,

/
Q) "O ' 15000 ("')
E E - 10000 U) (l) o ::J
' .. ~ O> -Oc <> <U 1 o (/) 5000 ::J (l)
(l) u . z o
1 2 3 4 ,
Período de imunossupressão ém semanas
· · ·:· · grupo A. -- -grupo B --grupoC
30
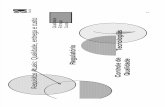
Figura 1. Número de leucócitos/mm3 de sangue de· camundongos, expressos em medianas: Grupo A ., 20 camundongos BALB/c imunossuprimidos com 1,0mg de dexametasona; Grupo 'B - 1 o camundongos BALB/~ imunossuprimidos com_ 0,5mg de dexametasona ~ grupo C~- 10 camundongós· C57Bl../6 imunossuprimidos com 0,5mg dedexametasona . . , .. · ; · . · · . . :
I •,
. -· \ .
Apó.s rompa~ção dos ~alores···medianos dos leucócitos, pelo teste Kruskal-i ' . t -.. , .-. .'\ •
W~llis complementado pelo· métod.o -de .St(Jdent-Newman-Keuls, verificou-se que . ; -
quandó os camundongos d~: linhá~m SALB/c _foram imunossuprimidos·com 1 mg .. ~ . . . - . . .,. ;
de dexametasona, ós· valores de leucócitos · totais do ~ngue periférico, antes do . . .
procedimento de _imu~up~o. 'diferiram significativamente (p<0,05) dos • - • L.
valores observado~ após ,a.prjmeira.e segu~a semana de imunossupressão, que ' • j -~. • : - ~ '· • • '.
não difer~nciaram :sígn~cativa~nte · entre .si (p>0,05); . entretanto na terceira '· . .
semana de·. imun~ss.~ptessão . ·o·. _nu~er9 -d~ · leucócitos · foi estatisticamente • . • • • ,' :· / ' ! • .\ ._ . , • - I
semetha,nte ao .obseryac;to ahtes dQ. Procedimento de imunossupressão, ou seja, . ,, . . ·/ . . . ·, ' . .
iguàl aos valores normàis{ía.~!a 1 - grupó,A). . . . , .. . ..
Já os cam~ndongÓs 'da linhagem BALB/c que forar,:i imunossuprimidos com . ' '
0,5mg diári~s de dexàmet!~na, apresentaram os valores çte leucócitos totais do l ,• . '
sangue perjférico, antes do p~~mento de imunossupressão, significativàmente
diferentes (p<0,05) · dos_ v,tore~ observa~o~ após a primeira, segunda e terceira
semana,· de · imu11o~upressão, qu~ ··pôr ~_ua vez· nã? diferiram significativamente
entre. si (p>0,05), indican~o que após' ·a. primeira ~mana da administração de
;...

31
dexametasona, a drQQa Íf1~uziu· uma imunossupressão que se manteve em um
mesmo patamar áté a terceira semana de imunossupressão (Tabela 2 - grupo B). . ·' - . ', '
No caso dos camundongos õa· linhagem C57BLJ6, imunossuprimidos com .. \ . "'· .
0,5mg de dexame1asona, ~ observou-se ·que os valores de leucócitos totais do • t ,. •
sangue periférico, antes- dó' procedi.manto ' de imunossupressão, diferiram . , - .. . . ~ ; ... .
significativamente. (p< 0,0~) dós I yalores observ.ados após a primeira e segunda . ._ ~ . ' - .
semana de imtinossupressão; que não diferiram significativam~nte entre si i •
(Tabela 3 - grupo_ C).. . .
. Com relação aos valóres ·relativos de leuoocitos, ob~rvou-se que tanto na
linhagem - BALB/c qu~nto · ná C5iBLJ6, em ambos os ~rotocolos d~ . . - - . ,, .
' . imunossupressão, houve uma inversão na proporção dos valores de linfócitos em
relação aos neutrófi~ ~o c;tecorrer da adminis~çã~ da droga (Tabelas 1, 2, 3).
/
. '

Tab
ela
1.
Res
ulta
dos
do· 1
euco
gram
a de
sa
ngue
pe
rifér
ico
de
20
cam
undo
ngos
B
AL
B/c
fê
mea
s (g
rupo
A
) su
bmet
idas
à im
unos
supr
essã
o co
m d
ose
diár
ia d
e 1
mg
de d
exam
etas
ona
, ant
es (
AI.
) e
após
a p
rimei
ra,· s
egun
da
e te
rcei
ra s
eman
a da
imun
oss.u
pres
são
· -.
Neu
tróf
tlos
(VR
) L
infó
cito
s (V
R)
Cam
undo
ngos
A
.L
1lla
em.
2!ia
em.
3lla
em.
A.L
. 1A
ae~
2lla
em.
39-e
m.
1 30
8
' ª'
78
. 7
0
16
16
22
,
2 25
8
8
95
91
75
~2
5 -
9 -
3 21
87
90
72
79
. 13
10
28
,4
24
86
M
79
7S
14
' 8
-21
5
28
90
90
90
14'
10
10
10
6 25
89
90
8
5
75
11
10
15
7 30
82
95
12
10
18
5
28
• 8
30
89
92
81
.10
11
8 1
9
91
21
88
90
88
73
12
10
12
J 10
28
94
' 90
8
8
72
8 10
14
'
11
211
. -
89
12
30
80
10
70
20
10
13
29
88
95
9
0
71
14'
5 10
1-4
28
95
--
72
5
15
30
93
96
-70
7
' 18
32
89
90
-
68
11
10
17
. 32
90
95
92
68
10
5 8
~8
31
92
96
-8
9
8 ,.
19
30
90
10
-
10
10
10
20
23
89
N
9'
17
11
8 8
l,J
IV
VA
= V
alor
es A
bso
luto
s (n
º de
cél
ulas
/mm
3 de
san
gue)
; VR
= V
alor
es R
elat
ivos
(%
); (
-) :=
Dad
o nã
o ob
tido

-.,
QI
(")
e e
e:
:::,
Q
J
<.
~C
D
<1>
-cil
a
. ci
: Q
C
D
a,
(")
' G
. -
·
_/
<1>
<11•
-
e.
;::
o '·
<1>
a;·
. (/)
.,,
-,
!>),.
., m
o
~
r--.
"t)
3
• ,
~ ~
>
õ ~
- &i'
..,,
Tab
ela
2.
Res
ulta
dos
do
teu
cogr
ama
de
sang
ue p
erifé
rico
de
1 O
cam
undo
ngos
B
ALB
/c f
êm.e
as
(gru
po B
) _ s
ubm
etid
as à
im
unos
supr
essã
ó co
m d
ose
diár
i~ d
e 0
,5m
g de
dex
amet
ason
a, a
ntes
( A
I.)
e ap
ós a
prim
eira
, se
_gun
da e
terc
eira
sem
ana
da im
unos
supr
essã
o ·
·
_ Neu
tróf
tlOI
!VR
) U
nfó
clto
a (Y
R~
Cam
un
do
ng
o•
A.L
1
~e
m.
-2~e
m.
3~
em
. A
.J.
1lls
em
2l!s
em.
3gse
m.
1 17
50
73
6
6
69
46
,
27
32·
2 2
4
47
56
u
46
43
,, 3
23
48
52
·7
2 4
7
48
4 11
4
8
. 70
6
6.
88
41
30
3"
~
5 25
50
74
75
4
8
28
8 20
'
40
85'
60
78
59
35
40
7
28
87
48
68
. 68
·32
52
32
8 21
47
64
70
5
6
36
9 4
34
64
91
66
36
\
10
19
32
70
58-
71
82
29
42
1
VA
= V
alor
es A
bsol
utos
(nº
de
célu
las/
mm
3 de
san
gue)
; V
R=
Val
ore
s R
elat
ivos
(%);
( -
) = D
ado
não
obtid
o
w
w
'

,
' '
Tab
ela
3.
Res
ulta
dos
do ·
leue
ogra
ma
de
san
gue
perif
éric
o de
1 O
cam
undo
ngos
C
57B
L/6
mac
hos
(gru
po
C)
subm
eti~
os
à.
imun
ossu
pres
são
com
. d
os~
diár
ia
de.
0,5m
g de
de
xam
etas
ona,
ant
es (
A.1
.) e
apôs
a p
rimei
ra e
seg
unda
sem
aria
da
imun
ossu
pres
são
------
---~
-N
eutr
ófilo
s (V
R).
'·L
lnfó
cit<
>~ (V
R)
Cam
undo
ngos
A
.L
'Í11 sem
. ~
em
. A
.l.
151 aem
29 a
em.
1 13
65
·
80
,8
7
35
19
2 13
65
75
87
35
3$
3
10
70
75
90
30
35
4 10
84
· 90
90
16
10
5 11
74
85
89
26
,
14
6 9
.94
'89
90
16
10
7 .
6 60
70
9
4
40
28
I
8 6
60
65
91
40•
35
-· 9 12
60
80
86
40
20
,
10
10
65
85
80
45
15
. (
• •
\ 1
VA
= V
alor
es A
bsol
utos
(nº
de
célu
las/
rnrn
3 de
san
gue)
; VR
= V
alor
es R
elat
ivos
(%);
(.·)=
Da
do
não
.obt
ido
'
__,·
-.
/
/
\
(.,..
1 A
,

35
5.2. Quantificação dos oocistQs recuperados de camur:idongos infectados
Apenas os camu~ongos da- linhagem C57~LJ6 que foram imunossuprimidos e
1 infectados com C. parvum (grupo 3) desenvolveram infecção e liberaram grandes
rquantidades de oocistos na~ fezes,' o mesmo não ocorrendo com os câm\,lndongos dos
~grupos controle da mesma linhagem (grupos 5, 8 e 10), nem com os cam~ndongos ·da
linhagem BALB/c (grupos 1 e 2)·e seus respectivos grupos controle (grupos. 4,6,7 e 9). ,· .
Os números de oocistos, expressos em· média aritmética, recuperados dos
: camundongos do grupo 3 estão representados na figura 2. Nota-se que a maior liberação de· r . . 1·oocistos se deu no oitavo dia após a infecção. Os valores a partir do 18~ dia do experimento
\
não estão apresentados, já que a partir deste dia apenas três camundongos estavam vivos.
i 35000 1 ,(1)
.S 30000 ~
.g 25000 e-m rJ a.. __ 20000 i3:ii ~ .5 15000 CI) ·e: o m -(1.1
'§ 1000.0
5000
•
2 0 -l---~--~ 1 2 3 4 5 14 15 17
animais.vivos 10 10 10 10 10 10 10 8 7 7 7 7 5 4 4 4 4
1 ~ Figura 2. Número total de oocistos, expressos em média aritmética, recuperados a partir das fezes de camundongos C57BU6 imunossuprimidos com. dose diária de 0,5mg de dexametasona (grupo 3), até o .11.12 dia pós-infecção
/
/

36
I
Na tabela 4 está apr~sentado o número total de oócistos recuperados por camundongos
da linhagem C57BU6 imunossuprimidos · e in~tados com ' 2x104 oocistos dé C. pa',vum
(grupo 3). Todos os camu~donQOS d~ gru~ 3 liber"aràm. oobstos nas- fezes.' a partir do quinto
dia da infecção, sendo esse _diagnóstico realizado pela técnica de flutuação em sacarose ~ .
(SHEA TER, 1923). Todavia, . observaram-se variações nó te,npo d'e sobrevida dos
camundongos, sendo que apenas um deles permaneceu vivo e liberando oocistos até o final . ' do per.íodo de infecção_ (29º dia}. _ _,,..
No quadro 1 estão representados_ os núméros de camundongos que evoluiram ao óbito, 1 • ~ ••
,de todos os grupos que· foram' utilizados em nossos e..xperimentos, demonstrand<? que só os
camundongo~ da linhagem C57BU6. que foram i~unossuprimiqos ou imunossuprimidos e '1
infectados com C. parvum morreram.·
Quadro 1. Resumo dos procedimentos de imunossupressao é _infecção realizados!! do
dia,de 'óbito dos animais
Grupos linhagens dexametasona , inóculo n• nº de óbitos dia do óbito
A BALB/c . 1 rng <ftârio - 20 zero · -
B BALB/c 0,5.mg diário - 10 zero -e C57BU6 0,5 mg diário - 10 03 152 dia
,
1 , BALB/c 1 mg diário 2x1 O" oocistos 10 zero -2, BALB/c 0,5 mg diârio 2x1 O" oocistos 10 zero -
3 C57BL/6 · 0,5 mg diário 2x1 O" oocistos 10 06 -142 dia
4 BALB/c - - 05 zero· -- .
5 C57BU6 - -'
05 zero -' . '
6 ' BAl.,B/c 1 mg diário - 05 zero -
7 BALB/c 0,5 mg diário - 05 zero . -
8 C57BU6 0,5 ·mg diário - -· os- 01 15ª dia
9 BALB/c · - 2x1 O" oocistos 05 zero -
10 C57BU6 - 2x·104 oocistos 05 zero I -
11 C57BU6 0,5 mg diário 2x1 O" oocistos 05 05 12~ dia
•n - nº de animais por grupo
,,
/

Tabe
la
4.
Núm
ero-
de
ooci
stos
de
e.
parv
um
recu
pera
dos
das
feze
s de
ca
mun
dong
os
imun
ossu
prim
idos
com
dos
e di
ária
de
0,5m
g de
dex
amet
ason
a (g
rupo
3),
do 1
2 ao
152
dia
pós-
infe
cção
C
57B
U6
·
Cam
undo
ngo
Per
lodo
de
infe
cção
em
dia
s 1
2 3
4 5
e 7
8 9
' 10
11
12
13
·
14
15
1 o
o O
· o
3875
11
803
1050
10
5000
23
100
+
+
6825
+
16
5313
+
,
.2
o o
o o
5383
84
00
2677
5 40
800
2362
5 ,
+
+
+
Óbi
to
3 o
o o
o 12
60
, +
28
35
2887
S.
1134
0 22
050
8400
86
83
4620
31
5 12
60
4 o
o o
O·
3938
18
80
3780
.Ó
bito
5-o
o o
o '
+
' 11
025-
1680
0 16
800
' 10
50
+
210
~
. Ô
~lto
8 o
o o
o 22
05
240
+
.+
Óbi
to
7 o
o o
o '8
505
4987
!5
1932
0 17
220
1050
0 10
2900
'5
8700
13
650
8137
5 58
800
5250
0
8-
o o
·º o
5858
5 28
823
7308
0 24
570
2310
0 33
075
3780
0 51
45
2457
0 47
25
-40,4
3 -
9 o
o o
o·
+
6075
58
275
Óbi
to_
.10
o o
o o
+
+
788
9923
28
980
5418
0 é5
55
1470
12
075
Ôbl
to
Tota
Vdl
a o
o o
o 81
!541
1:
1772
1 20
2703
24
3188
12
1895
19
2360
11
2685
35
753
1226
40
8037
8 57
803
Tabe
la 4
(cQLn
t.)_
Per
fodo
de
Infe
cção
em
dia
s C
amun
dong
o 18
17
.
18
19
20
21
22
23
2"4
25
26
27
26
29
~o
Tot
al/
, ca
mun
dong
o
1 79
20
1365
0 38
75
1559
3 15
120
1275
8 36
75
Óbi
to
. 24
0182
-
2 10
-498
3
3 27
720
1260
13
5240
3Z
800
86
7~
28
350
óbit
o 38
8893
4 '
9398
-n
1
5 45
885
g 8
' 2-
445
é õ.
~
. 'E;
. o.
, 7
5188
0 71
40
4410
0 2B
350
6825
28
35
9187
5 40
95
8085
0 85
100
1260
0 42
525
3822
5 18
900
Óbi
to
98-4
425
:;
e.>
-
0. ~
CJ
8 +
+
12
285
+
+
8453
Ó
bito
33
6284
e
. ("
" r.
6435
0 ~ i:
-·
9 .
(1)
5 o
10
1189
71
~ -·
a
, Q
) -1
"'
"'
-ri
rn
Tota
Vdi
a 87
300
2205
0 19
5300
81
743
8869
5 52
398
9187
5 40
95
8085
0 85
100
1260
0 42
525
3622
5 18
9,00
22
5177
6 ~·
~ó
~ ~
J>
+ =
dev
ido
ao b
aixo
par
asiti
smo
·não
foi p
ossí
vel q
uant
ifica
r ,
% ~-
-l.,
.,I
~•
L -
-.J
Q
VI

38
Alguns camundongos liberaram pequenas quantidades de oocistos em determinados
dias, não sendo pc;>ssível recupera-los, ~vido à perda d~stes no procedir}lento de . .
purificação_ Na figura "3 está ~presentado º. total de oocistos obtidos na , infecção
experimental do grupo 3, verificando-se 1,1~ rendimento cerca de 1 O vezes maior que o
inóculo utilizado_
'·
) 2500000 l ioooooo 1
2251776
1500000
1000000
500000
Total de oocistos inoculados Total de ooc::i&1os recuperados (29dias)
Figura 3. Número total c(e oocistos inoculados e número total de oocistos recuperados do grupo 3 (1 O camundongos C57BLJ6 imunossuprimidos , com dose diári~ de 0,5mg de dexametasona e inoculados com 2x104 oocistos de Qyptosporidium parvum)
,,
5.3. Manutenção da cepa de Cryptosporidium paNUm em camundongo
O grupo de cinco camundongos da linhagem C57BU6 (grupo 11) infectaçjo com
-oocistos isolados do grupo 3 também iniciou a liberação de oocistos nas fezes a partir do 42
dia de infecção_ Dentre os cinco animais, três morreram no 1 Oº dia da infecção e os outros
dois morreram no 12º dia_ Na figura 4 está representado o total de oocistos recuperados
nesse grupo de camundongos, duran~ os doze dias nos quais os· animais eliminaram
oocistos.

500000
420350
)
100000
o -+----
Total de oocistos inoculados T atai de oodstos recuperados (12dias)
- '
39
Figura 4. Número total de oocistos inoculados e número total de oocistos recuperados do grupo 11 (5 camundongos C57BU6 imunossuprimidos com dose diária de 0,5mg de dexametasona e inoculados com 2x104
· oocistos de Ctyptosporidíum parvum recuperados dos camundongos do grupo 3)
'

.,,,, B I B L IOTECA Faculdade de Ciencias FarmaC'êuticas
Uni·,ersidade de São Paulo

40
6. DISCUSSÃO
A manutenção do ciclo de Cryptosporidium parvum em laboratório é de
importância fundamenta( para a obten~ de parasitos em massa e para produção
de antígen~ à serem empregados em estudos imunológicos, ~oleculares e para '·
esclarecimento . dos vários aspectos que dizem respeito à relação parasito-- l
hospedeiro.
No início de nosso trabalho, convivemos com a dificuldade de sé obter uma . - ,,. . ~
fonte de C. . parvut11 para concr:etizaçãp de estudos que já vinham sendo realizados
no nosso laboratório; para isto, foi necessário efetuar um trabalho de busca
exaustiva de bezerros que esti.vessem liberando· oocistos nas fezes, em algumás
fazendas de gado'leiteiro do'm~nicípio_ de Caçapava.
Apesar da grande quantidade de oocistos recuperáveis de fezes de bezerros
. infectados;.as dificuldades de manutenção desse modelo, ~is como os riscos de
. contaminação do meio e a . 'necessidade de um. espaçq -adequado para
pe~rnanência do animal, ·nos levaram a avaliar o modelo murino para manutenção·
deste protozoário.
Em nossos· experimentos para infecção do bezerro, foi necessária uma
adaptação cuidadosa das condições laboratoriais: o animal foi isolado em local . .
adequado ~ foi alimentado com leite desnatado para evitar a presença de gordura
nas fezes, o qu~ dificultaria a flutuação dos oocistos na solução de sacarose. Vale
salientar . que, apesar do bezerro ter sido alimentado com ' leite desnatado, a
matérià fecal coletada se manteve com uma considerável quantidade de gordura e
detritos, 9 que d~ certo modo dificultou a· recuperação e quantificação dos obcistos
de C. parvum_
Senqo· o bezerro um animal pouco usual em nossos trabalhos laboratoriais.
houve maior dificuldade em sua manutenção, tendo sido necessária, devido ao · . ' ' . ..
seu porte, presença de dois maniputadores para alimentá-lo e coletar a matéria

41
fecal; além' di~so, em função do elevado volume de fezes excretadas pelo ·animal,
existiu um risco potencial' de contaminação do meio e dos manipuladores. /
Por outro · _la9o, q_uand9 / tra~hamos com camundongos, um urnco
manipuladpr '!'anu~u (?S anim~is-e devido .. ã ·pequena quantidade de gordura na
mat~ria f~I. apen~~ um~ etapa de, purificação em solução de sacarose foi . - . ·. . - , - - . ' . '
suficiente para se obter -uma . preparação. contendo oocistos purificados, com ' .-- .
pequena qúantida.de de d~~os. -~is, devido :ao fato dos camundongos se
encóntrarem núm_a área· r~strita, _em. gáiql~ -individualizadas, foram menores os ' . . \
riscos de contàmir_1aÇ?Q. pessoal ~ -am~ie~I quando comparado com o observado
na maI:\lpulação do0
bezéff0,·-- : -. - . ' • ) r
·,_ - j • ' -'-,
No pré~nte estuq~;. dérri9nstr~1"90S q~e á admínístração de dexametasona . . .... . ,
por via .subcutâ_nea, na 'dos,e di~ria ,9e .,ó~$r11g,,. a camundongos das linhagens
BALB/c- e· _Ç57BU6 _-du~n_te. todo ·q.,período. <io experime.nto -de ímunossupressão,
alterou o ·quad;~ ini~noJógico dos· animais; induzindo à diminuição da ,contagem • !::º -.. ... .;, . • • ; - •
· global de l~uqócitos· circulantes,.- bem- çoino: à dimi~uição significativa dos valores
relativ~ dos lintÓcitOS-'n'a ci;éul~çã~:sa~üínea, a·partlr do 6~dia de administração • • • • • ' . • • - ~ : ,J' • • ~ : • ' ·' • - . • •• ' • ' 1 /
do corticosteróide. Segundo-J?fNTO _(19.~.1),_ esfe ·quadro de leucopenia e . ~ - . . . -... : . •, ' . .
linfopenia, acompanhado de neutrofilià, . pode. ser usado como critério seguro na r"" · ~ \ • • 'i l • ; { .. -- · ' '.,( - ' - ... • • • .~ • '
. avaliação imunológicà q~. módelo experime11tai n;unno sub.~tido à corticoterap_ia. ·' • ... 1 ' •• •, \.
+ • • •
J • -~ ''· / .. ' ' ' '
·No decorrer do-e_sqúema de imuôossupressão dos camundongos BALB/c, ao - . ..... .
administramos - a _· dóse dtf _1:mg de· .dexamelaso_na diárias pqr camundongo, os
val~res globais de · ~ucóptps .-retomaram , a · níveis · normais na 32 · semana do
procedime~!º ~ -i~u~~Yp;~o _(ta~a _1),- ind~ndo-que pode ter havido
algum fator que levou 'a _,jão man~nção-da ~ade imunossupressora da droga. . ,
' . '
Já o esquema· de ~dm.inist~~o de 0,5mg de dexametasona por animal . -. '
permíti.u _ o desenvolvimento de um quadro de ºy:nunossupressão eficiente, nas duas
linhagens de camundongo estudadas: Apesar disso, só os camundongos da
linhagem C57BL/6, desenvolveram criptosporidiose, eli~inando oocistos nas fezes, /
' ,

42
indicando que existe um fator de predisposição genético fundamental na
susceptibilidade ou não à infecção pelo C. parvum.
E~te fato _foi inicialme~t~-d~nstr~do por RASMUSSEN ~ HEALEY (1992),
que, , ao analisarem a · s~~ptib1fid~de · de cinco diferentes linhagens de
camundongos à imunoss.up~e5;são, .seguida de in~~- com é>ocistos de e. •'
parvum, eviden~ram que os .q.,mundongps ·. da linhagem C5?BU6 são ' - ,, . .
promissores para o d~s~hvolvirnento. de in~s ·crônicas e para avaliação do· ' \ , . ' , '·, . ' ' .
potencial · de agentes anti- Cryptospóridium parvum, ao ·contrário das outras
linhag~ns estudadas: ,
' ·= , Dentre as ,.três · vias 4e éldrTiinístraçã9. utílízadas em outros trabalhos,
intraperiton~I, su~~· e oral, ~~lh~s a via subcutânea para realização . • r - .
do experimento de ímunóssupre$$ão,·<tevido .. â fàéilidad~ de padronização da dose . . ;.,
de imunossupressor administrada pará: cada camundongo e menor toxicidade . . ,.
; ... -.
Segundô GOODMAN & GILMANN_-'(1996) a v~locidade de absorção de uma . .
· droga após injeçã~ subcu.tãnea · ~-. su"cientemente · estável e lenta para
proporcionar l!m' ~ito ~ristant~. ,,_b .. qu~'prok>nga ô.e~ito da droga e diminui a , l ' -
· toxicidade, quando -comparada às vias~oral e'· intraperitoneat, .que por propiciarem . . . \ \
uma maior veJocidade.d~ absÓrção d~droga, poclem aumentar· a toxicidade desta . . . .:.~-. .... - . .
-A inoculaçãô de .2x1 Q~ .OÔCistos ·ct~ C.' pa'wm,. pela via intragástrica, apesar
de ser· 'significantemente ' mên~r-' que· . a· 'qu~ntidàde utilizada por outros
~squisadores (RASMUSSEN &·_HEf'.LEY, 1992;-PÉTRY .~i al.,_1995), foi suficiente
para induzir inf~o com .liberação de cpnsideráveis quantidades de oocistos nas r ' • •
fezes dos camundongos, . ·podendo · ser .~ma ferramenta interessante para . .. ·. ' ..
amplificação de ~uenos Jsolados, obtidos de bezerros que venham a eliminar
pequenas quantidades desse-pa,:asíto nas fezes.
O óbito de· alguns camundongos da linhage·m C57BU6, no iníéio do período
, de i~fecção, podé ter. ocorrido em função de um somatório do efeito

· . /
43
imunossu~essor da droga com o efeito da própria inf~; da mesma maneira o
óbito de camundongos· e,~ linhagem C57BU6 que for;m apen.as imun~suprimidos
(grupo e e g~po 8) indica uma maior susceptibíl~d~de de;,ses camun~ongos ã • \ 1 -- • • • ~ • •
1munossupressão com_ esse corticóide, assinalando a necessidade de uma melhor
padronizaçã<? da do~ de . i_~únossupressor e da quantidade do inóculo de e paivum, o que possiveln:,ef)te .resultaria . nºuma maior sobrévida dos· camundongos
. ·'. ' .
e numa ma,or recuperação de oocistos. (
-. j \ . I
Ressaltamos a ~impÔ,-1ãncia da realização· da imunossupressão, já que os · , • • • . j • ·-
camundongos da linhagem. BALS/c'e-C57BL/6 que -foram ·infectados sem serem 1 • • ' • . • • • • • •
submetidos a corticoteral)la ·(grupos-.-9 e ·10, respectivamente) rião eliminaram . . .• - .
oocistos nas fezes., indicando que ~xiste~urna .. r~a~tência na1ural à infecção por e. . . ·, : ... . parvum, nas duas linhagens de camundongo ~tupadas. Essa resistência· foi
marcante nos camundo~~--da linhàgem -BALB/c, que mesmo submetidos à I ,. • •' •
imunossupressão com·aexaroetasona e infectados posteriormente. (grupos 2 e 3),
não liberaram oocistos nas fezes. . ,· '
.I
Apesar da quanti<;tade de · ~ ~tos ~ecu~rados de camundo~gos ter sido
· substancialmente menor· qu~ à q~ntidade de oocistos · comumerite. recuperados
de bezerros infectados, ·consideramos vijvel a manutenção de C. párvum por meio ' • 1 • ~ ~ ' - ' - •
de sucessivas pa~r:1~ em- camundongos C57BL/6 im1,mossuprimidos com
dexametasona. . '· .. _
' ~ . o· modelo .murinó é de fácil mánipufação,, ·mai_s viável financeiramente e de
menor risco de contàmjnãção aos man~ucado~ e ào meio, e constitui uma
alternátiva v~ável' para obteilção ~ pa~itos em massa, para serem utilizados em
estudos · reíacionados a · aspedos - morfoiógicos, bioquímicos, imunológicos,
histopatológícos, terapêuticos e da relação paraslt~ospedeiro.
8 \tl~iüíE(; A Faculdade t1c (\er.cias Fa,macêulicas
UniYersidade de São Paulo


44
7 . CONCLUSÕES
Cam~ndongos da linhagem · . C578U6, quando submetidoS à
. imunossupressão com dexametasona, mostraram-se susceptíveis à infecção por
Cryptosporidium parvum; , I
Camundongos da linhagem, BALB/c mostraram-se resistentes à infecção
por C. parvum, mesmo após imunossupre~são _ com dexametasona, não
consistindo em um modelo conveniente para manutenção deste parasito;
· Oocistos de C. parvum recuperados _de camundongos infectados, foram . . '•
capazes de infectar outros camundongos C~!BU6, demonstrando a víabílídade
desse modelo de manutenção do parasito;
' O modelo. animal padronizado em no~so laboratório é uma importante
ferramenta para: realizaçã~ de estudos que possam éselarecer as várias l~cunas
que ainda , existem em relação à histopat~logia, patogenia, mecanismo de
infecção, resposta imune e terapêutica na çriptosporidióse; .

Faculdade de Ciencias Farmacéu\icaS Uni\lersidade de São Pâulo

45 .
8. RE_FERÊNCIAS. BIBLIOGRÁFICAS
. .
ADJEI M,: JO~~S , JT. ~IGGS MW, ENRIQUEZ JF. Evi~ence of thymus-
_independent -local and _5Vstemic antibody responses to Cryptosporidíum parvum • • I ' • •
infection in nude mice. l~fect. lmmun. 1997; ~7: 3947-3951.
ADJEI AA, JONES JT, E~RIQUEZ FJ. Oifferential intra-epithelial ~phocyte , .
phenotypes . ~lowing Cryp~pciridu,m · ;,arvum. challenge in suscéptible and
resistant.athymic strai,:t~ oünice_,.Parasitol. lnt 2000; 49: 119-129 . . ,. .
AGNEW DG, UMA AAM, NEWMAN RD, WUHlB T, MOORE RO, et ai.
Cryptpsporidiosis in Northeastern Brazfüan Ghíldren: association with íncreased
diarrheà morbídity. J. infect. Ois. 1998; 177:754-760.
AGUIRR-E SA.' MASON · PH, ··· PERRYMAN LE. Susceptibility of major
histocompatibiÍity cç,mplex ·(MHC) class 1- and MHC ·c1.ass 11-deficient mice to ·
Cryptospor/díum parvum infecti~n. lnfect .lmmun. 1994; 62(?):, 697-699.
. . . -
AGUIRRE SA, ·P.ERRYMAN .LE, DAVIS WC; MCGUIRRE TC. IL-4 protec1s adult \. ,. ..!. • ,. . .
C57BU6 micê· fro_m pról9nged Cryp_tosf!Oriciíum_ parv_um infection: Analysis of CD4+
n(l + IFN-r+ ·aód CD4~· ájJ+·'IL-4+ -~phocytes in gut-associated lyrnphoid ti~sue ' . .: ' . . - .
during resoiution óf ~ -'. J: ltnm~~, 1998; 1061: 1891-1900.
. .. . .: ~-· . . '
. -~\ ···-"'" ... ' -~-' ··~- .,· ·• .· -. ...
ARROWOOD MJ.'· MEAD·_;JR : :MAH~t;, JL, · STEllLING CR. Effects of immune· • ·r , ' ·· , .. •. . ~ - .• -- . - • . •. -
colostrums ~nd orally ~rfürjist_ered ân~ozoite monocional an~i~ies- on the
outcome of CryptosPQltt/iúm panium ~s in neonatal mice. lnfect lmmun . . .. . . . . . . '
1989; 57: 2283-2288.
AWAD-EL-KARIEM FM, ROBINSON HA. OYSON DA. WRIGHT S, FOX MT, . ' '
MCDONALD · . V. Differentiatíón be~· buman and animal strains of
Cryptosporidium parvum . using isoenzyme typing. Parasitology 1995; 110: 129-
132.
De acorcÍ~ com a norma preconinlda pelo Grupo de Vancouver

r 46
A YDIN Y. ÔZKUL IA. lnfectivíty of Cryptosporidíum- muris directly isolated from
the murine stomach for various laboratory a·nimals." Vet Parasitai. 1996; 66:
257-262. ;
., BAKER JR, MULLER' R, .DOLLINSON D. Opportunístic . Protozoa ín humans,
. .
Adv. Parasitai. 1998; 40: 189-~90. /
BASKERVILLE :1
A. · RAMSAY ~o. ~tLLWARD-SADLER 6H, cooK RW, . I.'. • .
CRANAç:,E 'MP: Chronic ~ncreatitis and biliary. fibrosis associated with
cryptosporidiosis in simian .AlDS: J . Cq~p. pathQ0
l. 1991; 105: 415-421 . . . ' ' \ .... -
,. . ~ ; ~
BJORNEBY JM, HUNSAKER )~D. RIGGS MW, PERRYMAN Lé. Monoclonal . . antibody imunotherapy1 íii nu~e. ~ice: persistentty i~ed with Cryptosporídíum
parvum. lnfect: lmmun. 19.91; 59: t-1727)176 . .
·'· -. ., . / ,,.
BLAG.BURN BL, DRAIN KL, LA~D TM. MOORE PH. KINARD RG, LINDSAY D . *. ~.
S, et ai. Dicationic furaQs inhibít de'(e!opment of Ciyptosporidum parvum in ."' . . . ~ · .....
HSD/ICR suckling Swiss.mice. ·J .. Parasitol. 1998;.84(4): 851-856.
\
BRASSEUR P, LEMETEIL D, BALLET JJ, · Rat model for human
cryptosporidiosis. ,J. Clin. Microbiol. 1988;. 26: 1037-1039 .
. ,.· .
BLANSHARD C, JACKS9N AM,. SHANSHON DC. FRANCIS N, GAZZARD BG. ' . .
Cryptosporidiosis in HN-seropositive-patients. Quart J . Med. 1992; 85: 813-
823. ·
BUKHARI Z, SMITH ·HV. Effect of three concentratíon techniques on viability of i . ' .
Cryptosporidium parvum oocysts recovered from bovine feaces. J . Clin.
Microbial. _199~; 33(10): 2592-2595.
CHECKEY W, GILMAN RH, EPSTEIN '"-º· SUAREZ M, DfAZ JF, CA~RERA L,
et . ai. A~yi:nptomatíc · and -symptory,atic cryptospqrtdíosis~ their acute effect on
weight gain in Peruvian children. Am. J. Epidemio!. 1997; 145: 156-163.
'·

47
. .
CHE~ W ~ .HARP JA, HARMSEN AG. Requinments for CD4+ ~ells and gamma
interferon in resolution of established CryptospÓridium parvum infection in mice. • ' - r •
lnfect. lmmun. 1993; 61(9): 3928-3932.
CHEN W, HARP _JA, HARP JA, HARMSEN AG, HAVELL EA Gamma interferon
functions in resistance _ to Cryptosporidium parvum infection in severe combined
immu,:,od~ficient mice. Jnfeét. fmmun. 1993b ; 61 : 3548-3551.
CHROUSOS GP. The ·, hypothalamic-p!tuttacy-adrenal axis and
immunemmediated inftammation. N. Eng. J . Med. 1995; 332: 1351-1.362.
' . DELAUNAY A. GARGALA. G, LI X, 'FAVENNEC L', BALLET JJ. Quantitative flow
1
cytometric evaluation of maximal Cryptosporidium parvum oocyst infectivity in a . - / .
neonatal mouse model. App. Envir .. Micmbiol. 2000; 66(10): 4315-4317.
DENG MQ, CLIVER DO. Cryptpsporidíum parvum development in ·the BS-C-1 - ' . . . )
cell line. J. Parasito!. 1998; 84(1-): 8-15.
DILLINGHAM RA. LIMA AA, GUERRANT RL CryptosporidiÔsis: epidem·iology
and impact. Microbes and infection, 4002; 4: 1059-1066.
DOYLE PS, CRAB.B j, PETERSEN C. Anti-Cryptosporidium parvum antibodies
• inhibít infectivity in vrtro and in vivo. 1nfect lmun. 1993; 61 ( 1 O): 4079-40.~4.
EGYED z, SRÉTER T, SZÉLL Z, VARGA 1. · Characterization of
Cryptosporidíum spp: ...:. recent developments ~nd future needs. Vet Parasito!. . 1
2003; 111 : 1.03-114.
ENRIQUEZ J, AVILLA CR, IGNACIO-SANTOS J, TANAKA-KIDO J, VALLEJO
à; STERLING CR. Cryptosporidium_ in~on. in Mexican children: clinicai,
nutritional, enteropathpgenic, and diagnostic evaluations. Am. J . Trop. Med.
Hyg. 1997; 56: 254-257.
'\

48
ERNEST. JA, BLAGBURN BL, UNOSAY OS. lnfection dynamics of
Cryptosporidium parvum (Apícomplexa: Cryptosporidiídae) ín neonatal mice (Mus
' masculus). J . Parasito!. 1986; 72: 796-798. . · ' '
FAUCI AS. Mechanisms,of corticosteroid action on tymphocyt~ subpopulations.
Redistribution of circulating T and E;\_ lymphoeytes to the bone marrow. lmmunol.
1975; 28: 669-680.
FAUCI AS, DALE DC. The·effect of ín viv,o hydrocortísone mi subpopufations of
human\lymph~. J. Clil'.\. lnvesi .1974; 53: 240-246. . . ,,: .
FAYER R, MOR~N U, UPTON -_ SJ . . Epíderníology of Cryptosporidium:
transmission,. detection and id~tification. lntem. · J. Parasito!. 2000; 30: 1305-\
1322. '
FLANIGAN TP, A.Jt T, MARSHALL R. soAvÉ .f( PJKAWA M, KAETZEL e .
Asséxual development of Cryp~ium parvum wtthin á diff'erentiated
human e·nteroccyte cell line. lnfect. lmmun. 1991; 59(1): 234-239. • ' 1. 1 • -~
,
FRANZEN e,· MULLER A. Cryptosporidia .and Micro~porídia - Waterbome
Disea_ses in lhe ímunocompromjsed h~t. Diagn Miçrobiol lnfect Ois. 1999; 34:
245-262.
GOOQMAN & GIL.MANN: Honnônio adrenocorticotrófico; esteróides
adrenocorticais e seus a'1á~ogos sintéticos; inibidores da síntese. e das ações
dos hormônios aô~nocorticãís Em: As báses fártJ1acológ~s da terapêutica. . . ' .. , . Rio de Jarseiro, Mcgraw-Hill. interame~na editores, .SA, 1996:1090-1091,9ª . .
edição, . / . r ' .
GUT J, PETERSEN ·e. NE~SON ~ . LEECG J. Cryptosporidium parvum in vitro
cultivation in Madin-Oart>y éanine Kidney cells. J . protozool. 199-1; 38: 72S-73S.

1 ·,
HA YWAR.D. AR. CHMURA ·K, cos~s M. Jnterferon-1 is required for innate
.immunity to Cryptosporfdíu,;, parvum ~ J. tnfect. Di;. 2000: 182: 1001-1004.
HEAL~Y MC, YAN(; s~ RASMUSSEN KR, JACKSON MK, ou e. Therapeutic • j ' , • ,,
efficacy of . paromomycin . io immunossupressed adutt mice infected with I • - .
Gryptosporidium patvum. J. Parc:asítol. 1995; 81(1):'114-116. 1
' . -HEINE J, ~ON. HW, WOODMANSEE DB. Per~istent Çryptosporidium
infection ín congenita.lly ath~ic· ~Nude) mice. lnfect. lmmun. 1984; 43{3f 856-
859.
HIJAWI NS, MELONI. BP, -~ORGAN U~. THOMPSON RCA: Complete ' -
development and long-term maintenance of Cryptosporidium parvum human
an~cattte genotypes in cell ~tture. lnt. J. Parasito!. 2001; 31: 1048-1055. ·' . ' .
. ~ i
49
HOJL YING N, MOLBAK K, JE~SEN. S. Cryptosporidium spp. , a_ frequent cause I -
of diarrhea in li~rian children. J . élin. MK:robiot 1986;-23(6): 1109~1113. .
HUNTER PR, NICHOL~ G. Epidemioiogy and ciinical fea~res of
Cryptosporidium infections ln imunoS$upresse<i patients. Clin. Microbiol. Rev.
2002; 15(1): 145-154 . .
HUNTER CA, SUBAUSTE CS, VAN CLEAVE VH, REMINGTON JS. Production 'V' l • • • • •
of y-interferon by ~tural_ k,iller ~Hs fr_om ~9)(oplasma gondii - infected SClD
mice: regulation by inténeukin~1 0, jnteneukin-12, and -~mor necrosis factor a.
lnfect. lmmuri. 1994; 62: 2818-2824.
• • 1
IVÉS N, GAZZARO B, EASTERBROOK ·P. ,The _dianging pattern of AIDS-. . . ' . .
defining illmisses with ttié introduction of highly a~e antiretroviral therapy . . .
(HAART) i!) a Londoo clinié: lnfection 2001 ~ 42:. 134-139.

KHAN IA, MATSúRA T, KASPER LH.·l~terteukin-12 enhances murine survival
against acüte toxoplasmosis. lnfect. lmmun. 1994; ·s2: -1639-1642.
KOSEC M, ALCANTA~ C, LIMA AM, GÜERRANT RL Cryptosporidiosis: an
updéite. Lancet lnfec. Ois. 2001; 1:'262-269. ,
LACROIX-~ND~-S, MANCASSOLA R, NACIRI M, lAURENT F, -Rote of
gamma interferon in chemokine expreS$ion in the illeum ot mice and in a murine
intestinal epíthelial ~n line after. Cryptosporídium parvum infection. lnfect
lmmun. 2002; 70(4):" 2090-2099. ·- , .
,,J
·' . '
LAURENT'F, ECHMANN L, SAVIOGE-TC. MoRGAN G, THEODOS Ç, NACIRI . . .
M, et ai. Cryptosporidíum parvu!J1 ·1nfectíon ·of Human intestinal epithelial cells
50
1 •• - • I
, induces the polarized s~tion. of C;X--C chemokines. lnfect. lmmun. '1997; .
65(12): 5067:-5073. '/ . '·.
__ LAWfON P, NAC(RI M, MANCASSOLA Rr PETAVY AF; ln vitro GUltivation of . . . ; I, . . . . - , . .
Cryptosporidiurp parvum. · jn the nón-adherent human monocytic THP-1 cell line. ... j • - ' •
J Eukar. Microbiol. 1997: 44(~}: ·6f3S.. .., :. , a ' •\ ,
-..:· . ' '
MACDONALD V ,' BRANC.OFT G_: Mechan,sms of innate and acquired resistance ' : . ' ' ' . ' .
to Cryptosporidiu~ ·parvum._i~fection in SCIO_ í!'ÍCe- Parasit. lmmunol. 1994; 16: _
· 315-320. '"
. .
MANGINI ACS DfAS-..RMOS GRISI SJEE, ESCOBAR AMU, TORRES DMADV, ' ' . . ' •. '
et ai. Parasitis~ por Crypt~riciium !?P · em crianças com diarréias aguda.
Rev. lnst. Med .. Trop. 1992; 34: 341-345_
'
MEAD J"f~- Cryptosporidiosis and the chaJJénges of chemotherapy. Drug
Resistance Updates 2002; 5: 47-57.
·B 1 8 LI o T e e A . .. Faculdod~ de Ciénc~s.Farmaeeu,t~S
Unive1sidade de São Paulo

51
MEAD JR, YOU X. ·Susçeptibility differences to . Cryptósporidium parvum
infection in two strains of gamma interferqn . knockout mice. J. Parasi~I. 19~8;
84(5): 1045-1048.
MELONI ijP, THOMPSON RCA Simplífied methods for obtaíning purífied .
oocysts from miei! and for growing. Cryptosporidium parvum in vitro. J. Parasito!.
1996; 82(5): 757-76.2. ,,
MONIS PT, THOMPSON. RCA. Cryptosporidíum and Giardia-zoonóses: fact or
fiction? lnfection. Gen. Evol. 2003; 3: 233-244. , ~ ..
. (
MORGAN UM, CONSTANTINE CC, O'OONOGHUE P, MELONI BP O'BRIEN·
PA, THOMPSON RCA. ~lecular characteózation of Cryptosporídi~,;, paryum ,,.. ·, ' -
from humans and other anin:ials using randOíJ1- amplified polymorphic .DNA
analysis. Am. J. ~rop. ~- H~ 1995; 52(6): 559-564, ,.
MORGAN UM,. FALL A, WARo-tA, HtJAWI N, SULAIMAN 1, FAYER R, et aJ.
Cryptosporidiutn hominis n. sp. {Apicomplexa: Cryptoporidiida~) from Homo . . -
s,apiens. J.- Eukaryot. Micfobiol,. 2Q02;_ 49(6): ·433-440_ ' - .
NEUMANN NF, GYÜRÉK LL, FINCH GR, BELOSEVIC M. lntact . '
Cryptosporidium parvum (?OCYSts jsolated after in vitro excystation are infectious
to neonatal mice. FEMS Microbiol. .Lett. 2000; 183: 331-336 . .
NORMAN FN GYÜRÉK-LL. FINCH GR, BELÓSEVIC M. lntact Cryptosporidium ' -~ . ' '
pa~um oocy~ts isola.ted after in vitro excysta~ ~re · infectious t~ neonatal
mice. FEMS Microbio!. Lett 2000; 183: 331-336.
OKAFOR JI, OKUNJI . PO. -Prevalence of Cryptosporídium oocysts ln fetal
samples of some school children in Enugu State, Nigeria. J . éommun. Ois.
1996; 28: 49-55.
. -I

\
52
OKHUYSEN PC, RICH SM, CHAPPELL CL, GRIMES KA, WI0MER G, FENG
X, et ai.· lnf~ity ·of a Cryptosporidium parvum isolate of corvine orjgin for
healthy adults and interferon-y knockout mice. J. lnfect Ois. 2002; 185: 1320- -. .
1~~ . /
OSHIRO ET, DORYAL _MEC, - NUNES VLB, SILVA MAA, SAIO LAM.
Prevalêr:tci~ dO Cryptospgridium . parvum em. crianças abaixo de 5 anos, ,. .
residente~ na zo~a ~r~an~ de Camp<Y Grande, MS, Brasil, 1996. Ver. Soe. Brás:
Med. Trop. 2000; 33(3): 277-280. /
PANCIERA RJ, THOMASSEN· RW, GARNER ·FM. Cryptosporidial infection in a • I • • •
calf. Vet Pathol. 1971; 8:·479-484: '.
PENG MM, XIAO _L, FREÉMAN AR; ARROWOOD MJ,. ESCALANTE AA,
WEL ,:-MAN AG, et . ai. __ Genetic ·potimoij)hism among eryptosporidium parvum • 11' • • :
isolates: .eviden~ of-~ dis,tinct humàn·transmissi~n cycles. Emerg. tnfect. Dis. ... i - '
1997; 3{4):·567-~73. . · ,
' . 1 . •
PENG MM, WILSON ML, ' HOLLAND -'RE, MESHNICK. SR, LAL AA, XlAO l. ' J • - -~- • • ' -
Genetic diversity Ç>f: Cryptosporjdium sw: in_ çattle in Michig~n: impli~tions for
und,ersta~ding the._transrm$Sion qynamics: Pàra~itor;'Res. 2003; 90: 1758-1790. . ' ... ~ . ' . .
~ .• ~ -,~ • - - • ' .- • ·, • J ·1 . . '
PERCH M. seóEMÂNN _ M,:,·JAKOBSEN MS, VALENTtNER-BRANTH P, • • • • 1 "'
STEINSlAND ·H,· FISCHER ,TI<, ' et at . Seven years' experience with . . . . . .~
CryptosporifJium 'paívqm) n ~Gyi,:-~.,.Bissau, Wes_t ~frica. Ann. Trop. P~ediatr. ·' ~ . . .
2001 ;_21(4): ,313-318. · ,.: ... , '. ·-._
•. · .. PERRYMAN Ü{ KAPIL·iJ:· JONES ML, HU.NT EJ. Prot~n of e.alves ~gainst
· cryptosporidiosis with immu~ bovi~ colostru~ i~ciuced ~ a Cryptosporidium ' # 1 •
parvum bovine · colostrum induced by a Cryptosporidium. parvum recombinant : - - • • I ~ • •
protein. Vaccine 1.999; 17: 2142-2149. '
.,,.-

53 PETERSEN C. Cryptosporidiosis in patients infected with the · human.
immunodeficiency virus. Clin. lnfect. Ois. 1992; 15: 903-909.
PETRY F, ROBl~.SON HA, · MCOONALD V. Muríne infection model for
maintenance and amplification of Cryptosporidium parvum oocysts. J. Clin.
Miérobiol. 1995; 33: 1922-1924 . ..._
PINTO PLS. Estud~s sobre o comportamento do S~ongyto;des vene~uefensis . '
Brumpt, 1934 em ratos submetidos a imunossupressão pela metil-prednisolona,. 1 ,,
1991 : 122. {Dissertação de Mestrado - Instituto . de Ciê~cias Biomédicas da
Universidade dê São Paulo].
REHG JE, HANCOCK ML_, WOODMANSEE DB .. Characterization of . '
cyclophosphamide-rat model of cryptosporidiosis. lnfect lmmun. 1987; 55: • 1 " ......
2669-2674.
REHG JE, HANCOCK ML, WOODMANSEE DB. ' Characterii:ation of a
dexamethasone-treated rat model. of cryptosporidial infectior.1. J. lnfect Ois.
1988; 158: 1400-1407.
RASMUSSEN KR, HEALEY MC. Experimental Cryptosporidium parvum
infections· in imunossupressed adult ·mice. lnfect. lmmun. 1992; 60(4): 1648-
1652.
RASMUSSEN KR, LARSEN NC, HEALEY MC. Complete development . of
Cryptosporidium paNum in a human endometrial ~rcinoma çell line. lnfecl
lmtnun. 1993; 61(4): 1482-1485~.
RIGGS MW. __ Cryptosporidiosís in cats, dogs, ferreis, raccoons, · opossums,
rabbits and non-human primates. l_n: Crypto~poridiosis of man and animais (J.P.
Dubey_, e .A. Speer and R'r. Fayer', eds), pp 113-120, 199_0. Boston:· CRC Press.

: "
54
RIGGS M'!'J, SCHAEFER OA, KAPIL SJ, BARLEY-MALONEY L -PERRYMAN \ ' .
LE. Ef!icacy of monoclonal antibodies · against defineó antigens for passive
immunotherapy óf chroníc gastrointesünal cryptosporídíqsis. Antimícrob. Ag.
Chemother. 2002; 46(2): 275-282. ·
SALLON S, DECKE.LBAUM RJ, SCH~ID li, HARLAP S, BftRA,S M, SPIRA DT.
Cryptospoiidium, malnutrition and chronic diarrhea ';n children. AJ.D.C. 1988; . . 142: 312-315.
scàn CA, SMITH HV, MTAMBO ~. GlBBS HA. An.~pidemíologicar study of
Ciyp~poridium pa_rvum in two herds of adult beef cattle. Vét. Parasitei. 1995; 1
57: 277 -288.
- SHEATER AL. The detection of intestinal protozoa ·and mang'e parasites by a . .
flotatiôn technic. J. Comp. Ther. 1923; 35: 265-75.
SHERW09D D, ANGUS KW, SNODGRASS DR, TZIPORI S .. Experimental
cryptosporidiosis in laboratory mice. lnfecl lmmun. 1982; 38: 471--475. ·
SLAVIN D. Cryptosporidiu~ meleagridi$ (sp. nov.). J. Comp. Pathol. 1955; 65: 1 1 • ,
262-266.
SMITH LM. BONAFONTE MT • . MEAD JR Cytokine expression and specific
lympf1ocyte proliferation in two strains of Cryptospoiidium parvum-infected
r gamma-interteron knock.out mice. J. Parasito!. 200~; 86(2): 300-307. i
SMITH LM, BONAFONTE MT, C~PBELL L,0, MEAD JR. Exogenous 1
interleukin-12 (IL-12) exarcebates. Cryptosporidium paNUm infection in ga,:nma
interferon knockout mtee. Exp. Parasito!. 2001; 98: 123-133.
TAGHI-KILANI R, SEKlA L. HAYGlASS KT. T}le role of humoral immunity in
Crypt~sporidiu;, spp. ln~on Studies with B çell~pleted mice. J . lmmunol.
1990_; 145: 1571-1576.

55
THEODOS CM,. SULLIVAN Kl, GRIFFITHS JK, TZIPORI S. Profiles óf h~aling
and nonhealing Cryptosporidium parvum~in~tion ín C57Bl/6 mice wi1h functional . '
8 and T lymphocytes: the extent of gamma _il)terf~ron ~ulation dete~ines the outéome of infection. lnfect. lmmun. 1997; 65(11): 4761--4769.
TUMWIN6 -JK, KEKITHNWA . ~ .. NABUKEERA N; AKIYOSHi DE, RICH SM,
WIDMER ~ -' et_ ai. ,ÓrypJospó~di~lll ·parvum-·i~ .children with diarrhe~ i~ M~lago
hospital, KampaJa, Uganda. Am. J.TrofJJ ~ect Hyg. 2003; 68(6):-710-715. · •. f
TZIPORI S, RAND. W, GRlFFITHS JK, wiOMER .G, CRABB J. Evaluation of an . . . . ~
animal módel· system for· cryptospor,~diosíi therapeutic'.· efficacy. of paramomycin ·
and hyperírrimune ~vir:t~ crik>~~ms-_ímm~~oglobulin> Cfin~ 1 Diag. Lab. lmmun.
1994; 1: 450-463. _. . - - . . ,, ..
- . -.:
i ·' ._.,
TZIPORI S, 'FENG X. WIPr,,tER G,. GRIMES ~. CHAPELL CL, RICH SM; et ai: • ,. ... j : ,,. , , ••
lnfectivity of. a. CfYplosporidium parv~m iso,ate Qf corvtne origin ·f.9r heafthy adutts , - ' ~· .. _,. . ' .
and ínterferon-y knockout niíC:'?;::J. lnfect 'rns: 2002;-185: 1320-1325. • " 1 - • - • : • '
,J
TZIPORI S, WARD H. Cryptbspondi'osis: bíology, pãthogenesis arid dísease. Mie. . ' '• -. .
lnfect. 2002; 4: 1047-:1058. _ - 1
UNGAR ~LP,_· · NA~f:i t . · Qu,anti{icatiQn t>f spedfiç antibody response to
C'Y:ptosporidiu,m antig~ns_by !aser.de~sitômetry. ln~t_!mmun. 1986; 53: 124-128. · ' \
UNGAR BLP SOAVE R' FAYER R 'NÀ.SH TE ErizyfOO.ímunoassay detection of ' . . ' ,_ , -· -
immunogtobulin , M and. G antibodie~ t9 Cryptr,sporidíiim in immunocompetent and -~ ·, . -.
immunocompromised persons. J tntect -Dis. 1986; 153(3): s10-51s. . - 1 • • • • - \ . - - . . . . ... .,.
. .
üNGAR BLP BURRIS·JA QUfNN CA. flNKELMAN FD. ·-New mouse models for ~. ) ' ' l •
. '-
chro~ic Cryptósporidium infection in immun~eficient hosts. lnfect l~ ~u~: 1990; . · .
58(4): 961-969.

s·6
UPTON SJ, TILLEY M, BRILLHART 0B. Effects of select medium on "in vttro·
development of Cryptosporidium parvum in HCT -8 cells: J. Clin. Microbiol. 1995;
33(2): 371-375.
UPTON SJ, TILLEY M, NESTERENKO Mv, gRILLHART OS. A simple and reliable
method of producing "in vítro" infeGtions of Cryptosporidium paNum (Apicomplexa).
FEMS Microbiol. Le~. 1994; 118: 45-50.
URBAN JF, FAYER.R, CHEN SJ, GAUSE WC. GATELY MK, FINKE~N-F. IL-
12' protects ímmunocompetent and immunodeficient neonatal . mice against
infection with Cryptosporidium parvum: J. lmmunol. 1996; 156: 263-268. . r
VERGARA-CASTIBLANCO CÂ,' FRElRE-SANTOS F, OT~lZA-LÓPEZ AM, ARES-. '
MAZ.As ME. Viability. and infecbvity of two Cryptosporidium paNUm bovine isolates
from di_fferent geographical location. Vet. Parasito!. 2000; 89: 261-267.
WATERS WR, HARP JA, WANNEMUEH,-LER MJ, CARBAJAL NY, CASAS IA. . . .
~ffects of Lactobacillus reuteri on Cryptosporidíum parvum infection of gnotobiotic
TCR-a-deficient mice. J. Eukaryot. Mi_crobfol.1~99; 46(5): 60S-61S. _,
WIDMER G, TZIPORI S, F!CHTENBÁUM CJ, GRIFFITHS JK Genotypic and
phenotypic characterization of Crypto_sporidium parvum isolates from people with 0
AIDS. J: infec. Ois. 1998~ 178: 834-840.
WIDMER G, COREY EA.. STEIN 81 GRIFFITHS JK, TZIPORI S. Host cell
apoptosis impairs CryptQsporidium parvum development J: Parasito!. 2000; 86(5):
922:..928.
WOODS KM. NESTERENKO MV. UPTÔN· SJ. Efficacy of 101 aritimicrobials and ...
other agents on the de.velopment of Cryptosporidium parvum "Yn vttro·. An. :rrop. / . ' . . '
Med. Parasito!. 1996; 90: 603-615. ·

57
XIAO L, FAYER R, RYAN U, UPTON . SJ. Cryptosporidium taxonomy: Recent
advances and i~plications for public ~eatth. Clin. Microbiol. Rev. 2004; 17: 72-97.
'
YANG S, HEALEY MC. The immunossupressive effects ot dexamethasone
administered in · drinl(jng water to C57Bl/6N mice infected with Cryptosporidim
parvum. J. Parasitei. 1993;° 79(3): 626-30 . .
YANG S, BENSON SK, OU C, HEALEY MC. lnfection of imunossupressed . .
, C57Bl/6N adu1t mice with a sin~le oocyst of Cryptosporidiu.m parvum. J. Parasito!.
2000; 86(4): 884-887.
ZU SX, FANG GD, fAYER R, GUERRANT RL. Cryptosporidíosís: Pathogenesis .
and lmmunology. Parasito!. Today 1992; 8(1): 24-27 .
.,

J
)
, , '
58
Anexo 1 "'"" Técnica de Kinyoun modificada
Reagentes:
1. Metanol absoluto 2.. Álcool ácido 3., 1 O mi de àcido suÍfúríco ,+_ 90 mi c;fe etanol. Estocar a te,:nperatura ambiente 4 .. Fucsina. . , . . 5. Verde malaquita a 3%
. 6 . .. Dissolver 3 g de. verde malaquita em 1 oo mi de ·água .d~tilada. Estocar a temperatura ambiente. _,
Procedimento:
1.
2. 3. 4.
5.
. 6. 7.
Preparar uma lâmina com uma . a duas gotas da suspensão de .fezes ~ secar a 60~.-Fixar com metanol absoJuto por 30 segundos. Corar com fucsina por um minuto. Lavar com água destilada e escorrer. Descorar com . álcool:áctdo por dojs minutos~ Lavar: com ágl,Ja destilada e escorrer. · . . Corar ·com verde ,:nalaquíta por dois minutos. Lavar com água destilada e escorrer. Deixar secar a temperatura ambiente . Examinar em aumento de 490.X.
\ ·

1 '
. . -~ Anexo 2-A Apresentação tias gaiolas, especí_ficas para isolamento dos cam_undong~ e coleta das fe2?5.
Anexo 2-B Vista superior das gai~las nas quais os camundongos foram acomodados
59

60
Anexo 2-C Instalação dos camundongos
I
. '
Anexo 2-D Disposição das fezes no fundo das gaiolas
·,. I'